Axiale Spondyloarthritis Evidenzbasiert an die Wirbelsäule
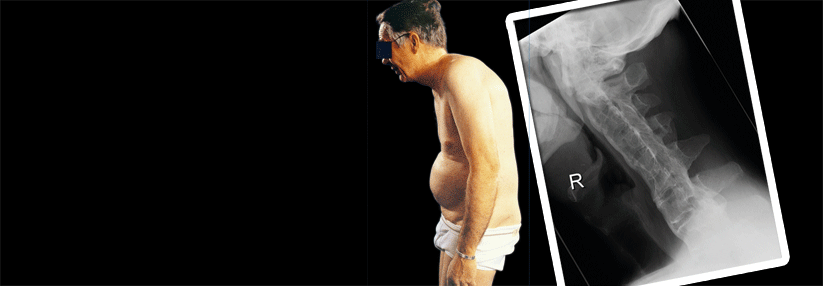
 Ausgeprägte Ankylose der Lendenwirbel bei axialer Spondyloarthritis.
© WavebreakMediaMicro – stock.adobe.com; Science Photo Library/Zephyr
Ausgeprägte Ankylose der Lendenwirbel bei axialer Spondyloarthritis.
© WavebreakMediaMicro – stock.adobe.com; Science Photo Library/Zephyr
Im Herbst 2022 formulierte die gemeinsame Taskforce von ASAS* und EULAR**, bestehend aus Rheumatologen, Epidemiologen, Physiotherapeuten und Patienten, 15 Empfehlungen zur Therapie der axialen Spondyloarthritis (axSpA). Einige Punkte aus dem Jahr 2016 haben ihre Gültigkeit behalten und wurden in das Update übernommen. Allerdings gibt es auch Neuerungen.
Empfehlung zur maßgeschneiderten Therapie
Die Behandlung der axSpA muss auf den Patienten individuell zugeschnitten werden. Zu berücksichtigen sind die Manifestationen der Erkrankung (axial, peripher oder muskuloskelettal), Komorbiditäten und psychosoziale Faktoren. Besonderer Wert wird darauf gelegt, dass die Erstdiagnose von einem Rheumatologen gestellt wird. Sie basiert auf den klinischen, laborchemischen und bildgebenden Befunden – nach Ausschluss von Differenzialdiagnosen – und nicht auf Klassifikationskriterien, betonen die Experten.
Empfehlung zum adäquaten Krankheitsmonitoring
Zum Monitoring der axSpA dienen patient-reported outcomes, klinische Befunde, Labortests und Bildgebung. Ausmaß und Häufigkeit des Monitorings richten sich individuell nach Manifestationen, therapeutischen Maßnahmen und Krankheitsaktivität. Zur Bestimmung von Letzterer wird der Ankylosing Spondylitis Disease Activity Score, kurz ASDAS, empfohlen. Röntgenbilder der Wirbelsäule weisen die röntgenologische Progression nach; aufgrund der langsamen Veränderungen reichen dabei Zwei-Jahres-Intervalle. Eine routinemäßige Magnetresonanztomografie der Iliosakralgelenke (ISG) oder der Wirbelsäule wird nicht empfohlen, ihr Einsatz ist aber zu erwägen bei unklaren Schmerzen oder Zweifeln darüber, ob eine Entzündung der ISG vorliegt.
Empfehlung zum Behandlungsziel
Jede Behandlung benötigt ein klares, vorab definiertes Ziel. Bei der axSpA besteht neueren Daten zufolge Evidenz dafür, dass ein höherer ASDAS mit einer höheren Anzahl von Syndesmophyten verbunden ist. Somit sehen die Autoren den ASDAS als angemessenen Ansatzpunkt. Wie effektiv das Treat-to-Target-Prinzip bei der axSpA ist, bleibt unklar. In einer entsprechenden Studie war es einer Standardtherapie nicht überlegen. Die Taskforce empfiehlt daher, ein ASDAS-Behandlungsziel zu bestimmen, die antientzündliche Medikation jedoch nicht ausschließlich daran auszurichten, sondern auch andere Faktoren zu berücksichtigen.
Empfehlung zur Edukation der Patienten
Alle Patienten sollten zu körperlicher Aktivität ermutigt werden, wenn nötig ist Physiotherapie zu verordnen. Prinzipiell scheinen begleitete Trainings effektiver zu sein als Übungen, die allein zu Hause durchgeführt werden. Rauchen triggert die Erkrankung und fördert die Progression. Auch wenn es keine Studien zum Nutzen einer Raucherentwöhnung hinsichtlich des Outcomes gibt, sollten Patienten ermutigt werden, diese Gewohnheit aufzugeben.
Empfehlung zu NSAR bei Schmerz und Gelenksteife
NSAR reichen oft aus, um Schmerzen und Beschwerden zu kontrollieren. Sie gelten daher als erste Wahl und können unter Berücksichtigung von Komorbiditäten und Nebenwirkungen bis zur maximalen Dosis verordnet werden. AxSpA-Patienten, die gut auf NSAR reagieren, dürfen diese zur Kontrolle der Erkrankung auch langfristig kontinuierlich einnehmen. Wenn möglich ist eine bedarfsorientierte Gabe jedoch vorzuziehen.
Empfehlung zu Opioiden und Paracetamol
Analgetika können kurzfristig verordnet werden, wenn z.B. NSAR nicht ausreichen, kontraindiziert sind oder Nebenwirkungen verursachen. Von einer Langzeittherapie raten die Experten ab.
Empfehlung zum Einsatz von Glukokortikoiden
Eine Möglichkeit zur Kontrolle lokaler Entzündungen ist nach wie vor die Injektion von Glukokortikoiden, beispielsweise bei Arthritiden und Enthesitiden. Studien zur Evidenz gibt es dazu bisher nicht. Die Taskforce geht aber davon aus, dass Glukokortikoidinjektionen effektiv sind. Sie sollten unter Ultraschallkontrolle erfolgen und nur kurzfristig eingesetzt werden. Ein chronischer systemischer Einsatz wird bei axSpA nicht empfohlen.
Empfehlung zu csDMARD bei axialer Manifestation
Disease-modifying antirheumatic Drugs (csDMARD) wie Methotrexat, Leflunomid und Sulfasalazin haben offenbar keinen Einfluss auf die rein axiale Manifestation. Daher werden sie normalerweise bei Versagen der NSAR nicht empfohlen (das Gremium lässt hier allerdings einen Interpretationsspielraum aufgrund der teueren Alternativen). Sulfasalazin hat bei Patienten mit peripherer Arthritis eine gewisse Effektivität gezeigt, daher könnten csDMARD in diesen Fällen eingesetzt werden.
Empfehlung zur Medikation in Phase 2
Eine Eskalation ist erforderlich bei hoher Krankheitsaktivität, z.B. ASDAS ≥ 2,1. Weitere Voraussetzung ist, dass mindestens zwei verschiedene NSAR über insgesamt vier Wochen keinen Effekt hatten und bei peripheren Manifestationen weder die Steroidinjektion noch ein Versuch mit Sulfasalazin erfolgreich war. Zur Intensivierung der Therapie stehen TNF-a-Blocker (TNFi), Interleukin-17A-Inhibitoren oder JAK-Inhibitoren (JAKi) zur Verfügung. Alle drei Wirkstoffklassen haben in Studien ihre Effektivität bei der axSpA bewiesen. Momentan werden Biologika den JAKi noch vorgezogen. Wegen der kardiovaskulären Sicherheitssignale von Tofacitinib bei RA-Patienten sollten JAKi bei über 50-Jährigen mit kardiovaskulären Risikofaktoren und über 65-Jährigen generell besser gemieden werden.
Empfehlung zur Medikation bei Komorbiditäten
Hat der Patient anamnestisch eine Uveitis, sind TNFi erste Wahl. Sie beugen einem Rezidiv vor. Auch bei aktiver chronisch-entzündlicher Darmerkrankung wirken TNFi positiv, wohingegen IL-17-Inhibitoren kontraindiziert sind. Aus PsA-Studien weiß man, dass Letztere Hautmanifestationen deutlich verbessern. Sie sind deshalb bei axSpA-Patienten mit schwerer Psoriasis angezeigt.
Empfehlung zum Vorgehen bei Therapieversagen
Spricht der Patient auf die Behandlung bzw. deren Eskalation nicht an, muss die Diagnose überprüft werden. Womöglich liegen Komorbiditäten wie Fibromyalgie, Depression oder Arthrose vor, die die empfundene Krankheitsaktivität erhöhen.
Empfehlung zum Switch nach Versagen des bDMARD
Zeigt das erste biologische DMARD keinen Erfolg, soll ein anderes Biologikum oder ein JAKi versucht werden. Da es keine Daten dazu gibt, welcher Wechsel zum besten Outcome führt, lässt die Taskforce alle Optionen zu. Berücksichtigt werden sollten dabei die bereits erwähnten Vorsichtsmaßnahmen bzgl. JAKi.
Empfehlung zum Tapern von bDMARD
Erreicht ein Patient unter einer Therapie mit bDMARD eine anhaltende Remission, kann das Biologikum langsam reduziert werden, z.B. durch Verlängerung der Intervalle zwischen den Injektionen. Definiert wird die Remission anhand des ASDAS (keine oder niedrige Aktivität). Ein abruptes Absetzen von Biologika kann Schübe auslösen und ist daher zu vermeiden.
Empfehlung zur Hüft-TEP und Osteotomie
Bei schwerer axSpA mit Befall der Hüfte, Behinderung, therapierefraktären Schmerzen und röntgenologisch nachgewiesenen Schäden kann unabhängig vom Patientenalter eine Totalendoprothese erforderlich werden. Ist es durch die Erkrankung zu schweren Deformitäten der Wirbelsäule gekommen, lassen sich diese in speziellen Zentren durch Osteotomien korrigieren.
Empfehlung zu ungewöhnlichen Krankheitsverläufen
Nimmt der Krankheitsverlauf plötzlich eine deutliche Wendung, müssen auch andere Ursachen jenseits der Entzündung in Betracht gezogen werden. Dazu gehören vor allem die bei Ankylose häufig vorkommenden Wirbelfrakturen. Um derartige Ereignisse nicht zu übersehen, ist unverzüglich eine Bildgebung zu veranlassen.
* Assessment in SpondyloArthritis international Society
** European Alliance of Associations for Rheumatology
Quelle: Ramiro S et al. Ann Rheum Dis 2022; DOI: 10.1136/ard-2022-223296