Der direkte Erstlinientherapievergleich klärt manches, aber nicht alles
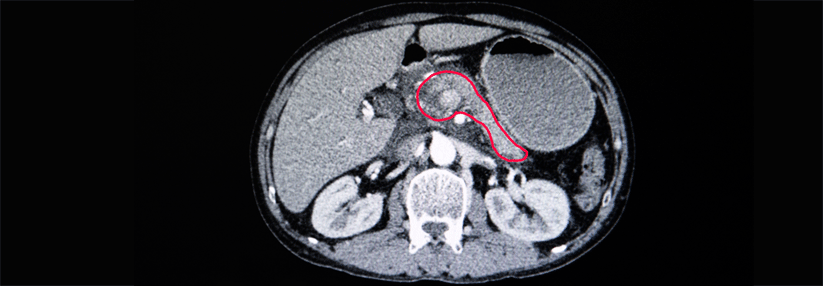
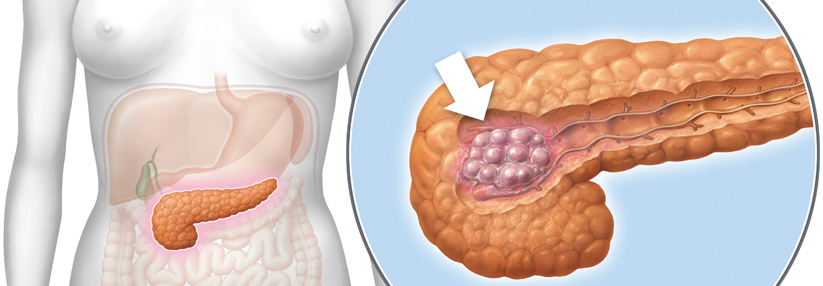
 In der NAPOLI-Studie wurde bei Patient:innen mit metastasiertem Pankreaskarzinom (mPDAC) NALIRIFOX eingesetzt.
© filins – stock.adobe.com
In der NAPOLI-Studie wurde bei Patient:innen mit metastasiertem Pankreaskarzinom (mPDAC) NALIRIFOX eingesetzt.
© filins – stock.adobe.com
Die Autor:innen der weltweit durchgeführten NAPOLI-Studie setzten als experimentelles Therapieregime NALIRIFOX bei Patient:innen mit metastasiertem Pankreaskarzinom (mPDAC) ein. Dieses bestand aus liposomalem Irinotecan (50 mg/m²), 5-Fluorouracil (2.400 mg/m²), Leucovorin (400 mg/m²) und Oxaliplatin (60 mg/m²) und wurde an den Tagen 1 und 15 in 28-tägigen Zyklen verabreicht. Als Kontrolle diente Gemcitabin (1.000 mg/m²) plus nab-Paclitaxel (125 mg/m²) an den Tagen 1, 8 und 15 in 28-tägigen Zyklen (Gem+nabPacli). Alle acht Wochen erfolgte die Kontrolle des Tumors. Die Behandlung wurde fortgeführt bis zum Progress, einer nicht akzeptablen Toxizität oder einem Widerrufen des Einverständnisses in die Studie.
Wie Prof. Dr. Eileen M. O’Reilly vom Memorial Sloan Kettering Cancer Center in New York berichtete, erhielten randomisiert 383 Patient:innen NALIRIFOX und 387 Gem+nabPacli.1 Die mediane Beobachtungsdauer der Auswertung, die sie vorstellte, betrug 16,1 Monate. Das mediane OS erreichte in Prüfarm vs. Kontrolle 11,1 Monate vs. 9,2 Monate (HR 0,83; 95%-KI 0,70–0,99; p = 0,04). Die Überlebensraten beliefen sich nach 12 Monaten auf 45,6 % vs. 39,5 % und nach 24 Monaten auf 26,2 % und 19,3 %. In allen untersuchten Subgruppen zeigte sich ein ähnlicher Trend.
Gute Ansprechraten
Das mediane PFS nach Einschätzung der Prüfärzt:innen bezifferte die Referentin in der NALIRIFOX-Gruppe mit 7,4 Monaten und in der Kontrolle mit 5,6 Monaten (HR 0,69; 95%-KI 0,58–0,83; p < 0,0001). Nach zwölf Monaten lebten ohne Progress noch 27,4 % vs. 13,9 % der Patient:innen. Nach 18 Monaten betrugen die entsprechenden PFS-Raten 11,4 % und 3,6 %.
Ansprechrate und Folgetherapien
Die Ansprechrate war mit 41,8 % vs. 36,2 % unter NALIRIFOX höher und das Ansprechen dauerte im Median länger (7,3 Monate vs. 5,0 Monate). Als Folgetherapien erhielten 41,4 % der Patient:innen der Prüfgruppe ein Gemcitabin-basiertes Regime, während 35,4 % der Kontrolle nachfolgend mit einer 5-FU-basierten Therapie behandelt wurden.
Für Prof. O‘Reilly ist NALIRIFOX das neue Referenzregime in der Erstlinie von Erkrankten mit mPDAC. Diskutant Prof. Dr. Andrew H. Ko, Universität von Kalifornien in San Francisco, hob dagegen als wichtiges Fazit hervor, dass Gem+nabPacli beim mPDAC nach dieser Studie wahrscheinlich in die Zweitlinie rücken sollte.2 Dagegen bleibe unklar, ob NALIRIFOX auch einer Therapie mit FOLFIRINIX überlegen ist, die in anderen Studien ein ähnliches medianes OS ermöglicht hatte. Er verwies auf höhere Kosten von NALIRIFOX, sah aber in der relativ niedrigen Oxaliplatindosis einen möglichen Vorteil für bestimmte Personengruppen, beispielsweise Diabetiker, da weniger Neuropathien zu erwarten sind. Die relativ guten Ansprechraten weisen darauf hin, dass NALIRIFOX außerdem besonders dort sinnvoll sein könnte, wo aus palliativen Gründen eine Zytoreduktion angestrebt wird. Den OS-Vorteil dieser Kombination in der NAPOLI-3-Studie relativierte er: Die ASCO fordert als klinisch relevant bei einem bislang zu erwartenden medianen OS von 10–11 Monaten eine Verbesserung von 4–5 Monaten mit einer anzustrebenden HR von 0,67–0,69.
Quellen:
1. O’Reilly EM et al. 2023 ASCO Annual Meeting; Abstract 4006
2. KO AH. 2023 ASCO Annual Meeting; Abstract Discussion 3: „Targets and Triplets in Pancreaticobiliary Tumors“
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).