Immunsuppression steht im Fokus der Therapie
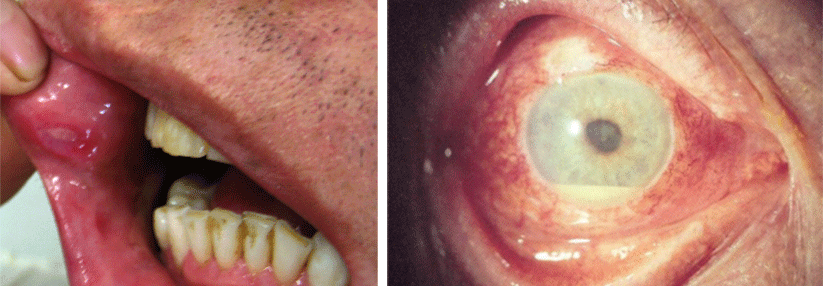
 Orale Aphthen finden sich bei fast allen Patientinnen und Patienten mit Morbus Behçet. Grund dafür ist vor allem die überschießende Aktivierung neutrophiler Granulozyten.
© Science Photo Library/Clinical Photography, Central Manchester University Hospitals NHS Foundation Trust, UK
Orale Aphthen finden sich bei fast allen Patientinnen und Patienten mit Morbus Behçet. Grund dafür ist vor allem die überschießende Aktivierung neutrophiler Granulozyten.
© Science Photo Library/Clinical Photography, Central Manchester University Hospitals NHS Foundation Trust, UK
Der Morbus Behçet ist den autoinflammatorischen Vaskulitiden zuzurechnen. Er betrifft meist Erwachsene zwischen 20 und 40 Jahren. Spezifische Autoantikörper wurden für den Morbus Behçet bisher noch nicht identifiziert. Es gibt jedoch einige genetische Veränderungen, die die Suszeptibilität für diese Erkrankung steigern. So ist das Risiko von Personen mit dem HLA-Antigen B51 etwa siebenfach erhöht. Auch Umweltfaktoren wie Schadstoffe oder Streptokokken- bzw. Herpes-simplex-Infektionen können dazu beitragen.
Vor allem auf die überschießende Aktivierung von Neutrophilen zurückzuführen sind mukokutane ulzerierende Läsionen. Fast alle Betroffenen weisen intraorale Aphthen auf, die meist schmerzhaft sind, häufig wiederkehren und im Intervall narbenfrei abheilen. Etwa 70 % der Patientinnen und Patienten entwickeln Aphthen an Skrotum, Vulva oder Vagina. Diese wiederum hinterlassen nach dem Abheilen häufig Narben.
| Behçet-Kriterien ab 4 Punkten erfüllt | |
|---|---|
| Manifestation/Symptom | Punkte |
| enorale Aphthose | 2 |
| genitale Aphthen | 2 |
| Augenmanifestation | 2 |
| Hautmanifestation | 1 |
| ZNS-Manifestation | 1 |
| Gefäßmanifestation | 1 |
| positives Pathergiephänomen | 1 |
Vaskulär zeigen sich meist Thrombophlebitiden
Die für den Morbus Behçet typische leukozytoklastische Vaskulitis spielt sich in Arterien und Venen unterschiedlicher Größe ab. Klinisch im Vordergrund stehen die Neigung zu thromboembolischen Gefäßverschlüssen sowie die Entwicklung arterieller Aneurysmen. Bei etwa einem Viertel der Betroffenen sind vaskuläre Manifestationen zu beobachten, meist Thrombophlebitiden der unteren Extremität. Auch Vaskulitiden der großen Gefäße können vorkommen. Als häufigste Todesursache beim Morbus Behçet gilt die pulmonale Vaskulitis mit Aneurysmabildung.
Zudem drohen weitere systemische Manifestationen wie Uveitis, Entzündung großer peripherer Gelenke oder Schleimhautulzerationen im Darm. Ein Fünftel der Menschen mit Morbus Behçet weist eine zentralnervöse Beteiligung auf in Form von parenchymatösen Veränderungen und thromboembolischen Prozessen.
Der Morbus Behçet wird primär klinisch diagnostiziert. Mit hoher Sensitivität und Spezifität liegt die Erkrankung vor, wenn eine Person in den ICBD*-Klassifikationskriterien 4 Punkte erreicht (s. Tabelle oben). Labor, Bildgebung und Histologie braucht man primär, um Differenzialdiagnosen auszuschließen. Im Labor sind vor allem Entzündungswerte und Marker von Organfunktionen relevant, um nach Zeichen einer Organbeteiligung zu suchen.
| Therapie nach aktuellen EULAR-Empfehlungen (2018) | |
|---|---|
| Manifestation | Therapie |
| orale/genitale Aphthen, akneiforme Läsionen | topische Glukokortikoide |
| Rezidivprävention von Haut- und Schleimhautmanifestationen | Colchicin |
| Rezidivprävention in ausgewählten Fällen | Azathioprin, Thalidomid, Interferon-α, TNF-α-Inhibitoren, Apremilast |
| Uveitis posterior | Azathioprin, Cyclosporin A, Interferon-α, TNF-α-Inhibitoren plus eventuell systemische Glukokortikoide |
| Uveitis mit drohendem Visusverlust | systemische und intravitreale Glukokortikoide plus Interferon-α oder TNF-α-Inhibitoren |
| isolierte Uveitis anterior | systemische Immunsuppression (vor allem bei jungen männlichen Patienten) |
| akute Thrombophlebitis | systemische Glukokortikoide plus Azathioprin oder Cyclophosphamid oder Cyclosporin A |
| therapierefraktäre Venenthrombosen | TNF-α-Inhibitoren, eventuell plus Antikoagulation |
| pulmonalarterielle Aneurysmen | systemische hoch dosierte Glukokortikoide plus Cyclophosphamid, bei Therapieresistenz TNF-α-Blocker und operative/endovaskuläre Reparatur |
| Vaskulitis der Aorta und periphere Aneurysmen | systemische Glukokortikoide plus Cyclophosphamid plus interventionelle Korrektur |
| gastrointestinale Manifestationen | systemische Glukokortikoide plus Mesalazin oder Azathioprin, bei Therapierefraktärität TNF-α-Blocker plus Thalidomid |
| Gelenkmanifestationen | Colchicin, eventuell plus Glukokortikoide intraartikulär, Azathioprin, Interferon-α oder TNF-α-Blocker |
| parenchymatöse ZNS-Beteiligung | systemische hoch dosierte Glukokortikoide plus Azathioprin oder TNF-α-Blocker |
| zerebrale Venenthrombose | systemische hoch dosierte Glukokortikoide plus kurzzeitige Antikoagulation |
Die Therapie hängt von der Art der Manifestation ab. Orientieren kann man sich an den EULAR**-Empfehlungen (s. Tabelle unten). Seitdem ist die Entwicklung aber weitergegangen. So haben TNF-α-Blocker an Bedeutung gewonnen. Bei schwerer Uveitis posterior und bei refraktärem Verlauf gastrointestinaler Manifestationen gelten sie heute als First-Line-Therapie. Einen positiven Effekt haben TNF-Blocker auch bei retinaler Vaskulitis gezeigt.
Apremilast ist zugelassen für die Therapie refraktärer Aphthen und hat sich zudem bei Arthritis als effektiv erwiesen, sowohl als Monotherapie als auch in Kombination mit anderen Substanzen. Erste vielversprechende Daten gibt es für Ustekinumab und Secukinumab.
Antikoagulation nur für kurze Zeit erwägen
Der Einsatz von Antikoagulanzien zur Prävention thromboembolischer Ereignisse wird nach wie vor kontrovers diskutiert. Denn sowohl Vitamin-K-Antagonisten als auch NOAK haben keinen klaren Effekt erkennen lassen, sodass die immunsuppressive Therapie bei thromboembolischen Manifestationen im Vordergrund steht. Wenn man eine Antikoagulation erwägt, sollte diese nur für kurze Zeit angesetzt werden. Und man sollte vorher abklären, ob Aneurysmen vorliegen.
* International Criteria for Behçet’s Disease
** European Alliance of Associations for Rheumatology
Zehrfeld N, Ernst D. internistische praxis 2024; 68: 217-228
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).

