Systematische und standardisierte Evaluierung der Genauigkeit von CGM
 Zur Bewertung der analytischen Leistung von CGM-Systemen werden eine Reihe von Standardverfahren benötigt.
© Issah – stock.adobe.com
Zur Bewertung der analytischen Leistung von CGM-Systemen werden eine Reihe von Standardverfahren benötigt.
© Issah – stock.adobe.com
Eine der auch international bekanntesten deutschen Forschergruppen im Bereich Diabetes-Technologie, unter der Leitung von Dr. Guido Freckmann (Institut für Diabetes-Technologie, Ulm), präsentierte am Tag vor dem diesjährigen Diabetes Technology Meeting (DTM) im Rahmen einer Vortragssitzung der International Federation of Clinical Chemistry (IFCC), einen Vorschlag der Arbeitsgruppe CGM zur Standardisierung der Testverfahren für die klinische Leistungsbewertung von CGM-Systemen. Diese Arbeitsgruppe wurde gegründet, um eine Reihe von Standardverfahren zur Bewertung der analytischen Leistung von CGM zu definieren, einschließlich der Festlegung von Studienprozeduren, Auswertung und Metriken dazu sowie der Erstellung neuer Richtlinien.
Ziel ist es, die Untersuchung der Genauigkeit von CGM-Systemen allgemein zu standardisieren, damit zukünftig alle klinischen Studien zu diesem Thema und vor allem deren Ergebnisse leichter miteinander verglichen werden können. Bisher ist dies angesichts der Unterschiede im Studiendesign und in der Methodik von CGM-Genauigkeitsstudien recht schwierig, wie Stefan Pleus (gleiches Institut) in seinem Vortrag über eine eigene, ausgesprochen aufwändige und informative Übersichtsarbeit vorstellte [1].
Ein weiterer Vortrag von Rolf Hinzmann (Roche) befasste sich speziell mit Vergleichsmessverfahren in CGM-Leistungsstudien. Da CGM-Systeme die Glukosekonzentration in der interstitiellen Flüssigkeit messen, die Ergebnisse aber mit der Glukosekonzentration im Blut verglichen werden, ist es unmöglich, eine konventionelle metrologische Rückführbarkeitskette zu etablieren. Es müssen daher analytische Faktoren der Vergleichsmethode selbst, aber auch die Probenherkunft (Matrix) berücksichtigt werden. Insbesondere wurde gezeigt, dass die physiologischen Unterschiede zwischen Glukosekonzentrationen in Blutproben unterschiedlicher Herkunft (kapillar, venös, „arterialisiert“-venös) die beobachtete Genauigkeit beeinflussen, und es wurden ihre Vor- und Nachteile für die Verwendung in CGM-Leistungsstudien diskutiert.
Zwei Merkmale von Glukosewerten sind entscheidend
Dr. Freckmann erklärte in seinem Vortrag, dass es zwei wichtige Merkmale gibt, die die klinischen Entscheidungen in Bezug auf die Glukosewerte bestimmen: 1. der Wert selber und 2. die Änderungsrate bei den Glukosewerten: Ein Glukosewert von 90 mg/dL, der mit einer Geschwindigkeit von 2 mg/dL/min fällt, erfordert eine Intervention. Der gleiche Wert von 90 mg/dL, der mit 2 mg/dL/min steigt, hingegen nicht. Daher müssen bei der Entwicklung von Testverfahren beide Faktoren berücksichtigt werden.
Eine grafische Darstellung dieser Problematik gelingt durch die Darstellung der „dynamischen Glukoseregion“ (DGR), die sowohl die Glukosewerte (Y-Achse) als auch die Änderungsraten (X-Achse) integriert (siehe Abbildung 1). Für eine Genauigkeitsprüfung schlägt die Arbeitsgruppe vor, dass ≤ 70 Prozent der Messwerte in der „neutralen“ grünen Zone liegen sollten und jeweils mindestens 7,5 Prozent der Messwerte in den Bereichen „Alarm niedrig“, „Alarm hoch“, „niedriger Blutzucker“ und „hoher Blutzucker“.
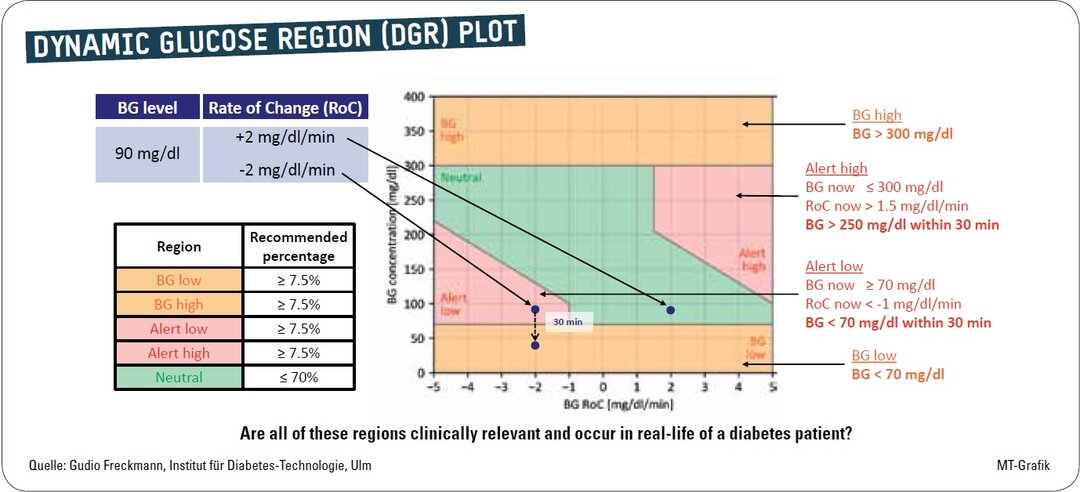
Dieser Vorschlag stellt sicher, dass die Daten aller klinisch relevanten Glukosewerte und Änderungsraten in die Genauigkeitsprüfung des CGM einbezogen werden. Bei klinischen Studien erfordert dies eine Manipulation der Glukosewerte, damit sowohl hohe als auch niedrige Werte sowie Änderungsraten innerhalb ein und derselben Kliniksitzung induziert werden. Wenn dieser Vorschlag umgesetzt wird, wird er sicherstellen, dass die relevantesten Situationen aus dem wirklichen Leben in den Genauigkeitstests untersucht werden. Die Arbeitsgruppe hofft, dass dies ein zukünftiger Standard für die Leistungsbewertung aller CGM-Systeme wird und eine entsprechende Publikation ist derzeit unter Begutachtung [4].
CE-Kennzeichnung vs. Kriterien in USA und Australien
In der gleichen Sitzung stellte John Pemberton vom Birmingham Children‘s Hospital in Großbritannien die CE-Kennzeichnung den Zulassungsbedingungen der FDA und Australiens gegenüber.
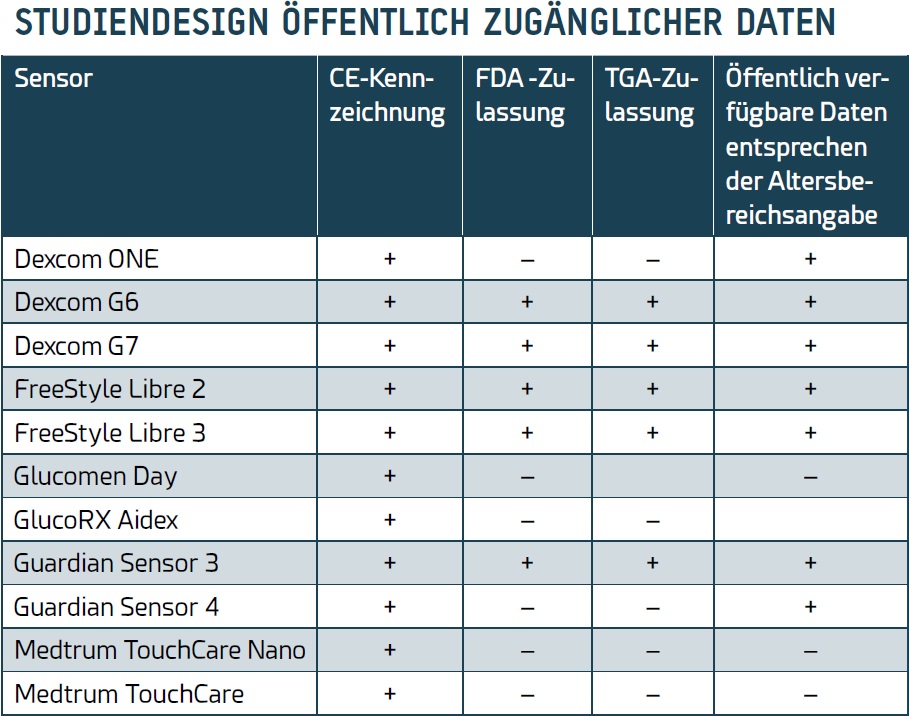
Sein Forschungsteam hat nach der vergleichenden Untersuchung mehrerer Studien festgestellt, dass mehrere CGM-Systeme eine CE-Kennzeichnung für Indikationen haben, die über diejenige hinausgehen, die durch öffentlich verfügbare Daten abgedeckt sind, was im Gegensatz zu Zulassungen in den USA und Australien steht (siehe Tabelle 1). Dort werden anscheinend strengere Kontrollen angelegt sowie eine umfassendere produktspezifische Bewertung der klinischen Daten durchgeführt. Die CE-Kennzeichnung wird als Ersatz für eine 100-prozentige klinische Datenauswertung betrachtet, was jedoch aufgrund der mangelnden Transparenz bei den für die CE-Kennzeichnung verwendeten Daten möglicherweise nicht immer der Fall ist.
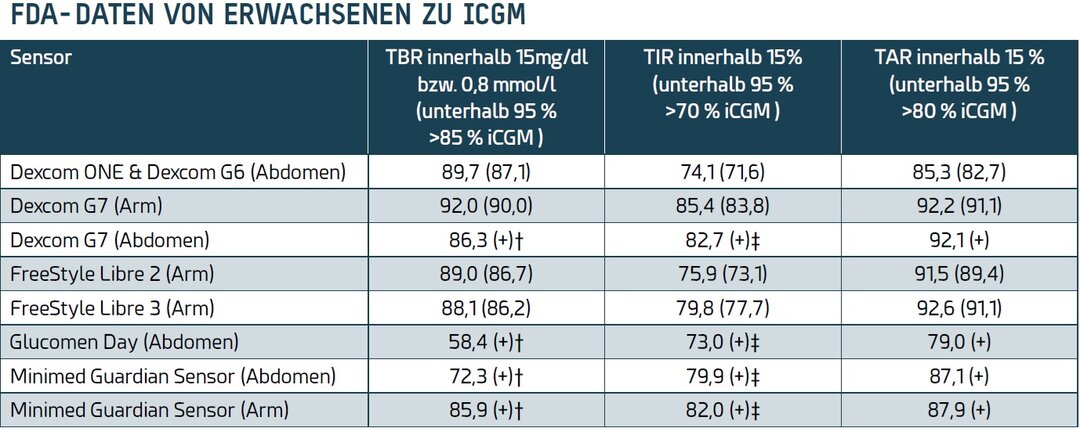
Bei der Anwendung der von der FDA in den USA veröffentlichten iCGM-Kriterien auf klinische Daten, die von britischen Herstellern bereitgestellt wurden, wurden mehrere Studienprotokolle identifiziert, die die Glukosevariabilität minimierten und dadurch die CGM-Genauigkeit bei allen Messwerten verbesserten. Bei vielen in Großbritannien erhältlichen CGM-Geräten liegt die berichtete Genauigkeit im hypoglykämischen Bereich unter derjenigen des FDA-iCGM-Standards oder Messung liegen nicht vor (siehe Tabelle 2). Seiner Ansicht nach müssten die Regulierungskriterien in Großbritannien verschärft werden. Er schlug vor, dass die nationalen Organisationen für Patientensicherheit in den EU-Mitgliedstaaten eine Untersuchung beantragen, bei der klinische Daten ausgewertet werden, die für die Zulassungen verwendet wurden. Es gibt auch eine passende Publikation des Autors dazu [2].
Neue grafische Methode für die CGM-Genauigkeit
Am ersten Tag des Diabetes-Technologie-Meetings wurde eine weitere, im Rahmen der IFCC-Arbeitsgruppe entstandene Arbeit von Manuel Eichenlaub (Institut für Diabetes-Technologie, Ulm) vorgestellt. Hier handelt es sich um eine neue grafische Methode zur Charakterisierung der Genauigkeit von CGM-Systemen namens CG-DIVA (Continuous Glucose Deviation Interval and Variability Analysis).
Die CG-DIVA basiert auf den zuvor genannten iCGM-Kriterien und vereint verschiedene gängige Verfahren in einer übersichtlichen grafischen Darstellung (siehe Abbildung 2). Dazu werden die Verteilungen der Abweichungen zwischen CGM-System und Vergleichsmethode in verschiedenen Glukosebereichen dargestellt. Weiterhin werden die Schwankungen der Genauigkeit einzelner Sensoren charakterisiert.
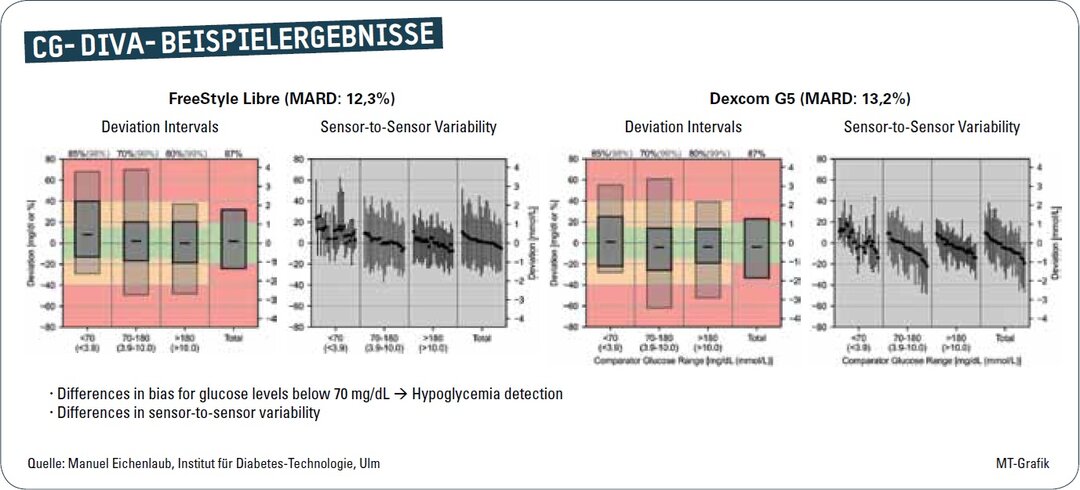
Die CG-DIVA bietet somit ein umfassendes Bild der Genauigkeit eines CGM-Systems und vereinfacht den Vergleich zwischen mehreren Systemen. Auch hier gibt es bereits eine entsprechende Publikation, eine weitere ist im Review-Prozess [3,4].
Literatur:
Freckmann G, Eichenlaub M, Waldenmaier D, Pleus S, Wehrstedt S, Haug C, et al. Clinical Performance Evaluation of Continuous Glucose Monitoring Systems: A Scoping Review and Recommendations for Reporting. J Diabetes Sci Technol. 2023:19322968231190941. Epub 20230820. doi: 10.1177/19322968231190941. PubMed PMID: 37599389.
Pemberton JS, Wilmot EG, Barnard-Kelly K, Leelarathna L, Oliver N, Randell T, et al. CGM accuracy: Contrasting CE marking with the governmental controls of the USA (FDA) and Australia (TGA): A narrative review. Diabetes Obes Metab. 2023;25(4):916-39. Epub 20230205. doi: 10.1111/dom.14962. PubMed PMID: 36585365.
Eichenlaub M, Stephan P, Waldenmaier D, Pleus S, Rothenbühler M, Haug C, et al. Continuous Glucose Deviation Interval and Variability Analysis (CG-DIVA): A Novel Approach for the Statistical Accuracy Assessment of Continuous Glucose Monitoring Systems. J Diabetes Sci Technol. 2023: 19322968221134640. Epub 20221103 doi: 10.1177/19322968221134639. PubMed PMID: 36329636
Eichenlaub M, Pleus S, Rothenbühler M, Bailey TS, Bally L, Brazg R et al. Comparator Data Characteristics and Testing Procedures for the Clinical Performance Evaluation of Continuous Glucose Monitoring Systems. Diabetes Technology & Therapeutics (submitted) 2024. doi: 10.1089/dia.2023.0465.
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).