Lymphom Eine vorbestehende klonale Hämatopoese kann hinter dem Phänomen stecken
 Seltene Fälle zeigen, dass CAR-T-Zellen Lymphome verursachen können, wobei in einem Fall eine andere Ursache vorlag.
© KeronnArt – stock.adobe.com
Seltene Fälle zeigen, dass CAR-T-Zellen Lymphome verursachen können, wobei in einem Fall eine andere Ursache vorlag.
© KeronnArt – stock.adobe.com
Bereits im November 2023 veröffentlichte die FDA ein Statement, das besagt, dass eine sekundäre T-Zell-Neoplasie nach der Therapie mit BCMA- oder CD19-gerichteten CAR-T-Zellen auftreten kann. Erst kürzlich gab es einen weiteren Bericht über 22 Fälle von T-Zell-Lymphomen bei Patient:innen, die zugelassene CAR-T-Zell-Produkte erhalten hatten. Von ihnen wiesen drei Erkrankte Tumoren auf, die das CAR-Transgen exprimierten.
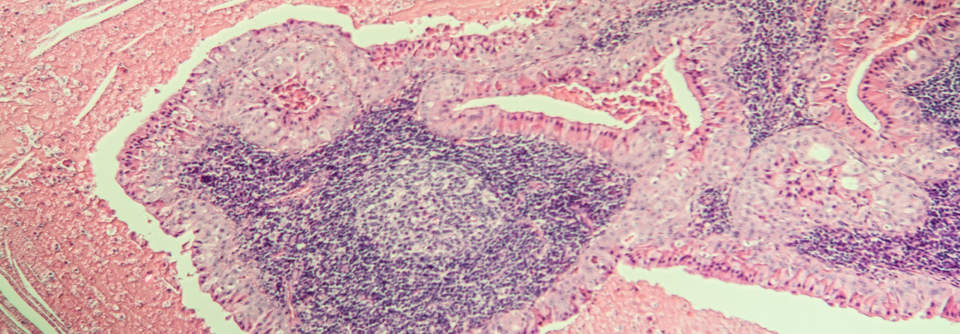
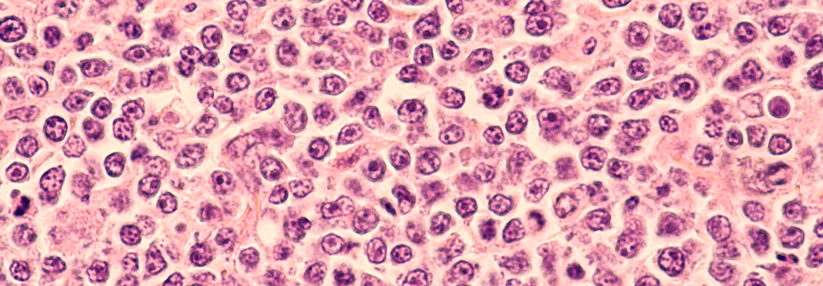
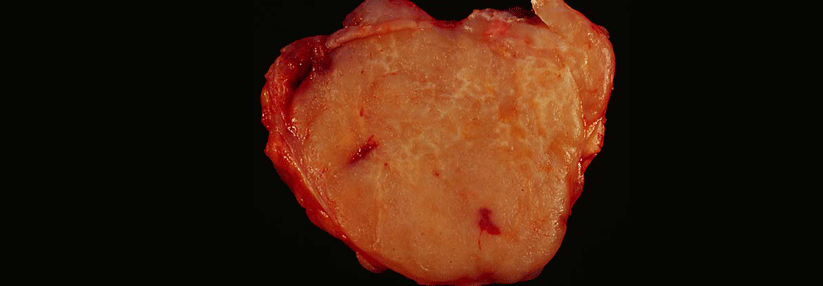
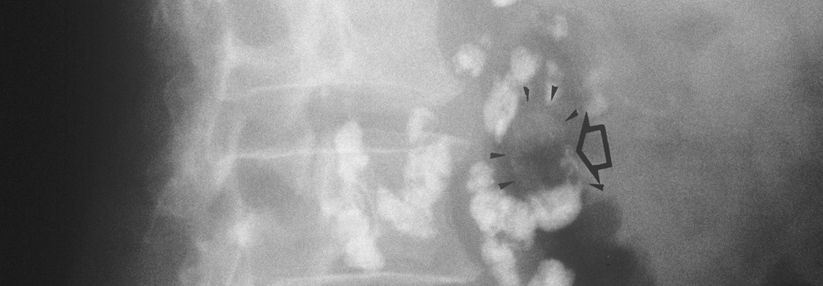
In diese Statistik ging wohl auch der Fall ein, den Kolleg:innen um Prof. Dr. Guido Kobbe, Universitätsklinikum Düsseldorf, präsentierten. Ein 60-jähriger Mann war aufgrund eines primären ZNS-Lymphoms mit CAR-T-Zellen behandelt worden, nachdem eine konventionelle Immunchemotherapie und eine autologe Stammzelltransplantation versagt hatten. Sechs Wochen nach der CAR-T-Zell-Therapie detektierten die Forschenden ein Lymphom vor allem im Knochenmark, das sich tatsächlich von den CAR-T-Zellen ableiten ließ. Aber offenbar war nicht der Einbau des CAR-Gens in der Nähe eines Onkogens für die maligne Transformation verantwortlich:
CAR-T-Zell-Mutationen analysiert
Die detaillierte Analyse der Integrationsstellen ergab, dass diese bei den normalen CAR-T-Zellen zufällig im Genom verteilt waren, sich in den Zellen des CAR-T-Lymphoms aber auf nur 13 Stellen konzentrierten. Am häufigsten waren die Gene DPF2, RAB11FIP3 und NPLOC4 betroffen, die allerdings keine bekannten Onkogene sind. Eine Mutagenese infolge der Insertion des CAR-Gens kann man den Autor:innen zufolge daher ausschließen.
In den Lymphomzellen waren weitere Gene, v. a. DNMT3A und TET2, mutiert. Ein solcher Befund weist auf eine klonale Hämatopoese hin. Tatsächlich zeigten sich diese Mutationen bereits in Blutproben des Mannes vor der CAR-T-Zell-Therapie. Höchstwahrscheinlich, so die Autor:innen, waren solche Zellen deshalb auch für die Herstellung der CAR-T-Zellen verwendet worden.
Die Forschenden schlagen vor, das somatische Mutationsmuster der generellen Hämatopoese bei weiteren Patient:innen mit CAR-T-positiven T-Zell-Lymphomen auf Alterationen in u. a. TET2 und DNMT3A hin zu untersuchen. Das Gleiche gilt für T-Zell-Produkte, die für die Generierung der CAR-T-Zellen verwendet werden.
Quelle:
Kobbe G et al. N Engl J Med 2024; 391: 1217-1226; DOI: 10.1056/NEJMoa2402730