Schlaganfall und Stroke Mimic Molekularbiologische Methoden könnten künftig bei der Differenzialdiagnose helfen
 Neue molekularbiologische Methoden können in Zukunft bei der Differenzialdiagnostik helfen.
© peterschreiber.media – stock.adobe.com
Neue molekularbiologische Methoden können in Zukunft bei der Differenzialdiagnostik helfen.
© peterschreiber.media – stock.adobe.com
Die neurologische Diagnostik kämpft derzeit noch mit drei Problemen: Sie betreffen die Genauigkeit, die Verfügbarkeit und die Individualisierbarkeit, konstatierte Dr. Steffen Tiedt vom Institut für Schlaganfall- und Demenzforschung der Universität München. Die unzureichende Genauigkeit spiegelt sich darin, dass Ärzte von vielen Therapien gar nicht genau wissen, warum sie funktionieren. Sie haben daher auch keine Parameter, um vorab zu eruieren, welcher Patient wie von der Behandlung profitieren wird. Da zudem ein Verfügbarkeitsproblem besteht – viele Patienten verlassen das Krankenhaus ohne vollständige Diagnostik – wird eine Individualisierung des diagnostischen Prozederes oft unmöglich. In den entsprechenden Algorithmen ist es auch gar nicht vorgesehen.
Für Abhilfe könnte nach Auffassung des Kollegen ein besseres Verständnis von Genen, Proteinen und Metaboliten, die neurologische Krankheitsprozesse steuern, sorgen. In der klinischen Routine nutzt man bislang aber nur einen Bruchteil des vorhandenen Potenzials: Von rund 3.500 zirkulierenden Proteinen werden gerade 20 bestimmt, von 25.000 Metaboliten nur einer, nämlich Glukose. Aber was sagen zirkulierende Proteine über das, was in den Köpfen passiert? Mittlerweile weiß man, dass das Gehirn und speziell die neurovaskuläre Einheit kein separates Kompartment ist, sondern intensiv mit der systemischen Biologie interagiert – mit dem Herzen, der Leber, dem Immunsystem, dem Mikrobiom. Dr. Tiedt plädierte deshalb dafür, verstärkt in klinischen Studien Biomaterialien für -omics-Analysen zu sammeln.
Die meisten neurologischen Krankheitsprozesse basieren darauf, dass viele genetische und exogene Faktoren akkumulieren. Die Interaktionen zu analysieren und zu einem Gesamtbild zusammenzusetzen, hilft prädiktive Modelle zu entwickeln, die präzisere Interventionen erlauben. Dass ein Screeening funktionieren kann, um ein Target zu identifizieren, zeigt das Beispiel Trimethylaminoxid: Das Phospholipid entsteht im menschlichen Darm durch bakterielle Verstoffwechselung tierischer Nahrungsmittel und wird in den Blutkreislauf resorbiert. Es wirkt atherogen und prokoagulatorisch. Der Spiegel korreliert mit dem Risiko kardiovaskulärer Komplikationen, berichtete Dr. Tiedts.
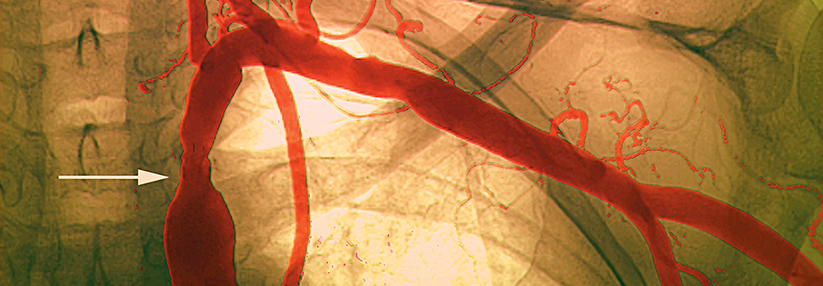
Seine Arbeitsgruppe untersucht Zusammenhänge von zirkulierendem Metabolom und Schlaganfall. In einem Kollektiv von neurologisch gesunden Patienten aus der Notaufnahme und Schlaganfallpatienten versuchen die Wissenschaftler Metabolite zu finden, die helfen können, in der Akutsituation, wenn die Bildgebung noch keine validen Resultate liefert, zwischen Schlaganfall und Stroke Mimics zu unterscheiden. Aus dem großen, fast 700 Metabolite umfassenden Panel schälten sich in mehreren Schritten vier heraus: symmetrisches und asymmetrisches Dimethylarginen (SMDA/ADMA), Pregnolonsulfat und Adenosin. „Diese Signatur schlägt die multimodale CT-Bildgebung hinsichtlich der Differenzierung der beiden Entitäten“, betonte Dr. Tiedt. Die Forscher konnten zeigen, dass die Metabolite erst in der Akutsituation ansteigen und nicht schon bei Risikokandidaten erhöht sind.
Aktuell läuft die Folgestudie namens PROMISE*, welche die Heterogenität des Schlaganfalls mittels klinischer und molekularer Phänotypisierung darstellen soll. Dazu werden Patienten bei Aufnahme, an den Tagen 2, 3 und 7 sowie nach 90 Tagen Blutproben abgenommen und das Genom, Proteom und Metabolom untersucht. Bisher sind 504 Patienten mit ischämischem und 130 mit hämorrhagischem Schlaganfall, 51 mit Stroke Mimics und 102 Gesunde eingeschlossen. Die Daten werden derzeit analysiert.
Quelle: Neurowoche 2022
* Precision Medicine in Stroke