Small Vessel Diseases als Ursache für Schlaganfall enttarnen
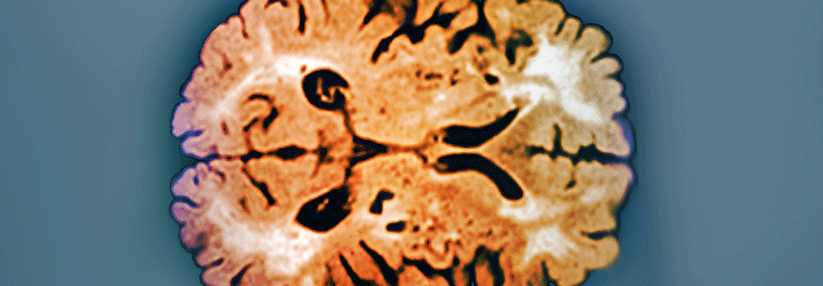 Koloriertes Kernspintomogramm eines 47 Jahre alten Patienten mit CADASIL.
© Science Photo Library/ Zephyr
Koloriertes Kernspintomogramm eines 47 Jahre alten Patienten mit CADASIL.
© Science Photo Library/ Zephyr
Small Vessel Diseases (SVD) treten gewöhnlich sporadisch auf, sind aber die häufigste monogenetische Schlaganfallursache, erklärte der britische Neurologe Professor Dr. Hugh Markus, Universität Cambridge.
Seit 1994 ist das NOTCH3-Gen bekannt, dessen Mutation für die zerebrale autosomal-dominante Arteriopathie mit subkortikalen Infarkten und Leukenzephalopathie verantwortlich ist. In den letzten Jahren haben die Forscher viele weitere Gene entdeckt, die ebenfalls monogenetische Small Vessel Diseases verursachen. Dieser Wissenszuwachs führt zwar dazu, dass immer mehr Patienten diagnostiziert und immer häufiger genetische Ursachen erkannt werden. Doch insgesamt ist die Diagnostik oft schwierig, die Therapie umso mehr.
Also hat die European Academy of Neurology eine Expertengruppe aus Genetikern, Neurologen und Patientenvertretern beauftragt, entsprechende Empfehlungen zu erarbeiten. Im März wurden das Konsensuspapier zunächst online veröffentlicht.1
SVD-Verdachtsmomente
- einschlägige Familienanamnese
- junges Erkrankungsalter
- charakteristische Neuro-Bildgebungsbefunde (z. B. frontotemporale Läsionen bei CADASIL)
- extrazerebrale und/oder systemische Begleitsymptome
- typischer klinischer Phänotyp (z. B. Alopezie und Rückenprobleme bei CARASIL)
Großes Spektrum, schwierige Diagnostik
Anhand von Fallbeispielen aus der eigenen Klinik erläuterte Prof. Markus die Inhalte der neuen Leitlinie. Die unten zusammengefassten Kasuistiken illustrieren das vielfältige Spektrum der Small Vessel Diseases und wie groß die Herausforderung ist, sie adäquat zu diagnostizieren und zu behandeln.
Fall 1: CADASIL als MS und
Demenz verkannt
Fall 2: „Hüftprobleme” durch Hirninfarkt
Fall 3: Mini-Schlaganfälle bei autosomal-dominanter CARASIL-Variante
Quelle: 1. Mancuso M et al. Eur J Neurol 2020; 27: 909-927; DOI: 10.1111/ene.14183
Kongressbericht: 6th Congress of the European Academy of Neurology (Online-Veranstaltung)
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).