Variables Immundefektsyndrom: Jeder fünfte Patient entwickelt interstitielle Veränderungen
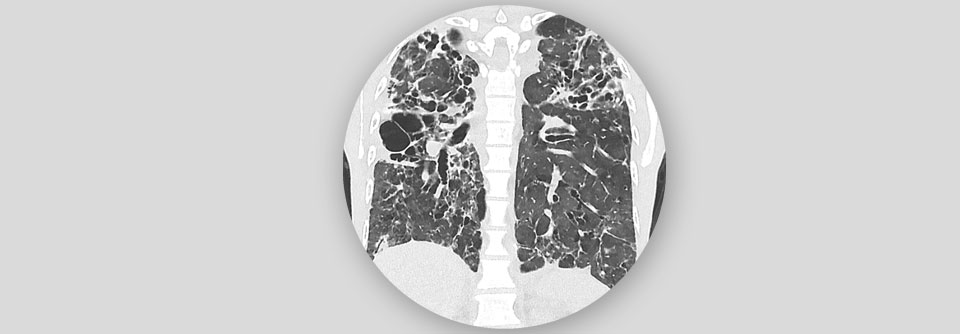 Nicht selten schlägt das variable Immundefektsyndrom auch auf die Lunge.
© wikimedia/Hellerhoff (CC BY-SA 4.0)
Nicht selten schlägt das variable Immundefektsyndrom auch auf die Lunge.
© wikimedia/Hellerhoff (CC BY-SA 4.0)
Das variable Immundefektsyndrom (CVID) ist eine primäre Antikörpermangelerkrankung mit Erniedrigung von IgG und IgA. Es betrifft prinzipiell jedes Lebensalter, beginnt aber meist im Jugend- oder jungen Erwachsenenalter. Die Prävalenz liegt bei 1:25 000. Bei jedem fünften Betroffenen finden sich monogenetische Ursachen, berichtete Professor Dr. Klaus Warnatz vom Zentrum für chronische Immundefizienzien des Universitätsklinikums Freiburg.
Klinisch entspricht das CVID einer Systemerkrankung, bei der es zu rezidivierenden bakteriellen Infektionen, aber in über 30 % der Fälle auch zu inflammatorischen bzw. Autoimmunphänomenen kommt. Mehr als 90 % der Betroffenen haben immer wieder Rhinosinusitiden, über 80 % häufige Atemwegsinfektionen. Auch gastrointestinale (ca. 30 %), urogenitale sowie ossäre Infektionen werden vermehrt beobachtet.
Zur Infektanfälligkeit kommt die Immundysregulation
Die Immundysregulation macht sich zumeist mit einer Splenomegalie und Lymphknotenvergrößerungen (zu je 40 %) bemerkbar. Außerdem ist häufiger mit einer interstitiellen Lungenerkrankung, Hepatopathie und/oder intestinalen Beteiligung zu rechnen. Autoimmunphänomene wie vor allem autoimmune Thrombozytopenie oder hämolytische Anämie finden sich bei jedem siebten Patienten. Behandelt wird die CVID durch Immunglobulinersatz und ggf. zusätzliche Immunsuppression.
Eine interstitielle Lungenerkrankung (ILD) manifestiert sich bei etwa jedem fünften CVID-Patienten. Häufiger als bei Leidensgenossen ohne ILD gesellen sich bei ihnen autoimmune Zytopenien (49 % versus 18 %), Splenomegalie (70 % vs. 39 %) und Lymphadenopathie (42 % vs. 25 %) dazu. Enteropathien sind eher vergleichbar häufig nachweisbar (27 % vs. 24 %). „Die ILD bei CVID ist somit Teil einer lymphoproliferativen Multisystemerkrankung“, sagte Prof. Warnatz.
In der Diagnostik der CVID-ILD ist neben Anamnese und klinischer Untersuchung die Lungenfunktion relevant. Als den entscheidenden Parameter in der Frühdiagnostik bezeichnete der Kollege die CO-Diffusionskapazität, die bei den Betroffenen reduziert ist. Einen zuverlässigen Labormarker für die Lungenbeteiligung gibt es nicht. Am tauglichsten scheint noch der lösliche Interleukin-2-Rezeptor zu sein. Laut Literatur spiegeln ansteigende IgM-Werte eine aktive Erkrankung wider. Die Bildgebung erfolgt klassischerweise mittels HRCT, je nach Zentrum werden aber auch die MRT und die PET-CT genutzt.
Zur Abklärung pulmonaler Infiltrate und des Keimspektrums sollte eine bronchoalveoläre Lavage erfolgen. In erfahrenen Händen hat sich die Kryobiopsie bewährt, sagte der Kollege. Manche Zentren fordern sogar eine videoassistierte Throrakoskopie (VATS).
Wann eine CVID-ILD behandelt werden soll, richtet sich nach den vorhandenen Symptomen, der Lungenfunktion und den CT-Veränderungen. Konsens besteht, immer dann zu therapieren, wenn sich die CT-Befunde verschlechtern und zusätzlich Symptome und/oder eine abnormale Lungenfunktion vorliegen. Bei allen andern möglichen Konstellationen muss man letztlich immer individuell entscheiden, erklärte Prof. Warnatz.
Zunächst wird man einen Therapieversuch mit einem Steroid (initial 0,5–1 mg/kgKG Prednisonäquivalent) machen und relativ rasch ausschleichen, um innerhalb von zwei Monaten auf < 20 mg/d zu kommen. Einige Patienten können nachhaltig von der Steroidgabe profitieren, sodass für sie erst mal keine weitere Behandlung nötig ist. Bei den anderen muss man über weitere Optionen nachdenken. Da es keine evidenzbasierten Strategien gibt, wird abhängig vom Einzelfall meist auf Rituximab mono oder in Kombination mit Azathioprin bzw. Mycophenolatmofetil gesetzt.
Quelle: 8. Symposium Seltene Lungenerkrankungen im virtuellen Fokus
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).