Bei Zirrhose auf Mangelernährung screenen
 Bei Patienten mit Leberzirrhose reicht es nicht aus, den Body-Mass-Index zu berechnen.
© iStock/eranicle; Daniel Berkmann – stock.adobe.com
Bei Patienten mit Leberzirrhose reicht es nicht aus, den Body-Mass-Index zu berechnen.
© iStock/eranicle; Daniel Berkmann – stock.adobe.com
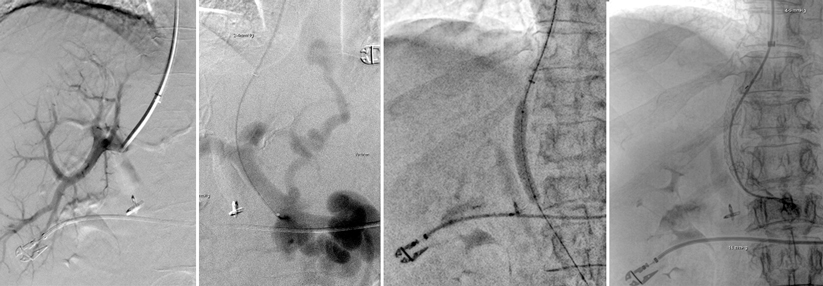
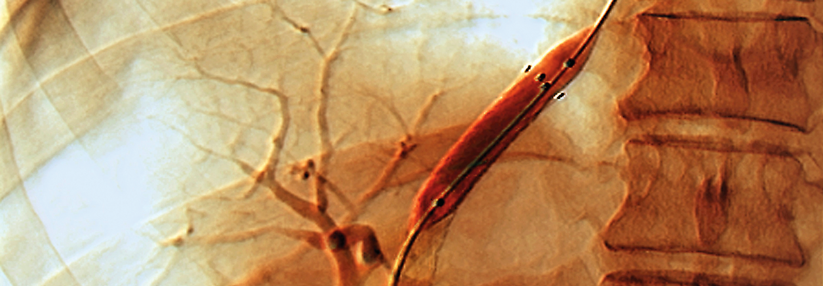
Bei vielen Zirrhosepatienten deckt die spontane Nahrungsaufnahme nicht den Bedarf. Im fortgeschrittenen Erkrankungsstadium findet sich zudem sehr häufig ein erheblicher Eiweißmangel, der eine Sarkopenie und reduzierte Muskelfunktion nach sich zieht.
Mangelernährung und Sarkopenie sind nachweislich mit einer höheren Sterblichkeit und höheren Komplikationsraten assoziiert. Außerdem ist das Überleben nach Transplantation und anderen Eingriffen bei mangelernährten Zirrhosepatienten verringert. Schließlich ist bekannt, dass Funktionen der Leber durch Mangelernährung eingeschränkt werden und sich durch Ernährungstherapie wieder verbessern lassen.
Körperzusammensetzung und Energiebilanz beurteilen
Es wird daher empfohlen, alle Patienten mit Leberzirrhose systematisch auf das Vorliegen einer Mangelernährung zu screenen. Aufgrund der Komplexität der Erkrankung reicht eine Bestimmung des BMI hierfür nicht aus; vielmehr müssen auch die Energie- und Nährstoffbilanz sowie die Körperzusammensetzung beurteilt werden. Als Screening-Instrument eignet sich besonders das „Royal Free Hospital-Nutritional Prioritizing Tool“ (RFH-NPT), das speziell für Zirrhosepatienten entwickelt und validiert wurde. Weitere Instrumente für Krankenhauspatienten sind der NRS-2002 und der MUST.
Nach der Diagnose einer Mangelernährung ist im nächsten Schritt zu überprüfen, ob eine Sarkopenie, also eine Reduktion von Muskelmasse und -kraft, vorliegt, denn diese geht mit einer schlechteren Prognose einher. In der Praxis eignen sich dafür die Bestimmung des Phasenwinkels mittels Bioelektrischer Impedanzanalyse oder die Messung der Handkraft. Zudem kann die Gebrechlichkeit mit dem Chair-Stand-Test, anhand der Gehgeschwindigkeit oder der Short Physical Performance Battery beurteilt werden. Ist ein aktuelles CT des Abdomens verfügbar, lässt sich daraus der Skelettmuskelindex als Maß für die Muskelmasse ermitteln.
Bei Patienten mit Leberzirrhose ist der 24-Stunden-Energiebedarf erhöht, der meist durch verminderte körperliche Aktivität ausgeglichen wird. Außerdem weisen Betroffene eine verringerte hepatische Glukosesynthese, verminderte Glykogenspeicher und eine verringerte Glykogensynthese auf.
Bereits früh im Erkrankungsverlauf findet sich vielfach eine Insulinresistenz, die zu einer verminderten Aufnahme von Glukose und Verwertung führt. Überdurchschnittlich viele Zirrhotiker entwickeln einen Diabetes mellitus.
Bereits während einer Nahrungskarenz über Nacht kommt es zu einer Entleerung der Glykogenspeicher und in der Folge zu einem vermehrten Abbau von Proteinen und zu einem Eiweißmangel. Typisch sind zudem eine Hyperhydratation, Kochsalzüberladung und häufig auch ein Mangel an Mikronährstoffen wie beispielsweise B-Vitamine oder Zink.
Für die Nacht eignet sich Trinknahrung
Vorrangiges Ziel der Ernährungstherapie ist es daher, sowohl eine adäquate Energie- als auch eine ausreichende Eiweißaufnahme zu gewährleisten. Empfohlen wird eine Gesamtenergieaufnahme von 30 kcal/kg Körpergewicht sowie eine Proteinzufuhr von 1,2 g (stabile Zirrhose) bis 1,5 g (Mangelernährung und dekompensierte Zirrhose) pro kg Körpergewicht pro Tag.
Um einen Eiweißkatabolismus so weit wie möglich zu vermeiden, sind mehrere Mahlzeiten und eine Spätmahlzeit sinnvoll. Nachts sollte zur Verkürzung der Nahrungskarenz Trinknahrung eingenommen werden. Die frühere Empfehlung einer Eiweißrestriktion bei Patienten mit hepatischer Enzephalopathie gilt nicht mehr. Spurenelemente und Vitamine sollte man vor allem während der ersten zwei Behandlungswochen großzügig supplementieren.
Ist eine ausreichende Ernährung auf oralem oder enteralem Wege nicht möglich, ist eine parenterale Ernährung inklusive aller Makro- und Mikronährstoffe angezeigt. Mit Glukose sollten 50–60 % und mit Fett 40–50 % des Nichteiweißenergiebedarfs gedeckt werden. Patienten mit kompensierter Zirrhose können Aminosäure-Standardlösungen erhalten; bei Patienten mit höhergradiger hepatischer Enzephalopathie, insbesondere nach gastrointestinaler Blutung, sollten leberadaptierte Aminosäure-Komplettlösungen eingesetzt werden.
Eine postoperative parenterale Ernährung nach abdominellen Eingriffen verringert nachweislich das Risiko für Komplikationen und verbessert den Eiweißstoffwechsel. Gleiches ist für eine enterale Ernährung anzunehmen. Nach einer Transplantation sollte man zeitnah innerhalb von 12–24 Stunden normales Essen und/oder eine enterale Ernährung beginnen.
Quelle: Plauth M. Dtsch Med Wochenschr 2019; 144: 1267-1274; DOI: 10.1055/a-0753-6081