Pleuramesotheliom Negative Ergebnisse einer Phase-3-Studie dürften noch nicht das Ende bedeuten
 Die Erhaltungstherapie mit dendritischen bei Pleuramesotheliom Patient:innen scheint noch weiter optimiert werden zu können.
© VS artdesign – stock.adobe.com
Die Erhaltungstherapie mit dendritischen bei Pleuramesotheliom Patient:innen scheint noch weiter optimiert werden zu können.
© VS artdesign – stock.adobe.com
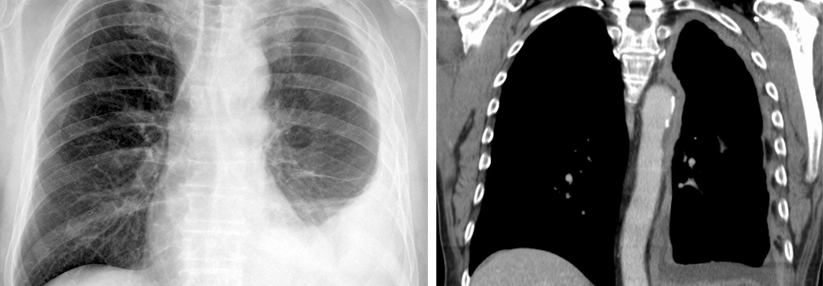
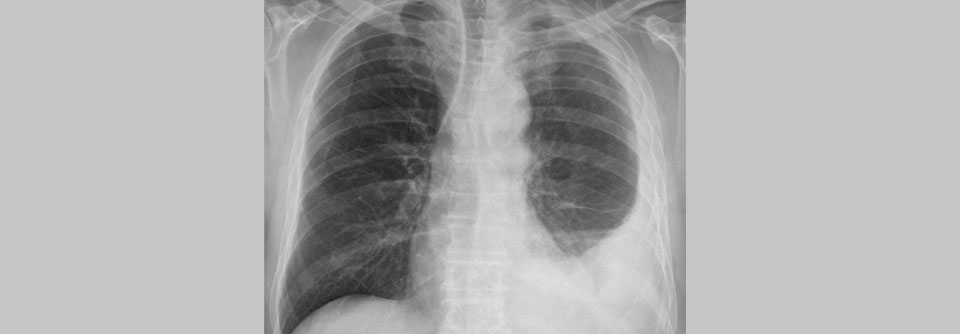
Das maligne Pleuramesotheliom ist nach wie vor eine therapeutisch schwierige Entität. Auf CPI spricht es meist gar nicht oder nur für relativ kurze Zeit an. Dass die Funktion der dendritischen Zellen in diesen Tumoren unterdrückt ist, führte niederländische Onkolog:innen dazu, autologe dendritische Zellen von Patient:innen mit einem allogenen Tumorlysat zu beladen; dieser Ansatz, der eine Aktivierung des Immunsystems gegen den Krebs induziert, wird neben dem Pleuramesotheliom unter anderem bei Erkrankten mit abdominellem Mesotheliom und Pankreaskarzinom erprobt.
Positive Ergebnisse in Vorarbeiten führten zur Phase-3-Studie DENIM, in der die Autor:innen eine Vakzinierung mit allogen stimulierten, autologen dendritischen Zellen als Erhaltungstherapie testeten. Die insgesamt 176 eingeschlossenen Patient:innen mit Pleuramesotheliom mussten nach einer Standardchemotherapie mindestens eine Krankheitsstabilisierung aufweisen. Sie erhielten daraufhin randomisiert entweder die dendritischen Zellen oder lediglich die beste verfügbare Supportivtherapie.
Besser auf den zweiten Blick?
Die Ergebnisse waren auf den ersten Blick enttäuschend und negativ, berichtete Prof. Dr. Joachim Aerts, Erasmus MC Cancer Centre, Rotterdam: Die Teilnehmenden vertrugen die Therapie zwar gut; nach median 15 Monaten Follow-up ergab sich hinsichtlich des primären Endpunkts OS aber ein kleiner numerischer Vorteil für den Kontrollarm mit median 18,3 Monaten versus 16,9 Monate unter den dendritischen Zellen (p = 0,62). Das mediane PFS betrug 3,2 Monate vs. 5,4 Monate zugunsten der Immuntherapie, aber der Unterschied fiel nicht signifikant aus (p = 0,60). Dazu sind allerdings mindestens drei Dinge zu bemerken, so Prof. Aerts:
- Im Gegensatz zu früheren Untersuchungen hatte sich die Frist zwischen dem Ende der Chemotherapie und der ersten Injektion der Zellen auf 11,6 Wochen verlängert – bedingt vor allem durch die Randomisierungs-Prozedur und zusätzliche Sterilitätstests. Dadurch hatte ein Teil der Patient:innen zu Beginn der Immuntherapie bereits eine Krankheitsprogression erlitten.
- Personen mit geringer Tumorlast und einem ECOG-Performancestatus von 0 hatten ein beinahe doppelt so langes medianes PFS (4,8 Monate in der Kontrolle vs. 8,8 Monate im Prüfarm). Darüber hinaus wiesen diejenigen Personen ein längeres PFS auf, bei denen die Vakzine zu einer Proliferation von CD4+ T-Zellen mit Hochregulierung des Ki67-Antigens geführt hatte.
- Die Überlebensdauer in der Kontrolle fiel überdies länger aus als das aus historischen Daten zu erwarten gewesen wäre – bedingt mutmaßlich durch einen hohen Anteil an Erkrankten in diesem Arm, die als Zweitlinientherapie PD1-Inhibitoren erhalten hatten.
Schließlich öffnet die gute Verträglichkeit der Vakzine Möglichkeiten der Kombination mit anderen Therapien.
Quelle:
Aerts J et al. IASLC WCLC 2023; OA02.05