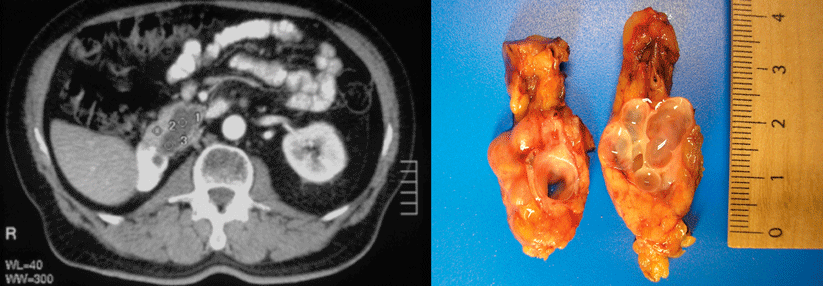
Patienten mit zystischer Pankreasraumforderung gehören ins MRT
 Handelt es sich um Zysten ohne Risikofaktoren, reicht zunächst eine MRT-Kontrolle einmal im Jahr.
© iStock/choja
Handelt es sich um Zysten ohne Risikofaktoren, reicht zunächst eine MRT-Kontrolle einmal im Jahr.
© iStock/choja
Aufgrund der stetig verbesserten Bildgebung sowie der gestiegenen Lebenserwartung nimmt die Inzidenz zystischer Pankreasläsionen zu. Prinzipiell unterscheidet man zwischen nicht-neoplastischen und neoplastischen Zysten, erläutern Professor Dr. David Anz und Kollegen vom Klinikum der Universität München. Innerhalb der letztgenannten Gruppe wiederum ist zwischen serösen und muzinösen Zysten zu differenzieren. Seröse Zystadenome und Pseudozysten bleiben immer gutartig, wohingegen muzinöse Läsionen wie intraduktale papillär-muzinöse Neoplasien (IPMN), muzinös-zystische Neoplasien, solid-pseudopapilläre Neoplasien sowie zystische neuroendokrine Tumoren Potenzial zur malignen Transformation haben.
Eine zuverlässige Differenzierung des Zystentyps allein anhand der Bildgebung ist meist nicht möglich, schreiben die drei Autoren. Bei therapeutischer Konsequenz hat daher eine diagnostische Punktion zu erfolgen. Im Fall einer IPMN lässt sich dabei visköses spinnbares Sekret mit erhöhtem Gehalt an karzinoembryonalem Antigen (CEA) und Lipase gewinnen. Pankreaspseudozysten sind im Gegensatz zu den neoplastischen Zysten nicht mit Epithel ausgekleidet. Sie enthalten zwar ebenfalls viel Lipase, jedoch nur wenig CEA. Pathogenetisch entstehen sie vermutlich infolge einer Gangruptur bei akuter oder chronischer Pankreatitis oder aufgrund von Obstruktionen der Ausführungsgänge im Rahmen postentzündlicher Veränderungen.
Differenzierung anhand von Lipase- und CEA-Gehalt
Während IPMN in der Regel asymptomatisch bleiben, verursachen insbesondere große Pseudozysten in einigen Fällen Schmerzen oder Verdrängungserscheinungen benachbarter Strukturen oder können durch Infektionen oder Einblutungen kompliziert werden. Selbst große Pseudozysten lassen sich gut endoskopisch drainieren, wohingegen IPMN reseziert werden müssen.
Muzinös-zystische Neoplasien zeichnen sich durch einen niedrigen Lipase- bei hohem CEA-Gehalt der Zystenflüssigkeit aus. Ihr Malignitätsrisiko hängt im Wesentlichen von der Läsionsgröße ab und steigt erst ab einem Durchmesser von mehr als drei Zentimetern an. Die seltenen serösen Zystadenome weisen niedrige Lipase- und CEA-Werte auf. Trotz ihrer Benignität können sie aufgrund ihrer Größe oder Symptomatik eine Operationsindikation darstellen. Die auch als Frantz-Tumoren bezeichneten solid-papillären Neoplasien sollten grundsätzlich operativ entfernt werden.
Häufig fallen Pankreaszysten erstmals im Ultraschall auf. Für die Differenzierung und Verlaufskontrolle der Befunde eignen sich radiologische Schnittbildverfahren jedoch besser, erläutern Prof. Anz und Kollegen. Zur Primärdiagnostik und zum Monitoring bevorzugen sie die MRT und nutzen die CT zusätzlich bei Unklarheiten bei gegebener therapeutischer Konsequenz. Eine ergänzende Endosonographie halten die drei Experten bei größeren, symptomatischen Zysten oder bei Verdacht auf prämaligne und maligne Läsionen für sinnvoll. Hohen Stellenwert messen sie der endosonografisch gesteuerten Feinnadelaspiration und -biopsie bei.
Eine Therapie ist grundsätzlich bei symptomatischen Zysten und bei erhöhtem Malignitätsrisiko angezeigt. Gemäß der europäischen Leitlinie gelten folgende Indikatoren als absolute Indikation zur Zystenresektion:
- Zytologie mit Malignitätsnachweis oder High-Grade-Dysplasie
- suspekte solide Gewebemasse in Assoziation zur Zyste
- durch Zyste bedingter Ikterus
- intraluminale perfundierte Knoten > 5 mm
- Dilatation des Pankreashauptgangs > 10 mm
Kriterien für mäßig erhöhtes Risiko und eine relative Operationsindikation sind:
- Zystengröße > 4 cm
- Zystenwachstum > 5 mm pro Jahr
- Erweiterung des Pankreashauptgangs auf 5–10 mm
- intraluminale perfundierte Knoten < 5 mm
- erhöhte Ca19-9*-Serumspiegel
- Symptome (Erstdiagnose Diabetes mellitus, akute Pankreatitis)
Bei Zysten ohne Risikofaktoren sind halbjährliche, bei stabilem Befund später auch jährliche MRT-Verlaufskontrollen angebracht, gegebenenfalls ergänzt durch die Endosonographie, schreiben die Autoren. Die Entscheidung über ein abwartendes bzw. operatives Vorgehen sollte dabei immer durch ein interdisziplinäres Team mit Erfahrung im Umgang mit zystischen Pankreasläsionen getroffen werden.
* Carbohydrate-Antigen 19-9
Quelle: Anz D, Seidensticker M, Mayerle J. „Vorgehen bei Nachweis von zystischen Pankreasraumforderungen“, Dtsch Med Wochenschr 2021; 146: 253-269; DOI: 10.1055/a-1221-7266 © Georg Thieme Verlag KG Stuttgart, New York