2023 wartet mit geänderten Definitionen und gestrafften Behandlungsempfehlungen auf
 Symptome und Zeichen einer Exazerbation sollen Ärzte nicht nur abschätzen, sondern messen, z. B. mithilfe von visuellen Analogskalen. (Agenturfoto)
© Andrey Popov – stock.adobe.com
Symptome und Zeichen einer Exazerbation sollen Ärzte nicht nur abschätzen, sondern messen, z. B. mithilfe von visuellen Analogskalen. (Agenturfoto)
© Andrey Popov – stock.adobe.com
Unter dem Oberbegriff COPD wird bekanntlich ein heterogenes Spektrum von Krankheitsbildern zusammengefasst, die sich sowohl ätiologisch als auch klinisch unterscheiden. GOLD trägt dem mit einer neuen Taxonomie Rechnung:
- COPD-A steht für COPD mit Asthma,
- COPD-G für genetische determinierte Formen, z.B. bei Alpha-1-Antitrypsinmangel.
- Eine durch (E-)Zigaretten oder Cannabisrauch induzierte COPD heißt jetzt COPD-C.
- Bei einer COPD-I sind Infektionen im Spiel,
- bei COPD-P Umweltbelastungen.
- COPD-U bedeutet, dass die Ursachen nicht bekannt sind.
Praktische Konsequenzen hat diese Klassifikation aktuell nicht. Sie soll vor allem bewusst machen, dass COPD mehr ist als Raucherhusten, und den Weg für stärker diversifizierte klinische Studien bereiten.
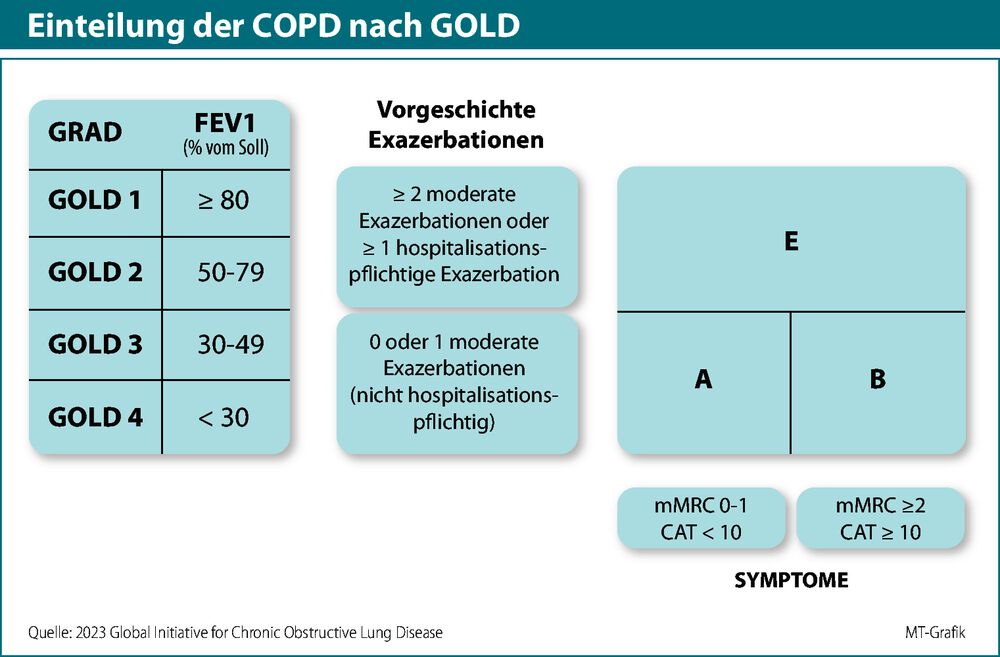
Wer das Vierfelderschema nicht leiden konnte, in dem man die COPD anhand von Symptomlast und Exazerbationen in Gruppe A bis D eingeteilt war, darf sich freuen: Das neue Schema hat nur noch drei Felder (s. Grafik unten). Es übernimmt Gruppe A und B, also die Nicht-Exazerbierer mit wenig oder vielen Symptomen, fasst aber Gruppe C und D zu Gruppe E zusammen.
E steht dabei für Exazerbationen. Das soll deutlich machen, welch hoher prognostischer Stellenwert Exazerbationen bei COPD zukommt.
Die wichtigste Änderung bei der Pharmakotherapie besteht darin, dass Fixkombinationen aus inhalativem Steroid und lang wirksamem Beta-2-Mimetikum verschwunden sind. „Besteht die Indikation für ein ICS, hat sich das Triple LABA/LAMA/ICS als überlegen erwiesen im Vergleich zu LABA/ICS“, konstatiert das GOLD-Komitee. Die Therapie wird dadurch einfacher: Erscheint ein ICS notwendig, wird es nur noch innerhalb der Tripletherapie gegeben. Laut Registern wie COSYCONET und DACCORD exazerbieren aber höchstens 20 % der Patienten so häufig, dass ein ICS infrage kommt.
Die Initialtherapie orientiert sich wie bisher daran, zu welche Gruppe ein Patient gehört. Gruppe A erhält „einen Bronchodilatator“. Für eine genauere Aussage bzw. Strategie fehlen schlicht die Daten.
Mortalitätsvorteil auch durch Rauchstopp und Reha
Für die Gruppen B und E stellt die duale Bronchodilatation mit LABA/LAMA die bevorzugte Option dar. Bei Patienten mit Eosinophilenzahlen > 300/µl kann man über eine Dreifachkombination nachdenken (mehr dazu im Interview). GOLD weist darauf hin, dass die Triples bei symptomatischen Patienten mit häufigen und/oder schweren, also hospitalisierungspflichtigen Exazerbationen einen Mortalitätsvorteil gezeigt haben. Das leisten nicht-medikamentöse Maßnahmen ebenfalls, allen voran Rauchstopp und pneumologische Reha, unter bestimmten Voraussetzungen auch Sauerstofftherapie, nicht-invasive Beatmung und Lungenvolumenreduktion.
Erweist sich die Initialtherapie als unzureichend, entscheidet das Kardinalproblem des Patienten, wie eskaliert wird. Dominiert die Atemnot, bleibt es bei der Bronchodilatation. Falls noch nicht an Bord, gibt es einen zweiten Bronchodilatator dazu. Reicht auch das nicht aus, soll über einen Inhalator- oder Wirkstoffwechsel nachgedacht werden, vor allem aber darüber, ob die COPD wirklich wichtigste und einzige Ursache der Dyspnoe ist. Als relevante Differenzialdiagnosen nennt GOLD Herzinsuffizienz, Pneumonie und Lungenembolie. Medikamentös ist mit den Bronchodilatatoren das Ende der Fahnenstange erreicht, die Eskalation zum Triple wird für Patienten mit dem Leitsymptom Atemnot nicht empfohlen.
Anders bei denen, die häufig und/oder schwer exazerbieren. Auch bei ihnen kann zunächst auf LABA/LAMA eskaliert werden, wenn die Eosinophilenzahl < 300/µl liegt. Mehr Eos im Blut rechtfertigen den Schritt zum Triple ohne diese Zwischenstufe. Noch einmal: Der Wechsel von Bronchodilatator mono auf LABA/ICS ist keine Option.
Exazerbiert der Patient unter einer dualen Bronchodilatation weiterhin, hängt das weitere Prozedere von der Eosinophilenzahl ab. Liegt sie über 100/µl wird auf ein Triple eskaliert. Bei Werten < 100/µl ist dagegen vom ICS kein Benefit zu erwarten. Dann müssen andere Optionen versucht werden, etwa Roflumilast bei einer FEV1< 50 % und chronischer Bronchitis oder Azithromycin bei Exrauchern.
Auch des leidigen Themas Exazerbationen haben sich die GOLD-Experten angenommen. Bisher definierte die Therapie die Komplikation und deren Schweregrad anhand subjektiver Einschätzungen von Arzt und Patient post hoc; das soll sich ändern.
Definiert wird eine Exazerbation nicht mehr als „Verschlechterung, die zusätzliche Therapie auslöst“. Sie wird jetzt als als symptomatisches Ereignis mit mehr Atemnot, Husten und Auswurf gesehen, das sich innerhalb von maximal 14 Tagen verstärkt und mit Tachypnoe und Tachykardie einhergehen kann.
Symptome und Zeichen einer Exazerbation sollen Ärzte nicht nur abschätzen, sondern messen, z. B. mithilfe von visuellen Analogskalen. Um den Schweregrad zu bestimmen, schlägt GOLD objektive Kriterien vor wie Herz- und Atemfrequenz, Sauerstoffsättigung oder besser noch Blutgase sowie CRP. Wichtig an jedem Punkt des Krankheitsgeschehens, besonders bei Verdacht auf eine akute Exazerbation: Differenzialdiagnosen sind sorgfältig zu prüfen und auszuschließen. GOLD nennt explizit Herzinsuffizienz, Lungenembolie und
Pneumonie.
GOLD-Report; Quelle: www.goldcopd.org
„Wenn es mit LABA/ICS gut läuft, gibt es keinen Grund, etwas zu ändern“
Interview mit Prof. Dr. Claus Vogelmeier; Universität Marburg, Chair des GOLD Science Committee
GOLD formuliert als Ziel, COPD früher zu diagnostizieren. Wie soll das gelingen?
Prof. Vogelmeier: Man hat im Grunde zwei Optionen. Die eine ist, man geht symptombasiert heran. In den USA gibt es z. B. einen Fragebogen namens CAPTURE*, der respiratorische Symptome und Anamnese abfragt und eine Vortestwahrscheinlichkeit liefert, ob jemand eine COPD hat. Damit könnte man Patienten früher finden, aber nicht ganz früh, wie wir es gerne hätten. Die zweite läuft über Vorsorge, etwa eine Spirometrie im Check-up 35 oder Nebenbefunde aus dem Lungenkarzinomscreening.
Was können Sie COPD-Patienten anbieten, die sie auf diese Weise identifiziert haben?
Prof. Vogelmeier: Gute Frage. Wir haben gerade in der RETHINC-Studie gesehen, dass es offensichtlich zu kurz greift, solchen Menschen einfach einen dualen Bronchodilatator zu geben. Um die Uhr zurückzudrehen, müssen wir genau ansehen, welche Probleme vorliegen. Wer ein Sekretproblem hat, profitiert vielleicht von einem Mukolytikum. Entzündliche Prozesse im Frühstadium könnten auf ICS ansprechen. Aber es gibt auch neue Konzepte zum Beispiel mit interventionellen Verfahren.
Das Therapieschema sieht vor, dass Gruppe A einen Bronchodilator bekommt. Wen setzen Sie auf einen kurz wirksamen?
Prof. Vogelmeier: Hat jemand im frühen COPD-Stadium sehr selten Symptome z. B. bei starker körperlicher Belastung, kommt man mit einem SABA und/oder einem SAMA aus. Entwickelt jemand regelmäßig Symptome im Alltag, würde ich nicht mit einer kurz wirksamen Substanz therapieren.
In Gruppe E haben Arzt und Patient die Wahl zwischen dualer Bronchodilatation und Triple. Wer bekommt sofort das Triple?
Prof. Vogelmeier: Bei einem Patienten mit einer schweren, stationär behandlungsbedürftigen Exazerbation als Erstmanifestation der Krankheit und hoher Eosinophilenzahl im Differenzialblutbild kann man neben einer LABA/LAMA-Therapie auch an ein Triple denken. Dieser Patient hat Argumente für die primäre Triplegabe: ein schweres Ereignis und eine klare T2-Signatur.
LABA/ICS soll nicht mehr verordnet werden. Was tun mit den vielen Patienten, die aktuell darauf eingestellt sind?
Prof. Vogelmeier: Das ist eine individuelle Entscheidung. Wenn es mit LABA/ICS gut läuft, gibt es keinen Grund, etwas zu ändern. Hat der Patient weiter primär Dyspnoe, sollte man auf LABA/LAMA wechseln. Wenn er weiter exazerbiert, wird auf die Tripletherapie eskaliert.
Eine wichtige Differenzialdiagnose bei Atemnot oder Exazerbationen ist die Herzinsuffizienz, die mit der COPD diverse Risikofaktoren teilt. Sollten Ärzte bei COPD-Patienten regelmäßig BNP messen, um zu merken, wenn das Herz schwächelt?
Prof. Vogelmeier: Bei akuten Exazerbationen auf jeden Fall, weil das therapeutische Konsequenzen hat. Viele Kollegen in der Praxis haben bereits Point-of-Care-Tests dafür. Wenn ein COPD-Patient mit akuten Symptomen kommt, kann es aber auch bei hohem BNP schwierig sein festzustellen, ob die primäre Ursache in der Lunge oder im Herzen liegt. Viele COPD-Patienten haben schon in stabilen Phasen erhöhte Herzbiomarker, und das korreliert mit der Mortalität.
*COPD Assessment in Primary Care to Identify Undiagnosed Respiratory Disaese and Exacerbation Risk
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).