Adjuvanz wohl nicht bei jedem lokal fortgeschrittenen Blasenkrebs nötig
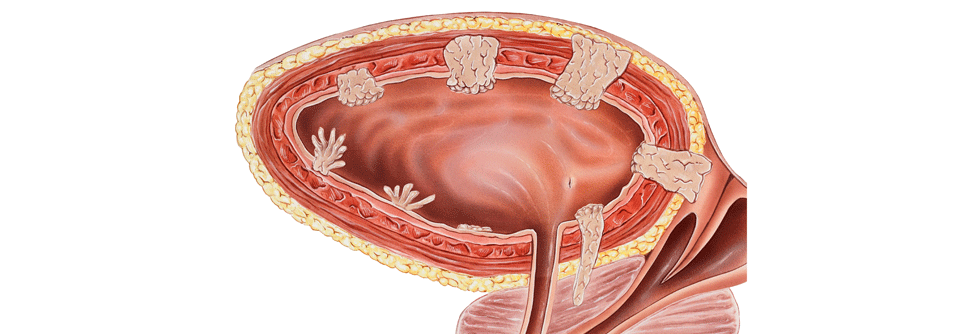
 Neue Studienergebnisse zeigen positive Trends zur Therapie des Blasenkarzinoms.
© MQ-Illustrations – stock.adobe.com
Neue Studienergebnisse zeigen positive Trends zur Therapie des Blasenkarzinoms.
© MQ-Illustrations – stock.adobe.com
An der international laufenden randomisierten und prospektiven Phase-3-Studie IMvigor011 nahmen Patient:innen nach Resektion ihres Hochrisiko muskelinvasiven Blasenkarzinoms (MIBC) teil.1 Im Gegensatz zur Vorläuferstudie IMvigor010 erhoben die Wissenschaftler:innen den ctDNA-Status nicht nur einmalig, sondern seriell über ein Jahr hinweg. Betroffene mit positivem ctDNA-Befund erhielten randomisiert adjuvantes Atezolizumab oder Placebo.
In seiner Präsentation legte Prof. Dr. Thomas Powles vom Barts Cancer Institute in London den Fokus jedoch auf diejenigen, die durchweg ctDNA-negativ blieben. Die Analyse dieser sogenannten Überwachungsgruppe umfasst bisher 171 Personen.
Lymphknotenstatus und T-Stadium irrelevant
„Die Rückfallquote nach 18 Monaten lag nur bei etwa 10 %“, erklärte Prof. Powles. Von zwei Todesfällen war einer nicht krebsbedingt. Zu den Patient:innencharakteristika merkte der Referent an: „Dinge wie der Lymphknotenstatus, das T-Stadium – sie wurden vom ctDNA-Status in den Schatten gestellt. Ob eine ctDNA-negative Person positive Lymphknoten hatte ist irrelevant – vielleicht hatte sie eine sehr erfolgreiche OP und sie wurden alle entfernt.“ Die Liste lege vielmehr nahe, dass ein negativer ctDNA-Befund in seriellen Tests all die anderen Risikofaktoren übertrumpft, die bisher genutzt wurden.
„In Zukunft leistungsfähige neoadjuvante Strategien“
Die wichtigste Frage sei nun, ob man den entsprechenden Personen angesichts der geringen Wahrscheinlichkeiten für Rückfall oder Tod die adjuvante Therapie ersparen kann. „Bei Checkpoint-Inhibitoren besteht bekanntlich eine 10%ige Chance für eine lebensverändernde Toxizität“, betonte Prof. Powles und schloss mit einem persönlichen Ausblick: „Dieses Feld verändert sich gerade sehr. Ich denke, in Zukunft werden wir leistungsfähige neoadjuvante Strategien haben. Zystektomie wird noch eine Rolle spielen, viele Erkrankte werden wir heilen können – aber adjuvante Therapien bei unselektierten Patient:innen werden die Zeit nicht überdauern“.
Dass Nivolumab adjuvanter Standard für das Hochrisiko-MIBC wurde, basierte auf frühen Ergebnissen der Phase-3-Studie CheckMate 274. Eine Langzeitanalyse, die erstmals auch Daten zum Gesamtüberleben enthielt, stellte Prof. Dr. Matthew Galsky von der Icahn School of Medicine at Mount Sinai in New York vor.2 Die 709 Teilnehmenden hatten 1:1 randomisiert adjuvantes Nivolumab vs. Placebo erhalten. Die primären Endpunkte waren das DFS in der ITT-Population und bei Patient:innen mit ≥ 1 % PD-L1; sie wurden in vorherigen Auswertungen erreicht.
Die vorgestellte geplante Zwischenanalyse ergab in der ITT-Auswertung einen positiven OS-Trend für Nivolumab. Mit median 69,5 Monaten vs. 50,1 Monate verfehlte er jedoch die Signifikanz (HR 0,76; 95%-KI 0,61–0,96). Unter den Erkrankten mit PD-L1-Expression wurde das mediane Überleben in beiden Studienarmen nicht erreicht. Die Überlebensrate nach 36 Monaten betrug unter Nivolumab 71,3 % vs. 56,6 % in der Placebogruppe (HR 0,56; 95%-KI 0,36–0,86).
Quellen:
1. Powles T. 39th Annual EAU Congress; Vortrag: „Clinical outcomes in patients with high-risk, post-cystectomy muscle-invasive bladder cancer (MIBC) with persistent circulating tumour DNA-negative (ctDNA-) status on serial testing: surveillance analysis from the IMvigor011 study“
2. Galsky M. 39th Annual EAU Congress; Vortrag: „Extended follow-up from CheckMate 274 including the first report of overall survival outcomes“
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).