Auch Myositiden schlagen auf die Lunge
 Bei über 50 % der Myositispatient:innen lassen sich Autoantikörper nachweisen.
© TANABOON – stock.adobe.com
Bei über 50 % der Myositispatient:innen lassen sich Autoantikörper nachweisen.
© TANABOON – stock.adobe.com
Über 40 % aller Patienten mit inflammatorischen Myopathien weisen eine interstitielle Lungenerkrankung (ILD) auf, wobei sich diese häufig schon vor der Myositis manifestiert. Ihr Verlauf variiert von subklinisch bis fulminant, insgesamt ist die ILD der häufigste Grund für Hospitalisierungen und Tod bei Myopathiepatienten. Trotzdem wird sie in den Klassifikationen von Polymyositis (PM) und Dermatomyositis (DM) nicht berücksichtigt, bemängeln Dr. Robert Hallowell vom Massachusetts General Hospital and Harvard Medical School in Boston und Dr. Sonye Danoff, John Hopkins University School of Medicine, Baltimore.
Über 50 % der Patienten haben Autoantikörper
Vor allem die Rolle der Antikörper und ihre Assoziation mit der ILD haben bei Myositiden an Bedeutung gewonnen. Heute weiß man, dass sich bei mehr als der Hälfte aller Myositispatienten bekannte Autoantikörper nachweisen lassen. Diese werden in Myositis-Specific Antibodies (MSA) und Myositis-Associated Antibodies (MAA) unterteilt. Eine ILD bei Myositis ist stark mit dem Vorhandensein von MSA assoziiert. Erst seit 2017 werden Autoantikörper überhaupt erst in der EULAR/ACR-Klassifikation berücksichtigt, monieren die Autoren. Dabei handelt es sich mit anti-Jo-1 zudem nur um einen einzigen Antikörper.
Bei therapieresistenter Dyspnoe auf Antikörpersuche
Trotz hoher Glukokortikoiddosen (40 mg Prednisolonäquivalent/d) kämpfte eine 60-jährige Patientin mit interstitieller Lungenerkrankung mit schwerster Dyspnoe. Ihr niedergelassener Lungenarzt wusste nicht mehr weiter und schickte sie zu den Experten ins Lungenzentrum. Dort kam man zunächst auch nicht recht voran. Bis auf ein leichtes Knisterrasseln beidseits basal erbrachte die körperliche Untersuchung keine Befunde. Die Frau hatte weder Gelenkschwellungen noch irgendwelche Hautauffälligkeiten, die für eine zugrundeliegende Kollagenose sprachen. Die ersten Tests auf Antikörper waren ebenfalls unergiebig: ANA, anti-Smith, anti-RNP, anti-Scl-70, anti-SSA/SSB, Rheumafaktor, anti-CCP und ANCA – allesamt negativ. Die Lungenbiopsie zeigte ein nicht-spezifisches Muster mit zellulären und fibrotischen Anteilen. Doch dann wurden die Kollegen fündig: Die Frau wies hochtitrige Anti-PL-12-Antikörper auf, passend zur Verdachtsdiagnose Myositis-assoziierte ILD.
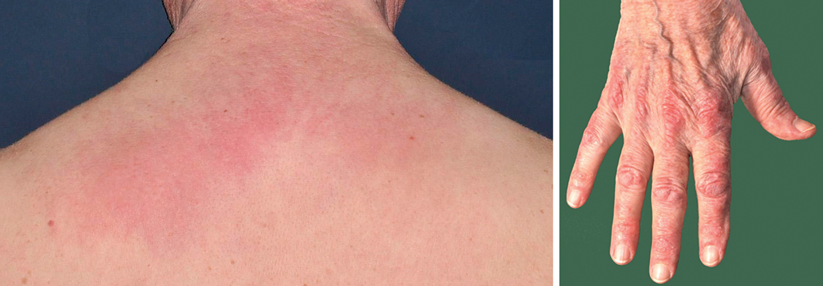
3.000 mg Mycophenolat-Mofetil täglich besserten die Dyspnoe der Patientin erheblich, berichten Dr. Hallowell und Dr. Danoff. Im Verlauf von sieben Monaten wurde die Glukokortikoiddosis auf 5 mg Prednisolonäquivalent/d reduziert. Daraufhin entwickelte die Frau jedoch zahlreiche Beschwerden. Es kam zu Gelenkschmerzen, Muskelschwäche sowie Erythemen im Gesicht und an den Händen. Parallel dazu stieg die anfänglich unauffällige CK auf 2.000 U/l.
Durch die zusätzliche monatliche Gabe von i.v. Immunglobulinen klangen Haut- und Muskelbeschwerden ab. Die Dyspnoe blieb weiterhin gebessert, was sich auch in den regelmäßigen CT-Aufnahmen nachweisen ließ.
Quelle: Hallowell RW, Danoff SK. CHEST 2023; DOI: 10.1016/j.chest.2023.01.031
Dabei gibt es viel mehr: Zu den MSA mit den größten pulmonalen Implikationen gehören die sog. Antikörper gegen Aminoacyl-tRNA-Synthetasen (ARS-AK, darunter anti-Jo-1). Sie kommen bei etwa einem knappen Drittel aller Patienten mit Dermato- oder Polymyositis vor. Je nach Antikörper und Patientenkohorte findet man sie zudem bei 56–100 % aller Betroffenen mit Myositis und ILD. Als Anti-Synthetase-Syndrom wird eine Kombination aus ILD, Myositis, Arthritis, Raynaud-Phänomen, Fieber und/oder Mechanikerhänden bei Vorliegen von ARS-Abs bezeichnet.
Mit einem ähnlichen Phänotyp ist der Anti-MDA-5-Antikörper assoziiert, wobei die ILD häufig besonders schwer verläuft. Dazu kommen Palmarpapeln, Ulzerationen und Hautnekrosen. Die klinischen Manifestationen unterscheiden sich bei diesem Phänotyp stark nach Ethnien. So haben Asiaten meist schwerere Verläufe als Nordamerikaner.
Darüberhinaus wurden zahlreiche weitere Autoantikörper beschrieben. Anti-Ro52 weisen etwa 20 % der Myositispatienten auf, liegt eine ILD vor, ist die Rate höher. Findet sich zugleich MDA-5, verläuft die ILD besonders progressiv. Auch PM-Scl ist mit der Myositis-ILD assoziiert, der Antikörper tritt bei bis zu 78 % der Betroffenen auf. Keine Zusammenhänge mit der ILD wurden dagegen bisher für die von den Myositiden bekannten Antikörper Anti-SRP und Anti-Mi-2 gefunden.
Husten und Dyspnoe mit Lufu und evtl. CT abklären
Eine ILD bei Patienten mit idiopathischen inflammatorischen Myopathien kann von asymptomatisch bis rasch progredient verlaufen. Bei erkältungsähnlichen Symptomen wie Husten oder Dyspnoe sollte immer auch an die ILD als mögliche Ursache gedacht und zur Abklärung eine Lungenfunktion erhoben und ggf. eine CT veranlasst werden, empfehlen die Autoren. Hinter respiratorischen Symptomen kann sich darüber hinaus auch ein Lungenhochdruck verbergen.
| Anti-Synthetase-Antikörper (Auswahl) | ||||
|---|---|---|---|---|
| Antikörper | Zielstruktur | Patienten mit Lungen-manifestation (%) | Patienten mit Muskel-manifestation (%) | Klinische Zeichen |
| Anti-Jo-1 | Histidyl-tRNA-Synthetase | 69 % | 84 % | Mechanikerhände, Arthralgien, Myositis |
| Anti-PL-12 | Alanyl-tRNA-Synthetase | 91 % | 33 % | Raynaud-Syndrom, isolierte ILD |
| Anti-PL-7 | Threonyl-tRNA-Synthetase | 75 % | 66 % | heliotropes Erythem, schwere ILD, Myositis,Perikarderguss |
| Anti-EJ | Glyceryl-tRNA-Synthetase | 98 % | 56 % | |
| Anti-OJ | Isoleucyl-tRNA-Synthetase | 100 % | 44 % | schwere Myopathie, seltener Raynaud-Syndrom |
| Anti-KS | Asparaginyl-tRNA-Synthetase | 100 % | 5 % | isolierte ILD |
| nach Hallowell RW, Danoff SK, CHEST (2023), DOI: https://doi.org/10.1016/j.chest.2023.01.031 | ||||
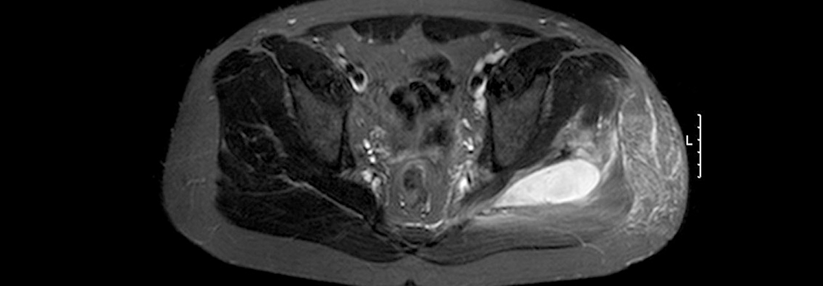
In der Bildgebung finden sich hauptsächlich (aber nicht ausschließlich) subpleurale und basale Veränderungen, am häufigsten konsistent mit einer nicht-spezifischen interstitiellen (NSIP) und/oder organisierender Pneumonie.
Behandelt wird die ILD abhängig von der Schwere der Lungenbeteiligung, zentrale Bedeutung hat dabei die Immunsuppression. Generell scheinen Betroffene mit einer Polymyositis darauf besser anzusprechen als diejenigen mit einer Dermatomyositis. Es existieren keine Studien, die die einzelnen Substanzen zur Behandlung der ILD prospektiv untersucht hätten. Die verfügbaren Daten weisen darauf hin, dass die am häufigsten verwendeten Immunsuppressiva wahrscheinlich austauschbar sind.
Die Autoren empfehlen folgendes Vorgehen: Bei erhaltener Lungenfunktion, minimalen Symptomen und weniger als 10 % Beteiligung in der CT ist ein Abwarten unter regelmäßiger Kontrolle der Lungenfunktion angezeigt. Patienten mit moderater Ausprägung (abnormale Lungenfunktionsparameter, Fortschreiten der Erkrankung und mehr als 10 % Beteiligung im CT) werden mit Prednisolon und Mycophenolat-Mofetil (MMF) oder Azathioprin (AZA) behandelt. Spricht die Erkrankung innerhalb von vier bis sechs Monaten darauf nicht an, sollte man die Therapie auf Tacrolimus (TAC) oder Rituximab (RTX) umstellen und die Gabe von intravenösen Immunglobulinen (IvIG) erwägen. Schreitet die ILD unter Prednisolon und AZA bzw. MMF sogar fort, wird gleich TAC oder RTX hinzugefügt, evtl. zusätzlich noch IvIG.
Bei ARS/MDA-5-Positivität gleich Tacrolimus
Die akute Exazerbation einer Myositis-ILD mit Hypoxämie und Lungenversagen macht eine Einweisung in ein Krankenhaus erforderlich. Dr. Hallowell und Dr. Danoff empfehlen zur Behandlung initial Solu-Medrol i.v., gefolgt von Prednisolon plus IvIG sowie mindestens ein steroidsparendes Immunsuppressivum (MMF, AZA oder TAC), je nach Vorbehandlung und Komorbiditäten. Bei ARS/MDA-5 positiven Patienten präferieren die Experten TAC, weil es bei diesen Patienten schneller wirkt als andere Immunsuppressiva. Bessert sich die Erkrankung innerhalb einer Woche nicht, wird ein zweites Immunsuppressivum hinzugefügt. Bei fulminanten Verläufen trotz aggressiver Immunsuppression ist der Plasmaaustausch eine Option.
Bis zu 25 % der Betroffenen weisen ein UIP-Muster und damit eine fibrotische Veränderungen in der Lunge auf. Ob bei ihnen Nintedanib wirksam ist – so wie bei einer SSc-assoziierten ILD – muss noch geklärt werden. Bislang liegen dazu nur wenige nicht-verblindetete oder retrospektive Daten vor.
Quelle: Hallowell RW, Danoff SK. CHEST 2023; DOI: 10.1016/j.chest.2023.01.031
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).