Dritter Checkpoint-Inhibitor in der Prüfung
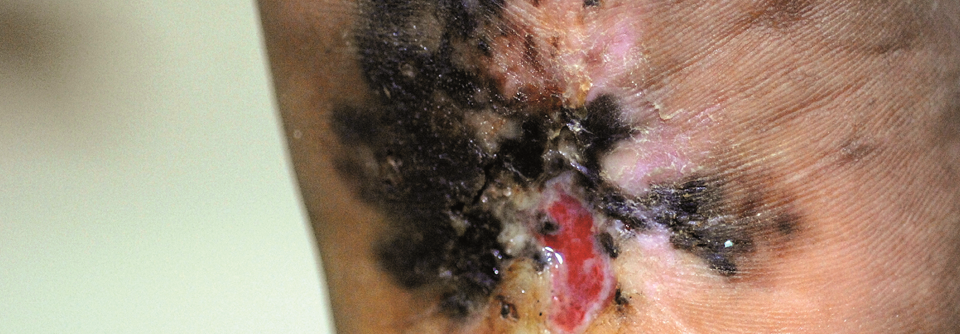 Zu sehen ist hier eine Nahaufnahme eines malignen Melanoms an der Ferse.
© Science Photo Library/MEDICIMAGE
Zu sehen ist hier eine Nahaufnahme eines malignen Melanoms an der Ferse.
© Science Photo Library/MEDICIMAGE
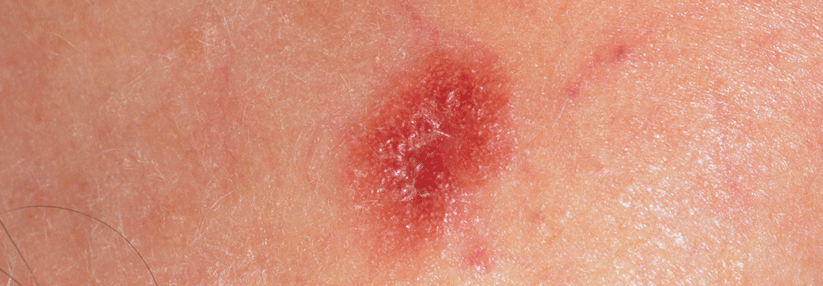
PD1- und CTLA4-Inhibitoren haben u.a. die Behandlung des Melanoms revolutioniert. Allerdings existieren zusätzliche Checkpoints, die die T-Zell-Aktivierung und deren Funktion hemmen können. Folglich besteht Bedarf an neuen Kombinationen und Substanzen, um die Prognose der Betroffenen weiter zu verbessern.
Mitglied der Immunglobulin- Superfamilie im Blick
Mit Relatlimab wurde ein Wirkstoff entwickelt, der an LAG3* auf Immunzellen bindet. LAG3 verringert die T-Zell-Proliferation und Effektor-T-Zell-Funktion und wird von vielen Tumoren, inklusive Melanomen, überexprimiert. In einer vorangegangenen Phase-1/2-Studie führte die Kombination aus Relatlimab und dem PD1-Inhibitor Nivolumab zu einem anhaltenden objektiven Ansprechen bei Erkrankten mit Melanomen, die nach PD1-Hemmern rezidivierten oder gegenüber diesen refraktär waren.
Prof. Dr. Dr. Hussein A. Tawbi vom MD Anderson Cancer Center, Houston, und sein Team prüften die Zweifachtherapie als Fixdosiskombination in der globalen, doppelblinden Phase-2/3-Studie RELATIVITY-047. Die 714 Teilnehmenden mit zuvor unbehandeltem, nicht-resezierbarem Melanom im Stadium III–IV erhielten 1:1 randomisiert alle vier Wochen per Infusion
- 160 mg Relatlimab und 480 mg Nivolumab als Fixdosiskombination oder
- 480 mg Nivolumab
bis zur Krankheitsprogression oder inakzeptablen Nebenwirkungen.
Alle Patienten und Patientinnen exprimierten LAG3 und PD1 auf den Melanomzellen. Personen mit einer vorangegangenen (neo-)adjuvanten Therapie durften ebenfalls an der Studie teilnehmen, wenn die Behandlung mehr als sechs Monate vor dem Rezidiv abgeschlossen war. Eine vorangegangene Interferongabe war erlaubt, wenn die letzte Dosis mindestens sechs Wochen vor Randomisierung erfolgte.
Mit 10,1 Monaten vs. 4,6 Monate lebten Teilnehmende unter der Fixdosiskombination länger progressionsfrei als Erkrankte unter alleinigem Nivolumab (HR 0,75; p = 0,006). Das Zwölf-Monats-PFS betrug im Prüfarm vs. Kontrolle 47,7 % vs. 36 %. Der PFS-Vorteil war in den meisten untersuchten Subgruppen gegeben: u.a. war er unabhängig von der Tumorlast, dem BRAF-Mutationsstatus sowie der Serum-LDH-Konzentration.
Inhibitorkombination wird besser vertragen
Median wurden die Betroffenen 5,6 Monate mit der Fixdosiskombination und 4,9 Monate mit Nivolumab behandelt. Die mediane Zeit bis zum Ende der Therapie betrug 8,3 Monate vs. 6,5 Monate. 5,9 % vs. 3,6 % der Teilnehmenden entwickelten infusionsbedingte Toxizitäten. Unter behandlungsbedingten Grad-3/4-Nebenwirkungen litten 18,9 % vs. 9,7 %. Drei vs. zwei Todesfälle führte das Studienteam auf die Therapie zurück.
Die Ergebnisse deuten darauf hin, dass die duale Checkpoint-Blockade in der Erstlinie gegenüber einer PD1-Inhibitor-Monotherapie bevorzugt werden sollte, resümieren die Autoren. Das Zwölf-Monats-PFS unter Relatlimab/Nivolumab sei ähnlich zu dem, was mit Ipilimumab/Nivolumab in der CheckMate-067-Studie erreicht wurde. Die Forschenden betonen aber, dass Schlüsse aus dem Vergleich zwischen unterschiedlichen Untersuchungen nur vorsichtig gezogen werden sollten. Mit Relatlimab könne bald ein dritter Checkpoint-Inhibitor für Melanomerkrankte zur Verfügung stehen.
* Lymphocyte-activation gene 3
Quelle: Tawbi HA et al. N Engl J Med 2022; 386: 24-34; DOI: 10.1056/NEJMoa2109970
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).