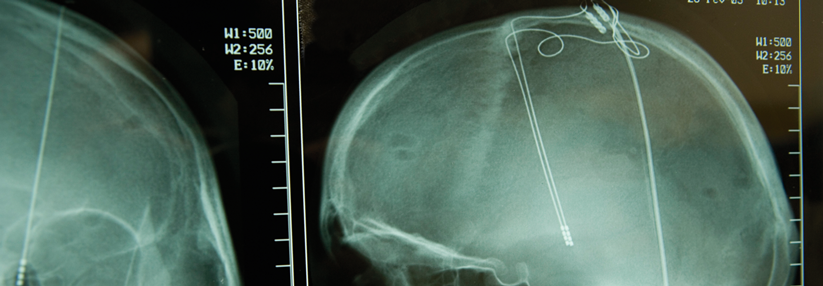
Hirnstimulation schon ab der Parkinson-Diagnose?
 Ein früher Einsatz könnte den Krankheitsverlauf abmildern.
© iStock.com/Naeblys
Ein früher Einsatz könnte den Krankheitsverlauf abmildern.
© iStock.com/Naeblys
Lange Zeit galt die tiefe Hirnstimulation (THS) als eine Art Rettungsanker in späten Stadien der Parkinsonkrankheit, wenn Medikamente nicht mehr ausreichen. Diese Sicht hat sich in den letzten Jahren gewandelt, angestoßen durch die EARLYSTIM-Studie. Wobei es sich hier streng genommen auch nicht um eine Frühtherapie handelte. Statt die THS wie üblich ca. 15 Jahre nach Krankheitsbeginn einzusetzen, wurde die Frist auf sieben Jahre verkürzt, erinnerte Professor Dr. Jens Volkmann von der Universität Würzburg. Die Patienten hatten definitiv schon Wirkfluktuationen entwickelt, wenn auch milde. Aber immerhin: Die frühe THS, zusätzlich zur medikamentösen Therapie durchgeführt, brachte Vorteile hinsichtlich der Lebensqualität im Vergleich zur optimierten Medikamentengabe.
Operativer Eingriff kein Grund zur Sorge
„Ein bisschen untergegangen ist anfangs die Frage, wie riskant das denn ist“, meinte der Neurologe. Patienten neigen dazu, operative Verfahren als gefährlicher anzusehen als Medikamente. Für die Beratung ist es also wichtig zu wissen, ob der Eingriff tatsächlich besondere Risiken birgt. Grund zur Sorge lieferte EARLYSTIM allerdings nicht. Die Rate schwerer Nebenwirkungen lag in beiden Behandlungsgruppen gleich hoch (Beobachtungszeitraum: zwei Jahre). Dabei traten unter alleiniger Medikation viel häufiger motorische und psychiatrische Symptome auf, während Komplikationen wie Wundheilungsstörungen oder Elektrodendislokation naturgemäß auf die THS-Gruppe beschränkt blieben. Dort machten sie etwa die Hälfte der Nebenwirkungsfälle aus.
„Wenn man das einmalige Risiko ausklammert, das durch die Operation entsteht, kamen Nebenwirkungen unter medikamentöser Therapie doppelt so häufig vor“, kommentierte Prof. Volkmann.
Inzwischen liegt eine Sekundäranalyse vor, derzufolge unter tiefer Hirnstimulation seltener nicht-motorische Fluktuationen auftraten und weniger hyperdopaminerge Effekte (z.B. nächtliche Hyperaktivität, Impulskontrollstörungen, Sprunghaftigkeit).1 Keinen Unterschied stellten die Untersucher bei hypodopaminergen Störungen wie Apathie und Depression fest. THS-Patienten benötigten seltener Neuroleptika und Antidepressiva. Das ist umso bemerkenswerter, als über psychiatrische Nebenwirkungen der tiefen Hirnstimulation diskutiert worden ist, erklärte der Kollege. Unklar blieb dabei, ob diese die Folgen der langjährigen Sensibilisierung durch die Medikamente sind, die durch die THS aggraviert werden.
Die Frage stellt sich, ob die tiefe Hirnstimulation nicht noch früher zum Zuge kommen sollte. Eine unter ethischen Aspekten höchst kritisch diskutierte Studie in den USA prüft sogar, ob es sinnvoll ist, Parkinsonpatienten direkt nach der Diagnose zu operieren. Basis dafür ist die Vorstellung, dass die gute Beweglichkeit, die Patienten unter THS erreichen, die Neurodegeneration beeinflussen könnte – z.B. durch verminderte glutamaterge Exzitotoxizität, verstärkte Neurotrophinausschüttung oder bewegungsinduzierte Neuroplastizität. Im Tierversuch scheint das zu funktionieren, da wirkte die THS neuroprotektiv in der Substantia nigra und besserte motorische Fähigkeiten. „Aber was das für Menschen bedeutet, ist vollkommen unklar“, so Prof. Volkmann.
Daten aus dem klinischen Alltag zeigen, dass noch eingie Hürden zu nehmen sind. Die Analyse der Krankenakten von 28 000 Patienten mit THS-Eingriffen ergab eine enorm hohe Revisionsrate zwischen 15 und 35 %, zur Hälfte verursacht durch Elektrodendislokalisation oder mangelnde Wirksamkeit – sprich: nicht zielgenau platzierte Elektroden. Wo diese optimal liegen sollten, haben Forscher aus THS-Patientendaten anhand der klinischen Resultate berechnet: im dorsalen und lateralen Anteil des Nucleus subthalamicus. Relativ kleine Distanzen können einen dramatischen Unterschied machen.
Scheitern der THS nicht einfach hinnehmen
„Es ist kein unabänderliches Schicksal, wenn die THS nicht funktioniert“, betonte Prof. Volkmann. Zeigt ein Patient nach Anlage des Devices nicht die Response, die der Levodopa-Test erwarten lässt, sollte man erwägen, die Elektroden neu zu positionieren.
Quelle: 1. Lhommée E et al. Lancet Neurol 2018; 17: 223-231
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).