Kardiorenale Protektion in Leitlinien verankert
 SCORE2-Diabetes berücksichtigt individuelle Faktoren und ermöglicht eine genauere Risikoabschätzung.
© zakalinka – stock.adobe.com
SCORE2-Diabetes berücksichtigt individuelle Faktoren und ermöglicht eine genauere Risikoabschätzung.
© zakalinka – stock.adobe.com
Ein Typ-2-Diabetes (T2D) kommt selten allein. Die meist älteren Patientinnen und Patienten sind oft übergewichtig/adipös, haben wegen weiterer Risikofaktoren wie arterieller Hypertonie und/oder Dyslipidämie kardiale Beschwerden (CVD) und dazu in vielen Fällen auffällige Blutzuckerwerte. Oder es wird primär ein T2D diagnostiziert und die Betroffenen haben dann ein hohes Risiko eine kardiovaskuläre bzw. kardiorenale Erkrankung (CVD + T2D/CVD + CKD) zu entwickeln, weil dauerhaft entgleisende HbA1c-Werte zu mikro- und makrovaskulären Folgekomplikationen an Herz und Nieren führen können.
Kardiovaskuläre Risikostratifizierung und -kategorisierung
Mit jedem Risikofaktor steigt bei diesen Patienten die kardiovaskuläre Morbiditäts- und Mortalitätsrate aufgrund eines akuten kardialen Ereignisses. Auch Herzinsuffizienz oder eine periphere arterielle Verschlusskrankheit (pAVK) treten häufiger auf.
Dem wird in aktuellen Leitlinien der EASD1/ADA2, der ESC3 und KDIGO4 zum Management kardiorenaler Erkrankungen bei Typ-2-Diabetes Rechnung getragen, und es werden entsprechende Behandlungs-Empfehlungen formuliert, um die Risiken zu senken. Diese Leitlinien sind das Ergebnis einer systematischen Aufarbeitung und Zusammenstellung der besten verfügbaren wissenschaftlichen Evidenz.
ESC-Leitlinie 2023
Die Schlüsselempfehlungen der ESC Guidelines for the management of cardiovascular disease in patients with diabetes [1], die von einer internationalen interdisziplinären Autorengruppe (Nephrologen, Kardiologen Angiologen, Diabetologen) erarbeitet wurden und auf kardiorenale Organprotektion fokussieren, stellte Prof. Dr. Dirk Müller-Wieland, Aachen, vor. Die Leitlinie wurde von der Aachener Arbeitsgruppe unter Leitung von Prof. Nikolaus Marx als Kardiologe, Prof. Massimo Frederici, Rom, und Prof. Dirk Müller-Wieland als Diabetologen sowie Frau Prof. Katharina Schütt, Leiterin des Bereiches Herzinsuffizienz, federführend begleitet und koordiniert.
Um Risiko-Patientinnen und -Patienten vor kardiovaskulären Folgeerkrankungen und Ereignissen zu schützen, wurde ein Algorithmus zur präventiven bzw. therapeutischen Herangehensweise erarbeitet. Zentrales Element für Behandlungsentscheidungen sind die Risikostratifizierung und -kategorisierung verschiedener Patientenpopulationen, wie sie sich in der Praxis vorstellen:
Es sind Menschen mit den Diagnosen
- Typ-2-Diabetes und atherosklerotische Herzerkrankung (ASCVD)
- T2D und Herzinsuffizienz (HF) sowie
- T2D und chronische Niereninsuffizienz (CKD)
Da jede dieser Konstellationen die Prognose der Patienten verschlechtern kann, wird in der aktualisierten Leitlinie folgendes Vorgehen empfohlen:
- Screening von Patienten mit CVD auf Diabetes
- Bewertung des kardiovaskulären Risikos bei T2D-Patienten
- Untersuchung von T2D-Patienten auf Herz-Kreislauf- sowie Nierenerkrankungen
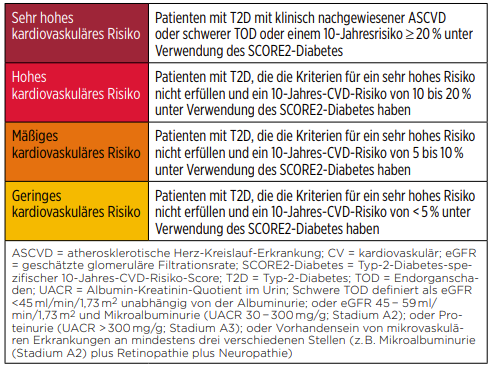
Daraus ergeben sich vier Risikokategorien bei Typ-2-Diabetes-Patienten: Geringes, mäßiges, hohes und sehr hohes kardiovaskuläres Risiko [2], das individuell zu bewerten ist, um über die weitere Behandlung zu entscheiden (Abb. 1).
Um in den europäischen Ländern und den verschiedenen Regionen das unterschiedliche kardiovaskuläre Risiko zu berücksichtigen, ist der ESC-SCORE aus 2016 zur Berechnung des 10-Jahres-Risikos einer tödlichen kardiovaskulären Erkrankung in Populationen von Ländern mit hohem kardiovaskulärem Risiko etabliert. Allerdings wurde bei diesem Score ein Teil von Patienten nicht berücksichtigt, wie Müller-Wieland anhand eines Patientenfalles zeigte:
Übergewichtiger Patient, 62 Jahre alt, keine manifeste ASCVD, Typ-2-Diabetes seit sechs Jahren, essenzielle Hypertonie, Fettstoffwechselstörung mit entsprechender Medikation, HbA1c-Wert von 7,6 %, eGFR nach CKD-EPI von 72 ml/min/1,73 m2, laut Definition UACR 10 mg Albumin/g Crea keine Albuminurie.
Im Rahmen der Leitlinienentwicklung zum Management kardiorenaler Erkrankungen bei Typ-2-Diabetes stellte sich also die Frage: „Was tun mit solchen Patienten ohne ASCVD, um deren Risiko abzuschätzen und eine Therapieentscheidung zu treffen?“
Neuer Risikoscore für T2D-Patienten
Nach Beratung mit dem SCORE-Konsortium-Team wurde von den Autoren der Leitlinie ein neuer SCORE2-Diabetes [3], ein speziell auf die diabetische Population zugeschnittener Risikoscore vorgeschlagen, der genau bei diesen Patienten genutzt werden sollte. Demnach lautet die neu in die Leitlinie aufgenommene Empfehlung, bei allen Patienten im Alter von ≥40 Jahren mit T2D ohne ASCVD oder schweren Endorganschäden das 10-Jahres-CVD-Risiko anhand des Systematic COronary Risk Evaluation (SCORE)2-Diabetes-Algorithmus abzuschätzen, um so bei diesen Patientinnen und Patienten die Risikofaktoren für ASCVD auf individueller Basis zu bewerten. Dabei sei es wichtig, die medizinische und familiäre Vorgeschichte, Symptome, Untersuchungsergebnisse, Labor- und andere diagnostische Testergebnisse sowie das Vorhandensein von ASCVD oder schweren Endorganschäden (target organ damage (TOD)) zu berücksichtigen. Vom damit ermittelten kardiovaskulären Risiko hängt dann wiederum u.a. die antiglykämische Differenzialtherapie ab.
Deutschland ist eine Region mit moderatem Risiko. Bei einem 60-jährigem Menschen ohne Diabetes, Nichtraucher und durchschnittlichen konventionellen Risikofaktoren ergibt sich anhand des SCORE2-Diabetes ein 10-Jahres-Risiko von 4,7 %.
Handelt es sich aber z. B. um eine Patientin – der SCORE2-Diabetes unterscheidet zwischen Männern und Frauen − mit neudiagnostiziertem T2D (HbA1c 6,73 %) und einer eGFR von 90 ml/min/1,73 m2, ergibt sich ein Risiko von 7,6 %.
Wurde die Diagnose gestellt, als der Betreffende erst 50 Jahre alt war, mit einem HbA1c von vielleicht 8,2/8,3 % und wenig eingeschränkter eGFR von 60, steigt das Risiko schon auf 12,7 %.
Ist der Patient, wie im Beispiel von Prof. Müller-Wieland, ein 62-jähriger Mann, beträgt das Risiko 14,8 %.
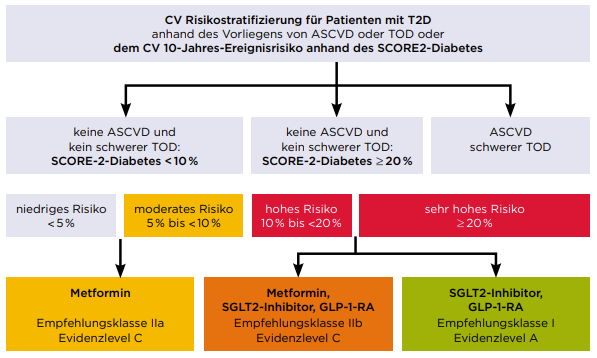
Dementsprechend sollte die Therapie gemäß der aktualisierten Leitlinie risikoadaptiert angepasst werden, um bei Patienten mit T2D ein bestehendes erhöhtes kardiovaskuläres Risiko zu senken, Herz und Nieren zu schützen und die Prognose zu verbessern. So wird in der Leitlinie u. a. empfohlen, die blutzuckersenkende Behandlung von Wirkstoffen ohne kardiovaskulären Nutzen bzw. nachgewiesene Sicherheit auf Wirkstoffe mit nachgewiesenem kardiovaskulärem Nutzen umzustellen. Der Einsatz von SGLT2-Hemmern und GLP1-RA hat bei hohem und sehr hohem Risiko eine Klasse IIb bzw. Klasse I-Empfehlung (Abb. 2).
Management des kardiorenalen Risikos bei T2D
Jeder dritte Patient mit Typ-2-Diabetes entwickelt im Laufe seines Lebens eine diabetische Nephropathie (DKD). Rund die Hälfte der Betroffenen entwickelt eine Albuminurie. Die Lebenserwartung von Patienten mit Albuminurie und T2D verkürzt sich um bis zu 16 Jahre, im wesentlichen aufgrund von Organschäden an Herz, Nieren und Gefäßen durch die Kombination metabolischer, hämodynamischer, entzündlicher und fibrotischer Faktoren. Diese gilt es zu verhindern.
2022 bis 2024: Fünf neue Dokumente
- KDIGO 2022 Clinical Practice Guideline for Diabetes Management in Chronic Kidney Disease [4]
- Diabetes Management in chronic Kidney Disease: A Consensus Report by the American Diabetes Association (ADA) and Kidney Disease: Improving Global Outcomes (KDIGO) [6]
- 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes [1]
- Chronic Kidney Disease and Risk Management: Standards of Care in Diabetes – 2024 [5]
- KDIGO 2024 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease [7]
Seit der Verfügbarkeit innovativer Medikamente, die einen umfassenden kardio-vaskulär-renalen Schutz und neue Behandlungsoptionen bieten, ist die chronische Nierenerkrankung (CKD) im Zusammenspiel der pathophysiologischen Prozesse zunehmend in den Fokus gerückt. In seinem Vortrag „Leitlinien zum Management kardiorenaler Erkrankungen bei Diabetes“ beschäftigte sich Prof. Dr. Thomas Ebert, Leipzig, beim Diabeteskongress mit der Frage der Notwendigkeit eines CKD-Screenings und fasste die neuen therapeutischen Möglichkeiten zusammen. Basierend auf für diese Patientenklientel relevanten Leitlinien der EASD/ADA, ESC und KDIGO sowie dazu aktuell veröffentlichten Dokumenten erläuterte er die eGFR- und UACR-basierte CKD-Diagnostik/-Klassifikation, warum welche Personen gescreent werden sollten und die Empfehlungen, die für eine spezifische Therapie der diabetischen Nierenerkrankung (DKD) generiert wurden.
Screening detektiert besonders gefährdete Patienten
Durch die jetzigen therapeutischen Möglichkeiten der Behandlung mit nephroprotektiven Substanzen gebe es mittlerweile eine klare Empfehlung, dass Menschen mit einem Risiko für eine Niereninsuffizienz auf das Vorliegen einer Nephropathie gescreent werden sollten. „Hierzu zählt natürlich insbesondere ein Diabetes mellitus (Typ 1 und Typ 2). Alle Menschen mit Diabetes müssen auf CKD gescreent werden “, betonte Ebert. Er verwies auf die Notwendigkeit einer umfassenden multifaktoriellen Betreuung der Patientinnen und Patienten entsprechend der Behandlungspyramide der KDIGO (2022). Dazu gehören in jedem Fall die dringende Empfehlung, auf das Rauchen zu verzichten, die Blutdruckregulation, gegebenenfalls eine Ernährungsumstellung (insbesondere Salzreduktion), Gewichtsnormalisierung, Lipidtherapie und dann je nach Risikoprofil die spezifischen Therapien.
Flow-Studie
Inzwischen wurden auf dem 61. Kongress der European Renal Association (ERA) in Stockholm die Daten der als bahnbrechend geltenden FLOW-Studie publiziert.
Diese hat gezeigt, dass Semaglutid das Risiko für schwerwiegende Nierenerkrankungen, kardiovaskuläre Folgeerkrankungen und die Gesamtmortalität bei Patienten mit T2D und CKD deutlich reduziert. Die Teilnehmer, die Semaglutid erhielten, hatten ein um 24 % geringeres Risiko für den zusammengesetzten primären Endpunkt, einschließlich Nierenschäden und Tod aufgrund von kardiovaskulären und nierenbedingten Ursachen, im Vergleich zu den Teilnehmern, die Placebo erhielten.
Diese Risikoreduktion war sowohl bei nierenspezifischen als auch bei kardiovaskulären Todesfällen konsistent. Auch bei den sekundären Endpunkten zeigte Semaglutid signifikante Verbesserungen. Der Gesamtabfall der eGFR war um 1,16 ml/min/1,73m2/Jahr langsamer, das Risiko schwerer kardiovaskulärer Ereignisse wurde um 18 % und das Risiko der Gesamtmortalität um 20 % gesenkt [8].
Therapeutische Empfehlungen
Um alle kardiorenalen Risiken bei Diabetespatienten zielgerichtet zu adressieren, sei nach Eberts Auffassung am besten der Empfehlung aus der neuen ESC Leitlinie (2023) zu folgen.
Auf Basis dieses Drei-Säulen-Schemas habe man in den aktuellen Leitlinien die Empfehlungen für eine spezifische Therapie der CKD bei Diabetes formuliert. Demnach kommen RAS-Blocker bei T1D oder T2D und Hypertonie in maximal tolerierbarer Dosis zum Einsatz, um möglichst das Ziel 130/80 mmHg, bestenfalls darunter, zu erreichen. Für die individualisierte Diabetes-Therapie (Zielkorridor HbA1c 6,5 bis 8 %) bei CKD-Patienten werden zusätzlich zur Behandlung mit Metformin (bei T2D, CKD und einer eGFR >30 ml/min/1,73 m2) SGLT2-Hemmer (bei Diabetes und einer eGFR >20 ml/min/1,73 m2) empfohlen. Wenn die Glukoseziele nicht erreicht werden, kann nach der ESC-Leitlinie zudem die Verordnung von GLP1-Agonisten in Erwägung gezogen werden.
Bei CKD und einer eGFR >25 ml/min/1,73 m2 bei normalem Kaliumspiegel sowie erhöhtem Albumin-Kreatinin-Quotienten (ACR) >30 mg/g sollte zur Reduktion des renalen Progresses außerdem Finerenon verordnet werden. Das Präparat hat in internationalen Leitlinien konsistent den höchsten Evidenzgrad (A) zur kardiovaskulären und renalen Risikoreduktion bei T2D mit Albuminurie erhalten. Die KDIGO-Leitlinie empfiehlt den Einsatz dieser Substanzklasse bei Patientinnen und Patienten mit Diabetes mellitus und einer Albuminurie (Albumin-Kreatinin-Quotient/ACR >30 mg/g).
Fazit
Alle Patienten sowohl mit T1D als auch T2D sollten auf CKD gescreent sowie multimodal und interdisziplinär therapiert werden. Die Diagnostik besteht weiterhin aus der Bestimmung von eGFR und UACR. In Bezug auf die Glukoseziele ist bei T2D eine individuelle Diabetesbehandlung mit RAS-Blockern, SGLT2-Inhibitoren und dem nsMRA Finerenon angezeigt mit direkter Evidenz zur Senkung des DKD-Progresses. Ebert ist überzeugt, dass nach (der inzwischen erfolgten) Veröffentlichung der Ergebnisse der FLOW-Studie die bisherige Drei-Säulen-Therapie bald erweitert wird und als Vier-Säulen-Therapie-Empfehlung aus RASi, SGLT2i, nsMRA und GLP1-RA in zukünftige Leitlinien eingeht. Zudem sind bei der Therapiestrategie gleichzeitig zahlreiche Begleitfaktoren zu beachten (Gewicht, Lipide, ASS) und entsprechend zu behandeln.
Interview: Elke Klug
Quellen:
Marx N & Frederici M (chairman), Schütt K & Müller-Wieland D (coordinators) et al. Eur Heart J 2023 Oct 14;44(39):4043-4140
https://leitlinien.dgk.org/files/29_2023_pocket-leitlinien_diabetes.pdf
SCORE2-Diabetes Working Group. Eur Heart J. 2023;44: 2544-56
KDIGO 2022 Clinical Practice Guideline for Diabetes Management in Chronic Kidney Disease. Rossing P et al. Kidney International, Volume 102, Issue 5, S1−S127
American Diabetes Association Professional Practice Committee. Diabetes Care 2024 Jan 1;47(Suppl 1):S219-S230
de Boer IH et al. Diabetes Care 2022 Dec 1;45(12):3075−3090.
Kidney Int 2024 Apr;105(4S):S117−S314
Perkovich V et al. N Engl J Med 2024;391:109−121
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).




![Abbildung 3: Umfassende Versorgung von Patienten mit Diabetes und CKD (nach [2])](/fileadmin/Bilder/Artikelbilder/2025/01_Januar_2025/Abbildung_3.png)