NSCLC Lazertinib als neue Therapieoption für EGFR-mutierte Nichtkleinzeller
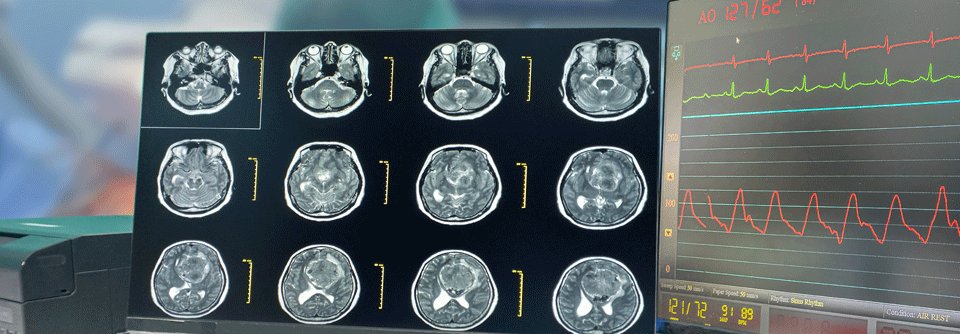 Forschende zeigen, dass intrakranielle Metastasen des EGFR-mutierten NSCLC effektiv kontrollierbar sind.
© Richman Photo – stock.adobe.com
Forschende zeigen, dass intrakranielle Metastasen des EGFR-mutierten NSCLC effektiv kontrollierbar sind.
© Richman Photo – stock.adobe.com
Die Prognose des EGFR-mutierten NSCLC hängt entscheidend vom Vorliegen zerebraler Metastasen ab, erläutern Forschende um Prof. Dr. Min Hee Hong vom Yonsei Cancer Centerin Seoul:1 Etwa ein Viertel der Betroffenen hat bereits bei der Diagnose Hirnfiliae und die Hälfte entwickelt diese im weiteren Krankheitsverlauf. Wie gut intrakranielle Metastasen pharmakotherapeutisch zu kontrollieren sind, entscheidet im Wesentlichen die Liquorgängigkeit der eingesetzten Wirkstoffe.
Im Gegensatz zu EGFR-TKI der ersten und zweiten Generation, welche diesbezüglich Defizite haben, überwinden Präparate der dritten Generation die Blut-Hirn-Schranke besser. Ein solcher Vertreter ist der sowohl gegen die…
Bitte geben Sie Ihren Benutzernamen und Ihr Passwort ein, um sich an der Website anzumelden.