Molekulare Therapien in der Dermatologie
 Interleukine sind unter anderem an der Modulation von Immunreaktionen und der Exazerbation von Allergie- und Asthmasymptomen beteiligt.
© Juan Gärtner - stock.adobe.com
Interleukine sind unter anderem an der Modulation von Immunreaktionen und der Exazerbation von Allergie- und Asthmasymptomen beteiligt.
© Juan Gärtner - stock.adobe.com
Interleukine sind an einer Vielzahl von zellulären Prozessen beteiligt: Differenzierung, Proliferation und Migration von Immunzellen sowie Modulation von Immunreaktionen. Das zunehmende Wissen über die Immunmechanismen hat die Therapie vieler chronisch entzündlicher Hautkrankheiten revolutioniert, schreibt ein Autorenteam um Dr. Alvaro Prados-Carmona vom Hospital Universitario San Cecilio in Granada. Es hat die verschiedenen Rollen der Interleukine und ihre Verbindung u. a. zu Psoriasis, AD, allergischer Kontaktdermatitis, Urtikaria und Hidradenitis suppurativa näher beleuchtet.
Wichtige Th1-Zytokine
Das zellvermittelte Th1-Netzwerk interagiert über IL-2, IL-12, IL-18 und IFNg. Das von den dendritischen Zellen produzierte IL-12 bewirkt beispielsweise, dass sich die naiven T-Helferzellen zu Th1-Helferzellen entwickeln können. IFNg ist dagegen das „Signature-Zytokin“ der Th1-Zellen. Es hilft dabei, Tumorimmunität und Immunreaktionen gegen intrazelluläre Erreger zu steuern, spielt aber auch eine Rolle bei Erkrankungen wie Psoriasis, Multipler Sklerose und Morbus Crohn. Zusammen mit INFa und INFb ist IFNg zudem an der Entstehung von Lupus, Lichen planus und Vitiligo beteiligt.
Wichtige Th2-Zykokine
Die Th2-Reaktion läuft vor allem über die antikörperproduzierenden B-Zellen ab, beteiligt sind aber auch Eosinophile, Basophile und Mastzellen. Zu den Th2-Zytokinen gehören IL-4, IL-5, IL-13 und IL-25 (= IL-17E). Eine zentrale Rolle spielt die IL-4-/IL-13-Achse. Die beiden Zytokine steuern die Differenzierung von naiven T-Helferzellen in spezifischen Th2-Zellen und sorgen dafür, dass B-Zellen IgE produzieren. Außerdem scheint die IL-4-/-13-Achse auch an Hautfibrose und der Narbenbildung beteiligt zu sein. IL-5, ebenfalls ein Th2-Zytokin, nimmt eine Schlüsselrolle in der Eosinophilenaktivierung ein – und damit bei Atopieerkrankungen. IL-31 ist ebenfalls ein für die Haut wichtiges Zytokin, über welches Nerven und Immunzellen interagieren.
Wichtige Th-17-Zytokine
Die Th17-Reaktion über IL-17, IL-22 und IL-23 dient vornehmlich der Abwehr extrazellulärer Bakterien und Pilze. Sie erhöht die Barrieredurchlässigkeit und verstärkt an der Entzündungsstelle die Neutrophilenrekrutierung. Daher führt eine gestörte Th17-Antwort zu chronischer Entzündung und Gewebeschäden, z. B. im Rahmen von Psoriasis, ankylosierender Spondyloarthritis oder chronisch-entzündlichen Darmerkrankungen. Das heterodimere IL-23 – bestehend aus den Untereinheiten p19 und p40 – wird hauptsächlich von dendritischen Zellen und Makrophagen produziert. Da es die p40-Untereinheit mit IL-12 gemein hat, wirken entsprechende Antikörper auf beide Zytokine (IL-12/23-Hemmer). IL-23 wird u. a. für die Proliferation der Th17-Zellen gebraucht, welche dann ihrerseits die IL-17-Zytokine (A bis F) und IL-22 ausschütten. Unter diesen nimmt insbesondere IL-17A eine wichtige proinflammatorische Rolle ein, das auf Epithelzellen, Endothelzellen und Fibroblasten einwirkt.
Treg-Zytokine
Die Zytokine der regulatorischen T-Zellen halten die Immuntoleranz aufrecht und sind sozusagen Gegenspieler der Autoimmunität. Zu ihnen gehören IL-10, IL-35 sowie TGFb (transforming growth factor beta) und die damit verbundene SMAD-Proteinfamilie. Da sie sich auf Zellregeneration, Zellwachstum und -differenzierung auswirken, kann eine Dysregulation mit Krebserkrankungen, Fibrose und Autoimmunerkrankungen wie Sklerodermie, aber auch mit verschiedenen Wundheilungsstörungen (Keloide) assoziiert sein.
Andere proinflammatorische Zytokine inkl. TNFa
Die Zytokine IL-1, IL-6 und TNFa sind maßgeblich daran beteiligt, Entzündungsreaktionen einzuleiten und aufrechtzuerhalten. Zwar sind sie wichtig für die Infektabwehr, aber durch ihre proinflammatorische Natur fördern sie gleichzeitig immunvermittelte entzündliche Erkrankungen. Das von Makrophagen, aber auch Th1-Zellen ausgeschüttete TNFa nimmt eine zentrale Rolle ein. Seine Signalwege betreffen neben der Entzündung selbst auch Fieber, Zellapoptose, Sepsis und Kachexie.
Vertreter der IL-1-Familie (IL-1α, IL-1β, IL-18, IL-33, IL-36α, IL-36β, IL-36γ) werden unter anderem von Keratinozyten produziert und sind mit verschiedenen entzündlichen Hauterkrankungen assoziiert. Chemokine der CCL(CXC-Motiv-Chemokin-Ligand)-Familie, zu der auch CXCL8 (IL-8) gehört, sorgen u. a. dafür, dass Immunzellen in die Haut einwandern, sie spielen beispielsweise eine Rolle bei der Psoriasis.
Alle zusammen und jedes für sich
Je nach Trigger (intrazelluläre Erreger, Helminthen und Gifte, extrazelluläre Bakterien und Pilze) reagiert das Immunsystem über drei verschiedene Hauptsignalwege, die ihrerseits verschiedene Schlüsselzytokine haben. Zwar agiert jedes Netzwerk für sich, durch einzelne Moleküle (u. a. IL-2 und IL-21) sind sie aber indirekt miteinander verbunden und ermöglichen eine Interaktion des gesamten Immunsystems.
JAK-Moleküle sind an Inflammation und epidermaler Hyperplasie bei Psoriasis beteiligt
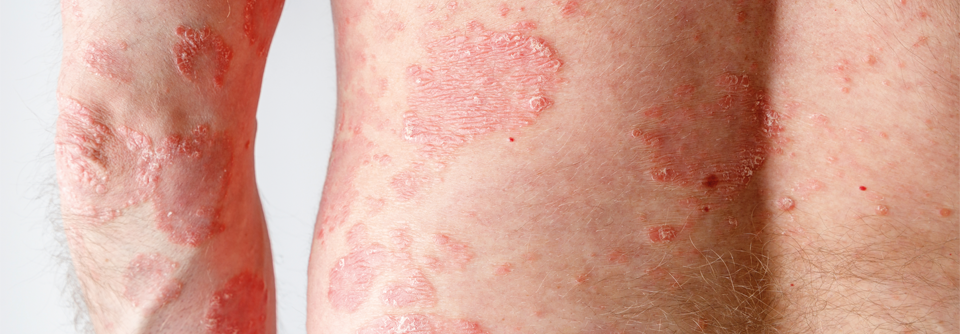
Welche dieser Moleküle lassen sich bislang adressieren? Bei der Psoriasis im Vordergrund stehen IL-17 und IL-23, da sie die Th17-Reaktion am Laufen halten. An ihr beteiligt sind aber auch die JAK-Moleküle, allen voran TYK2, die auf der intrazellulären Seite die Signale weitergeben und für die Inflammation und die epidermale Hyperplasie sorgen, hinzu kommen TNFa sowie PDE-4.
Eine hochregulierte PDE-4-Aktivität verringert die cAMP-Spiegel, was seinerseits die Zellen dazu bringt, TNFa, IL-23 und IL-17 auszuschütten. Molekulare Ansatzpunkte bei Psoriasis bieten daher Moleküle, die entweder Schlüsselzytokine oder ihre Rezeptoren blockieren: IL-23 bzw. -12/23 (Guselkumab, Tildrakizumab, Risankizumab bzw. Ustekinumab), IL-17 (Secukinumab, Infliximab, Brodalumab, Bimekizumab), TNFa (Etanercept, Infliximab, Adalimumab, Certolizumab, Golimumab), PDE4 (Apremilast) und TYK2 (Deucravacitinib).
Die Schlüsselzytokine, die bei der AD zu IgE-Überschuss, Eosinophilie und Hautbarrierestörung führen, sind IL-4, IL-13 und IL-31. Strukturproteine der Haut (u. a. Filaggrin) werden durch IL-4 und IL-13 herunterreguliert, was Hauttrockenheit und Infektanfälligkeit erhöht. IL-31 als neuronale Schnittstelle ist ein Schlüsselfaktor beim Juckreiz. Ansatzpunkte sind bei der AD IL-13 bzw. die IL-4/13-Achse (Tralokinumab, Lebrikizumab bzw. Dupilumab) und IL-31 (Nemolizumab) genauso wie die zellinterne Signalweitergabe über JAK (Abrocitinib, Upadacitinib, Baricitinib). Im asiatischen Raum scheinen außerdem Th17-Zytokine aufgrund der Barrieredysfunktion involviert zu sein. Die Anti-IL-5-Therapie spielt mehr beim atopischen Asthma eine Rolle, entweder über das Molekül selbst (Mepolizumab, Reslizumab) oder seinen Rezeptor (Benralizumab).
Bei der Urtikaria involviert sind vor allem IL-1, IL-6 und TNFa. Sie beeinflussen die Mastzellenaktivität. Hinsichtlich des Juckreizes kommt IL-31 hinzu. Es gibt zudem Hinweise darauf, dass an der chronischen spontanen Variante auch Th-17-Zellen beteiligt sind.
Therapeutisch werden bislang hauptsächlich Antihistaminika eingesetzt, aber auch Omalizumab, das sich gegen freies IgE richtet. Studien zu IL-1, IL-4/13, IL-31 und BTK (Bruton‘s Tyrosine Kinase) laufen.
Bei der HS ist die Pathogenese zwar noch nicht komplett geklärt, aber vieles scheint auf eine maßgebliche Th-17-Beteiligung hinzudeuten (IL-17 und IL-23). Außerdem sind TNFa und IL-1b hochreguliert. Neben den Anti-IL-17-Therapien werden daher auch Ansätze bezüglich der IL-23- und der IL-1-Hemmnug (Anakinra, Canakinumab) untersucht.
Spezifische Ansätze können unerwünschte Nebeneffekte reduzieren
Zwar greifen die neuen Ansätze ähnlich wie die älteren Immunsuppressiva ebenfalls modulatorisch in das Immunsystem ein, aber das Vorgehen werde immer gezielter, erinnern die Autorinnen und Autoren. Spezifischere Ansätze können die unerwünschten Nebeneffekte und die Notwendigkeit von Labortests reduzieren. Zwar sind viele Therapien bisher nur für Psoriasis und AD untersucht, es bleibe aber zu hoffen, dass das Wissen um die Signalwege zukünftig auch Menschen mit Vitiligo, Lupus und Sklerodermie zugutekommt. mes/SG
Quelle: Prados-Carmona A et al. JEADV Clin Pract 2024; doi: 10.1002/jvc2.537
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).