Sequenziell wirkt besser
 Das in der SEQUENCE-Studie geprüfte Regime konnte das Gesamtüberleben von median 9,7 Monaten auf 13,2 Monate verlängern.
© iStock / Eoneren
Das in der SEQUENCE-Studie geprüfte Regime konnte das Gesamtüberleben von median 9,7 Monaten auf 13,2 Monate verlängern.
© iStock / Eoneren
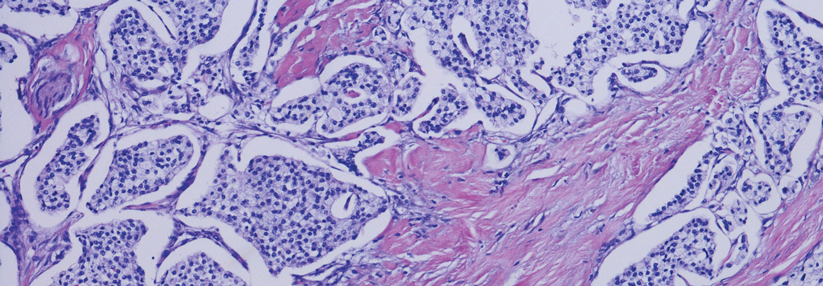
Verschiedene Chemotherapieregime wirken bei den Subtypen des Pankreaskarzinoms unterschiedlich gut: So erwies sich nab-Paclitaxel/Gemcitabin (nab-P/Gem) besonders effektiv für die Behandlung von Basalzelltumoren, während der klassische Typ besser auf FOLFIRINOX anspricht.
Die Wirksamkeit lässt sich möglicherweise durch eine sequenzielle Strategie mit initialer Gabe von nab-Paclitaxel steigern. Dieses Taxan führt im Tumor zu einer Depletion des desmoplastischen Stroma und verbessert damit die Penetration weiterer Zytostatika, erläuterte Prof. Dr. Dr. Alfredo Carrato, Hospital Universitario Ramón y Cajal, Madrid.
Akademisch initiierte Phase-2-Studie
Auch war die Sequenztherapie mit nab-P/Gem gefolgt von mFOLFOX in einer Phase-1-Studie bereits klinisch aktiv und wies ein gutes Sicherheitsprofil auf. Hier konnten beide Regime laut Prof. Carrato in voller Dosis verabreicht werden.
Forschende prüften diesen Ansatz in der akademisch initiierten Phase-2-Studie SEQUENCE in der ersten Therapielinie. Sie schlossen 157 Patient:innen mit metastasierten duktalen Adenokarzinomen des Pankreas ein, die randomisiert
-
entweder den Standard mit nab-P/Gem in vierwöchigen Zyklen bis zum Progress oder
-
die Sequenztherapie mit initialer Gabe von nab-P/Gem gefolgt von mFOLFOX an Tag 29 jedes sechswöchigen Zyklus
erhielten. Primärer Endpunkt war die Zwölf-Monats-Rate des Gesamtüberlebens, die laut Studienhypothese von 35,4 % in der Kontrolle auf 50 % gesteigert werden sollte.
Zeit bis zum Progress um median vier Monate verlängert
Die Gesamtansprechrate wurde mit 20,3 % vs. 39,7 % im Prüfarm nahezu verdoppelt, berichtete Prof. Carrato. Null vs. drei Patient:innen erreichten eine komplette Remission. Die Tumorkontrollrate stieg von 68,4 % unter dem Standard auf 79,5 % unter der Sequenztherapie. Die Zeit bis zum Progress verlängerte sich durch die zusätzliche mFOLFOX-Gabe von median 5,3 Monaten auf 9,3 Monate, was Prof. Carrato für das Pankreaskarzinom als gut bewertete (HR 0,462; p < 0,001).
Das PFS verbesserte sich von 5,2 Monaten auf 7,9 Monate (HR 0,516; p < 0,001). Die Teilnehmenden profitierten auch hinsichtlich des medianen OS von der Sequenz: Es betrug in der Kontrolle 9,7 Monate gegenüber 13,2 Monaten in der Prüfgruppe (HR 0,676; p = 0,023). Der primäre Studienendpunkt wurde damit erreicht: Prof. Carrato bezifferte die Zwölf-Monats-Rate des OS in der Kontrolle mit 35,4 % und im Sequenztherapiearm mit 55,3 % (p = 0,016).
Neutropenien und Thrombozytopenien deutlich häufiger
Die Behandlungsdauer in der experimentellen Gruppe war mit 8,3 Monaten doppelt so lang wie unter nab-P/Gem allein; allerdings kam es öfter zu Zyklusverzögerungen, Therapiepausen und Dosisreduktionen. Neutropenien traten mit 46,1 % vs. 24,1 % im Prüfarm signifikant häufiger auf als in der Kontrolle (p = 0,004), ebenso wie Thrombozytopenien (23,7 % vs. 7,6 %; p = 0,007). Bezüglich der weiteren Toxizitäten fielen keine Unterschiede auf. Vorläufige Daten zur Lebensqualität waren ebenfalls ähnlich.
Die signifikant verbesserte Wirksamkeit von nab-P/Gem/mFOLFOX, auch im Vergleich zu aktuellen Studiendaten, wertete Prof. Carrato als Fortschritt in der Behandlung des metastasierten Pankreaskarzinoms und als vielversprechende Alternative für das Management der Patient:innen.
Quelle: Carrato A. 2022 ASCO Annual Meeting; Abstract 4022
Kongressbericht: 2022 ASCO Annual Meeting
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).