TACE, TARE, Transplantation und mehr
 Erstmals haben die Autoren auch Empfehlungen zu den Karzinomen der Gallenwege und Gallenblase erarbeitet.
© iStock/Nerthuz
Erstmals haben die Autoren auch Empfehlungen zu den Karzinomen der Gallenwege und Gallenblase erarbeitet.
© iStock/Nerthuz
Seit der Erstauflage der S3-Leitlinie zum Leberzellkarzinom (HCC) hat sich einiges getan. Für die Systemtherapie sind viele Substanzen hinzugekommen, aber auch in den anderen Bereichen haben die Autoren zahlreiche Empfehlungen auf der Basis neuer Erkenntnisse modifiziert. Neben den neuen Medikamenten betrifft das besonders die Diagnostik, die Lebertransplantation und die zusätzlichen Interventionen im Kampf gegen den Krebs.
Diagnostik
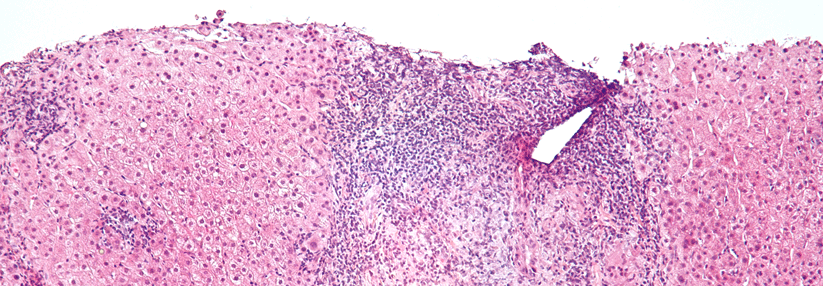
Sah die Leitlinie zur Diagnostik des HCC bei Zirrhose bislang zwei unabhängige Bildgebungen vor, sollen verdächtige Herde größer als 1 cm nun mittels kontrastverstärktem MRT abgeklärt werden. Das sei sensitiver als die CT. Bleibt der Befund unklar oder kann keine MRT durchgeführt werden, empfiehlt sich eine triphasische CT und/oder eine kontrastmittelverstärkte Sonographie.
Führt auch dies nicht zur sicheren Diagnose, sollte man biopsieren. Eine Biopsie ist zudem in der Palliativsituation mit therapeutischer Konsequenz ratsam und wenn Patienten in klinische Studien eingeschlossen werden sollen. Obligat ist sie vor definitiven Therapien von Erkrankten ohne Zirrhose.
Ablation
Für Personen ohne Leberzirrhose sowie Zirrhosepatienten mit solitärem Herd lautet das Ziel: Den Tumor entfernen, wenn dies komplett möglich ist. Für kleinere Geschwulste unter 3 cm, die tief und zentral im Organ liegen, kann sich eine Ablation aber besser eignen. Diese soll primär thermoablativ erfolgen, wenn der Krebs ungünstig liegt oder die Leberfunktion eingeschränkt ist.
Studien belegen mittlerweile, dass die Mikrowellenablation dafür ebenso gut geeignet ist wie die Radiofrequenzablation. Im Fall von größeren Tumoren bis 5 cm und erhaltener Leberfunktion soll vorher eine transarterielle Chemoembolisation (TACE) durchgeführt werden – das kann den Effekt der Ablation verstärken.
Liegen keine kurativen Behandlungsoptionen für Patienten im intermediären Stadium vor, sind transarterielle Methoden allein das lokale Mittel der Wahl. Dabei sollte man die TACE mitunter mehrfach wiederholen, um eine komplette Devaskularisation zu erzielen. Nach zwei Runden gilt es, die Methode vor dem Fortsetzen im Tumorboard erneut zu bewerten. Alternativ ist auch eine Radioembolisation (TARE) möglich. Sind beide Verfahren keine Option, kann man eine Hochpräzisionsradiotherapie (SBRT) erwägen.
Transplantation
Für Patienten mit HCC bleibt die Transplantation die effektivste Option, solange das Karzinom nur die Leber betrifft. Sie ist für Personen im Stadium A gemäß Barcelona Clinic Liver Cancer (BCLC) Staging System und innerhalb der Mailand-Kriterien der bevorzugte kurative Ansatz. Zudem darf der AFP-Wert nicht mehr als 1000 ng/ml betragen, da sonst das Rezidivrisiko zu hoch ist. Jenseits dieser Grenze sollte keine Indikation zur Transplantation ohne neoadjuvante Behandlung gestellt werden. Betroffene mit HCC (BCLC A) innerhalb der Mailand-Kriterien erhalten eine Bridging-Therapie, sofern es die Leberfunktion zulässt.
Patienten, die die Mailand-Vorgaben nicht erfüllen, aber innerhalb derjenigen der UCSF* liegen, können ebenfalls ein Spenderorgan bekommen – vor allem, wenn ein Downstaging gelingt, sodass die Erkrankten die Mailand-Kriterien erreichen. Für Bridging und Downstaging kommen Lokalablation, Resektion, oder transarterielle Verfahren (TACE, TARE) infrage.
Chemotherapie
Ist das HCC schon zu weit fortgeschritten für Interventionen, kommt die systemische Behandlung ins Spiel – im Fall einer erhaltenen Leberfunktion inzwischen bevorzugt mit Atezolizumab plus Bevacizumab (A+B). Eine Systemtherapie mit einem zugelassenen TKI soll nach Progress oder bei Unverträglichkeit von A+B zum Einsatz kommen. Ist A+B kontraindiziert, kann man zunächst Lenvatinib oder Sorafenib verwenden. Nach Sorafenib empfiehlt die Leitlinie Cabozantinib, Regorafenib oder – wenn der Alpha-Fetoprotein-Wert mind. 400 ng/ml beträgt – Ramucirumab. Für Patienten im Stadium Child-Pugh B sind in Einzelfällen Sorafenib oder ein PD1-Antikörper als Systemtherapie möglich.
Input zu Gallengang und -blase
R0-Eingriff als stärkster prognostischer Faktor
Sofern eine vollständige Resektion möglich erscheint, sollte man diese allen Patienten anbieten – auch wenn das Karzinom multifokal ist oder bereits Lymphknoten oder Gefäße infiltriert hat. Das senkt zwar die Prognose, spricht aber nicht gegen den Eingriff. Für Betroffene mit Gallenblasenkarzinom sind die Aussichten sehr schlecht und eine R0-Resektion gilt als maßgebend für das Langzeitergebnis. Im Fall von Tis- und T1a-Tumoren genügt die Cholezystektomie. Ist der Krebs fortgeschritten, empfehlen die Autoren, neben der Gallenblase auch Lebergewebe und Lymphknoten zu entnehmen. Die meisten Gallenblasenkarzinome werden allerdings zufällig im Zuge einer Cholezystektomie entdeckt. Beschränkt sich der Krebs dabei auf ein Tis oder maximal die Mukosa (T1a), betragen die Fünf-Jahres-Überlebensraten bis zu 100 %. Daher soll man in diesen inzidentellen Fällen nur nachresektieren, wenn die Gallenblase nicht komplett entfernt wurde oder sich der Tumor schon weiter ausgebreitet hat. Inoperable intrahepatische Cholangiokarzinome kann man versuchen, thermoablativ komplett zu entfernen. Im fortgeschrittenen Stadium ohne extrahepatischen Befall können ab der Zweitlinie oder als Zusatz zu einer Chemotherapie intraarterielle Verfahren zum Einsatz kommen. Liegt ein irresektables, nicht-metastasiertes perihiläres Cholangiokarzinom vor, das die Mayo-Kriterien erfüllt, kann eine Lebertransplantation unter Studienbedingungen erwogen werden. Da bis zu 80 % der Patienten nach der Tumorentfernung ein Rezidiv erleiden, sollten Ärzte eine adjuvante Systembehandlung mit Capezitabin anbieten.Nach zwei bis drei Monaten Behandlungserfolg überprüfen
Neoadjuvant raten die Experten von einer Chemotherapie außerhalb von klinischen Studien ab. In Einzelfällen kann man aber mit einer intensivierten Chemotherapie – z.B. mit Gemcitabin, Cisplatin und nab-Paclitaxel – versuchen, Erkrankte mit lokal fortgeschrittenem Karzinom einer sekundären Operation zuzuführen. Palliativ setzen die Autoren im Regelfall auf Gemcitabin plus Cisplatin, in der Zweitlinie bieten sich auch FOLFOX oder je nach molekularer Charakteristik des Tumors – die man bei ECOG 0–1 bestimmen sollte – u.a. Checkpoint-, FGFR-, BRAF-Inhibitoren an. Prinzipiell, so die Empfehlung, sollte man bei allen Patienten, die auf eine Systemtherapie gut ansprechen, nach zwei bis drei Monaten die Resektabilität nochmals prüfen.* University of California San Francisco
Quelle: S3-Leitlinie „Diagnostik und Therapie des Hepatozellulären Karzinoms und biliärer Karzinome“, AWMF-Register-Nr: 032/053OL, www.awmf.org
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).