Brustkrebsprävention: Nicht nur auf BRCA schauen!
 Wissenslücken zum klinischen Nutzen der Brustkrebsprävention müssen geschlossen werden.
© llhedgehogll – stock.adobe.com
Wissenslücken zum klinischen Nutzen der Brustkrebsprävention müssen geschlossen werden.
© llhedgehogll – stock.adobe.com
Das „Nichtschadensprinzip“ muss bei allen Maßnahmen der Brustkrebsprävention beachtet werden, bekräftigte Privatdozentin Dr. Kerstin Rhiem, Universitätsklinikum Köln. Wichtig sei zudem, dass Brustzentren mit den spezialisierten Zentren hinsichtlich Beratung und möglicher präventiver Interventionen zusammenarbeiten. Jeder Maßnahme müsse eine umfassende und ausführliche Beratung mit individueller Nutzen-Risiko-Abwägung vorausgehen.
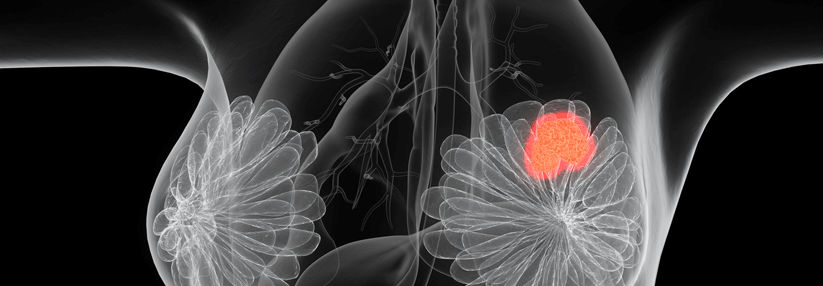
Im Vordergrund stehen derzeit Mutationen auf dem BRCA1- bzw. BRCA2-Gen. Diese sind beim Mammakarzinom mit einer Inzidenz von 25 % am häufigsten und zu ihnen liegen die meisten klinischen Daten vor. Doch es gibt weitere Gene mit Mutationen, betonte die Referentin. Ein Problem sei, dass es sich häufig nicht nur um brustkrebsassoziierte Gene handelt. Klinische Konsequenzen könnten aber nur gezogen werden, wenn eine entsprechende Evidenz für ein erhöhtes Brustkrebsrisiko vorliegt.
„Wir benötigen bei Interventionen den Beleg für einen klinischen Nutzen“, so Dr. Rhiem. Das bedeute:
- Kenntnisse zu Prävalenz und Penetranz der Erkrankung als Folge der Mutation,
- zum klinischen Erscheinungsbild,
- zum histologischen Subtyp,
- zum Krankheitsverlauf sowie
- zur Effektivität präventiver und therapeutischer Maßnahmen und
- zur Mortalität.
Diese Wissenslücken müssten anhand prospektiver Kohorten geschlossen werden.
Ein Kernelement: ein neues Register als Ergänzung zu den Krebsregistern. Dies sei das bundesweit neu eingeführte nationale Register HerediCaRe (Hereditary Cancer Registry), das vom Bundesministerium für Bildung und Forschung unterstützt wird. Genetische und klinische Daten werden zentral dokumentiert und ausgewertet.
Nicht alle Mutationsträger erkranken tatsächlich
Hintergrund aller Überlegungen ist, dass es in Deutschland ein effektives Früherkennungsprogramm zum Nachweis früher Brustkrebsstadien gibt (2b B ++), erklärte die Expertin. Dennoch gelte es selbst bei BRCA1-Mutationsträgerinnen, Nutzen und Schaden einer intensivierten Früherkennung individuell abzuwägen. Von etwa 1000 BRCA1-Mutationsträgerinnen haben nur etwa 100 einen auffälligen MRT-Befund. Bei nur 30 % der auffälligen Befunde handelt es sich um einen Tumor, so die Zehn-Jahres-Daten des Deutschen Konsortiums Familiärer Brust- und Eierstockkrebs zur intensivierten Brustkrebsfrüherkennung.
Bei gesunden BRCA1/2-Mutationsträgerinnen empfiehlt die AGO Mamma die bilaterale Salpingo-Oophorektomie aufgrund aktueller Daten nur noch zur Reduktion der Inzidenz von Eierstockkrebs und dem mit ihm assoziierten Sterberisiko sowie zur Reduktion der Gesamtmortalität. Zur Reduktion der Brustkrebsinzidenz und -mortalität wird sie hingegen nicht mehr empfohlen.
Für die bilaterale Mastektomie bleibt dagegen für gesunde BRCA-Mutationsträgerinnen eine „Kann“-Empfehlung zur Reduktion der Brustkrebsinzidenz bestehen (2a B +), berichtete Dr. Rhiem. Aktuelle Daten demonstrieren allerdings, dass die Mortalität nur bei den BRCA1- (2b B +) und nicht bei den BRCA2-Mutationsträgerinnen reduziert wird. Die aktuellen Daten zur chirurgischen Prävention sind entsprechend auch in die Empfehlungen zu den risikoreduzierenden Interventionen bei erkrankten BRCA1/2-Mutationsträgerinnen eingegangen.
Quelle: AGO Mamma State of the Art Meeting 2020