Brustkrebs: Die Suche nach geeigneten Biomarkern für HER2
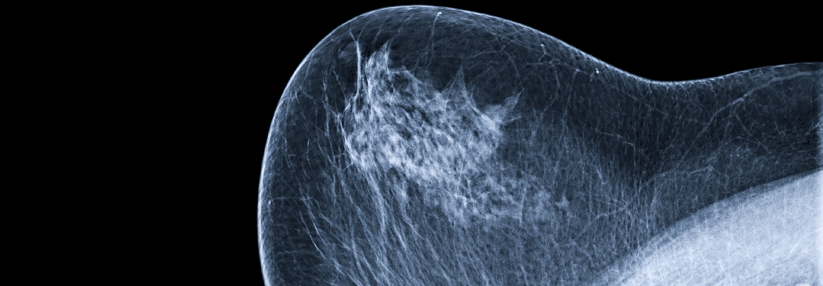
 Die Aufnahmelevel von 18F-FDG im PET-CT eignen sich als Marker bislang nur in Studien.
© iStock/gerenme
Die Aufnahmelevel von 18F-FDG im PET-CT eignen sich als Marker bislang nur in Studien.
© iStock/gerenme
Ein ähnlich gutes pathologisches Komplettansprechen (pCR) – das ergab die REDIX-HER2-Studie bei Patientinnen mit HER2+ Mammakarzinom nach einer neoadjuvanten Therapie für Trastuzumab Emtansin im Vergleich zur Standardtherapie mit Docetaxel, Trastuzumab und Pertuzumab.1 Wie Professor Dr. Thomas Hatschek vom Karolinska Universitätshospital in Stockholm berichtete, fiel die Rate für HR- höher aus als für HR+.2 Bei Ersterem erreichte sie in der Kontrolle 63,6 %, im experimentellen Arm 59,0 %.
Ab 10 % TIL scheint pCR relevant zu steigen
Gute Anhaltspunkte für die Wahrscheinlichkeit eines pCR nach neoadjuvanter Therapie könnten zukünftig die tumorinfiltrierenden Lymphozyten (TIL) und eine hohe Aufnahme von [18F]-2-Fluor-2-desoxy-D-glucose (18F-FDG) in der PET-CT* bieten. Wie Prof. Hatschek erklärte, korrelierten ≥ 10 % TIL in der Basisuntersuchung mit einem signifikant höheren pCR-Anteil im Vergleich zu Werten < 10 % (52,2 % vs. 30,4 %). Patientinnen, die nach zwei Behandlungszyklen einen frühen Abfall der 18F-FDG-Aufnahme im PET-CT von mehr als 75 % zeigten, erreichten zu 70,3 % ein pCR, die übrigen nur zu 22,5 %.
Irreführende Bildgebung
Lopez Velazco JI et al. ESMO Breast Cancer Virtual Meeting 2020; Abstract 110P
Erste Ergebnisse lassen auf ähnliches PFS schließen
Beide Biomarker sind laut Professor Dr. Valentina Guarneri von der Universität Padua Erfolg versprechend. Das PET-CT sei aber noch nicht reif für die Routine, erklärte sie in der Diskussion der Studie. Die Analyse und Dokumentation der TIL werde dagegen bereits in vielen Leitlinien empfohlen. Prof. Hatschek stellte auch erste Ergebnisse zum ereignisfreien Überleben vor. Nach median 28,5 Monaten Beobachtungszeit fand sich bislang kein Unterschied in den Armen Trastuzumab Emtansin vs. Docetaxel, Trastuzumab und Pertuzumab. Allerdings war die Zahl der Ereignisse auch noch sehr gering.* Positronen-Emissions-Tomographie-Computertomographie
Quellen:
1. Bergh JCS et al. J Clin Oncol 2019; 37; DOI: 10.1200/JCO.2019.37.15_suppl.501
2. Hatschek T et al. ESMO Breast Cancer Virtual Meeting 2020; Abstract 97O