Den Muskeln Beine machen
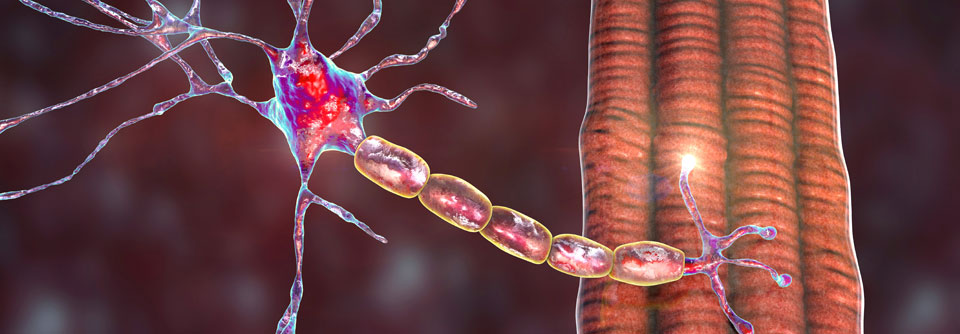
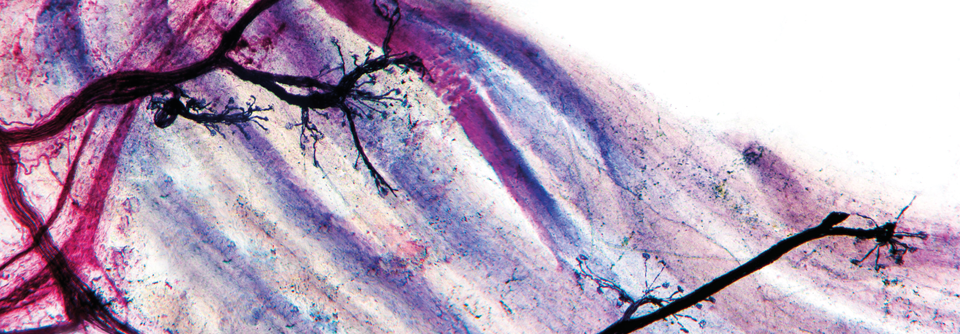 Verschiedene Antikörper blockieren bei Myasthenie die Übertragung an der neuromuskulären Endplatte.
© Science Photo Library/Wheeler, Dr. Keith
Verschiedene Antikörper blockieren bei Myasthenie die Übertragung an der neuromuskulären Endplatte.
© Science Photo Library/Wheeler, Dr. Keith
Hängende Augenlider und Doppelbilder, Schwäche in Arm-, Bein- oder Nackenmuskeln, Sprech- und Schluckstörungen: Das alles kann auf eine schnelle Ermüdbarkeit der Skelettmuskulatur nach Belastung hindeuten – das wichtigste Merkmal der autoimmunen Myasthenia gravis (MG). Die Beschwerden können fluktuieren und sich bis zur myasthenen Krise steigern. Um das zu verhindern und die Krankheitslast zu senken, steht eine wachsende Zahl von Therapien zur Verfügung. Die Entwicklung neuer Behandlungen ist auch dem immer besseren Verständnis der pathophysiologischen Mechanismen zu verdanken, schreiben Laura Tatsch und Dr. Bettina Schreiner von der Universitätsklinik Zürich.
Antikörper blockieren bei einer Myasthenie die Signalübertragung an der neuromuskulären Endplatte. Dabei gibt es verschiedene Subtypen der Erkrankung. Sie lassen sich danach unterscheiden, ob Antikörper gegen AChR, MuSK, LRP4 oder Agrin – oder eine Kombination davon – nachgewiesen werden (s. Kasten). Etwa 70 % der Patienten mit früher Manifestation (< 50 Jahre) und AChR-Antikörpern haben entzündliche Veränderungen im Thymus, z.B. eine lymphofollikuläre Thymushyperplasie. Über 60-Jährige zeigen dagegen in den meisten Fällen eine altersentsprechende Involution. Bei rund 15 % aller MG-Betroffenen besteht ein thymombedingtes paraneoplastisches Syndrom; diese Patienten produzieren fast immer AChR-Antikörper.
Subtypen der Maysthenia gravis
In etwa 85 % der Fälle wird die Myasthenie durch Autoantikörper gegen den Acetylcholinrezeptor (AChR) ausgelöst. Die Antikörper blockieren den Rezeptor und verringern dadurch (sowie über weitere Mechanismen) das Endplattenpotenzial. Rund 30–60 % der MG-Patienten bilden Antikörper gegen die muskelspezifische Rezeptor-Tyrosinkinase (MuSK). Sie verhindern die Interaktion zwischen der MuSK und dem Low-Density Related Protein 4 (LRP4), was unter anderem das Clustering von AChR an der motorischen Endplatte beeinträchtigt. Auch direkte Antikörper gegen LRP4 und Agrin wurden beschrieben. Zweifach positive Konstellationen kommen häufig vor – hauptsächlich AChR/LRP4, MuSK/LRP4 und AChR/Agrin.
Die Erkrankung ist bislang nicht heilbar. Das Behandlungsziel kann daher nur sein, eine Progression zu verhindern. Schlägt eine symptomatische Therapie der MG mit Pyridostigmin fehl, benötigen die Patienten eine krankheitsmodifizierende Immuntherapie und ggf. zusätzlich Glukokortikoide. Wegen der Nebenwirkungen ist eine steroidsparende Strategie indiziert. Bevorzugt eingesetzt werden Azathioprin, Mycophenolat-Mofetil, Methotrexat, Ciclosporin und Tacrolimus.
Azathioprin laut Experten zu Recht die erste Wahl
Azathioprin wird derzeit am häufigsten eingesetzt und ist auch laut Expertenmeinung die erste Wahl. Für das Nitroimidazol spricht unter anderem eine randomisierte Doppelblindstudie, in der Prednisolon mit und ohne Azathioprin (2,5 mg/kgKG/d) verabreicht wurde. Nach zwei Jahren Therapie benötigte die Gruppe unter Azathioprin deutlich weniger Steroide. Zudem kam es seltener zu einem Therapieversagen und die erzielten Remissionen hielten länger an.
Die Daten zu Mycophenolat-Mofetil (MMF) sind noch uneinheitlich. Eine prospektive Multicenterstudie ergab eine deutliche Verbesserung der Symptome, weshalb dieser Wirkstoff in manchen Leitlinien ebenfalls empfohlen wird. Für Ciclosporin ist der Effekt bei MG belegt. Sein Einsatz wird jedoch dadurch limitiert, dass schwere Nebenwirkungen möglich sind (z.B. Nephrotoxizität). Methotrexat kommt vor allem für solche Patienten infrage, die auf andere steroidsparende Wirkstoffe nur unzureichend ansprechen, diese nicht vertragen oder zusätzlich an rheumatischen Erkrankungen leiden.
Was den B-Zell-Antikörper Rituximab betrifft, sprechen frühere Beobachtungsstudien für eine Wirkung bei der Myasthenie. Von ihm profitieren vor allem Patienten mit MuSK-Autoantikörpern oder längerer Krankheitsdauer (z.B. wegen Therapieresistenz).
Einen hohen Stellenwert besitzt nach wie vor die Thymektomie. Verglichen mit Prednisolon allein verbesserte der operative Eingriff den Therapieerfolg bei Patienten mit AChR-Autoantikörpern, aber ohne Thymom. Der Therapieerfolg blieb fünf Jahre erhalten. Die Operation kommt auch in Betracht, wenn seronegative Personen mit generalisierter MG unzureichend auf die immunsuppressive Therapie ansprechen. Bei MuSK-, LRP-4- oder Agrin-Autoantikörpern wird die Intervention allerdings nicht empfohlen.
Rascher wirksame Optionen wie die Plasmapherese und die intravenöse Gabe von Immunglobulinen werden vor allem zur Behandlung akuter Exazerbationen und drohender myasthener Krisen mit Ateminsuffizienz eingesetzt. Sie eignen sich auch zur Überbrückung bei verzögert wirksamen Medikamenten, wenn man Steroide sparen will.
Immuntherapeutika setzen am Komplementsystem an
Inzwischen wurden zielgerichtete Immuntherapeutika für den Einsatz bei MG entwickelt. Basis dafür war die Erkenntnis, dass die Aktivierung des Komplementsystems bei Myasthenie eine wichtige Rolle spielt. Für den Komplementinhibitor Eculizumab konnten die Wirksamkeit und Sicherheit bei Patienten mit therapierefraktärer AChR-positiver Erkrankung in einer Studie gezeigt werden. Eine länger wirksame Alternative ist Rivalizumab. Dieser Antikörper inhibiert das terminale Komplementprotein C5. Dadurch verbessern sich die klinischen Symptome der Patienten und ihre Bewältigung von Alltagsaktivitäten.
Allerdings ist zu beachten, dass das Komplementsystem zur Abwehr kapselbildender Bakterien wie Meningokokken benötigt wird. Deshalb ist eine entsprechende Impfung und/oder eine präventive Antibiotikatherapie obligatorisch.
Einen neuen therapeutischen Ansatz bietet der Fc-Rezeptorantagonist Efgartigimod. Er reduziert Serum-IgG und AChR-Antikörper. In einer randomisierten kontrollierten Studie verbesserte das die Muskelkraft und die Lebensqualität der Betroffenen. Eculizimab, Rivalizumab und Efgartigimod sind inzwischen zur Behandlung bei der Myasthenia gravis zugelassen. Bei allen neueren Therapien ist den Autorinnen zufolge jedoch das Wissen über unerwünschte Ereignisse noch begrenzt. Daher sollte man während der Behandlung besonders auf belastende Nebenwirkungen achten.
Quelle: Tatsch L, Schreiner B. Swiss Arch Neurol Psychiatr Psychother 2023; 174: 106-109; DOI: 10.4414/sanp.2023.03396
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).




