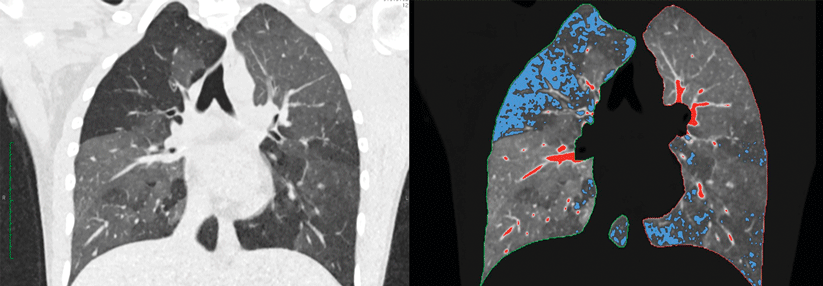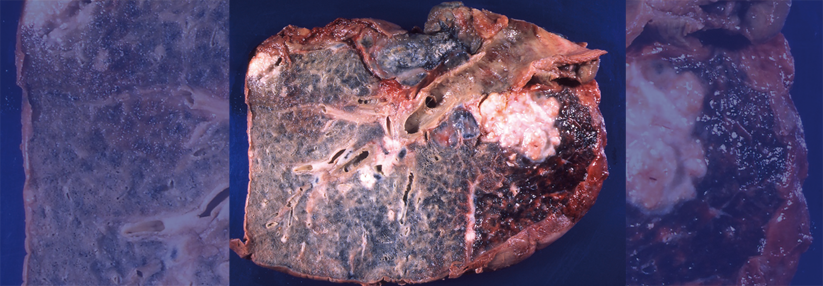
Ergänzung des TKI um weiteren Wirkstoff bietet Optionen nach Therapieversagen
 Bei Progress unter Erstlinienbehandlung könnte die EGFR-Therapie mit einem zusätzlichen Wirkstoff kombiniert werden.
© utah51 – stock.adobe.com
Bei Progress unter Erstlinienbehandlung könnte die EGFR-Therapie mit einem zusätzlichen Wirkstoff kombiniert werden.
© utah51 – stock.adobe.com
Viele Patient:innen mit EGFR-mutiertem (EGFRm) NSCLC werden auch unter modernen Kinaseinhibitoren wie Osimertinib irgendwann progredient. Eine MET-Amplifikation stellt einen der häufigsten erworbenen Resistenzmechanismen dar und findet sich je nach Quelle bei 7–50 %, erinnerte Prof. Dr. Dr. Myung-Ju Ahn, Samsung Medical Center, Seoul.1
Forschende testeten in der Phase-2-Studie SAVANNAH eine Kombination aus Osimertinib und dem MET-Inhibitor Savolitinib für Betroffene mit einem fortgeschrittenen, EGFRm NSCLC und MET-Überexpression oder -Amplifikation, die unter dem EGFR-TKI einen Progress entwickelt hatten. Die vorgestellte Wirksamkeitsanalyse beschränkte sich auf 80 Erkrankte, bei denen Osimertinib in der Erstlinie versagt hatte, und die strenge Kriterien an die MET-Expression erfüllten (IHC 3+/ ≥ 90 % und/oder FISH10+). Alle erhielten zweimal täglich 300 mg Savolitinib, und einmal täglich Osimertinib (80 mg).
Gut ein Fünftel nach einem Jahr noch ohne Progress
Nach Beurteilung der Verantwortlichen sprachen 56 % auf die Therapie an und die ORR schien über die prädefinierten Subgruppen hinweg konstant. „Die Ansprechdauer war relativ lang – sie betrug median 7,1 Monate gemäß den Investigator:innen“, ergänzte die Expertin. Das von den Forschenden ermittelte mPFS lag bei 7,4 Monaten, nach einem Jahr lebten noch 21 % progressionsfrei.
„Periphere Ödeme waren das häufigste unerwünschte Ereignis, was mit anderen MET-TKI übereinstimmt“, schilderte Prof. Ahn. 57 % der Behandelten erlitten Beschwerden vom Grad 3 oder höher. Am häufigsten handelte es sich dabei ebenfalls um periphere Ödeme (11 %) sowie eine Erhöhung der Alanin-Aminotransferase (6 %) und Pneumonien (5 %).
Nach Ansicht der Referentin könnten 300 mg Savolitinib zweimal täglich + Osimertinib eine neue chemofreie Option für Patient:innen bieten, die die Einschlusskriterien der vorgestellten Analyse erfüllen. Die Kombination wird nun in der Phase-3-Studie SAFFRON mit einer Platin-Pemetrexed-Chemotherapie verglichen.
Kombinationstherapie aus Kinaseinhibitor und ADC
Prof. Dr. Dr. Xiuning Le, MD Anderson Cancer Center, Houston, präsentierte wiederum Daten aus der Plattformstudie ORCHARD zu Datopotamab-Deruxtecan (Dato-DXd), einer biomarkeragnostischen Behandlungsoption.2 69 Patient:innen mit EGFRm NSCLC, die unter der Erstlinie mit Osimertinib progredient wurden, erhielten zusätzlich zum Kinaseinhibitor (80 mg täglich) das gegen TROP2 gerichtete ADC (4 mg/kgKG oder 6 mg/kgKG dreiwöchentlich).
Die Kollegin betonte, dass sie und ihr Team mit beiden Dosisleveln einen klinischen Nutzen beobachteten: „Bei der Mehrheit der Erkrankten schrumpfte der Tumor.“ Das mediane PFS (11,7 Monate vs. 9,5 Monate) und die Ansprechdauer (20,5 Monate vs. 6,3 Monate) fielen allerdings in der 6-mg-Kohorte deutlich länger aus. Auch sprachen Erkrankte mit der intensiveren Behandlung schneller an (1,4 Monate vs. 2,7 Monate). Die ORR unterschied sich hingegen kaum (36 % vs. 43 %).
Die mediane Behandlungsdauer und die Rate an Therapieunterbrechungen ähnelten sich zwischen den Gruppen. Die Referentin merkte gleichwohl an: „Nach vier bis fünf Zyklen erhielt mehr als die Hälfte der Patient:innen eine Dosisreduktion von 6 mg/kgKG auf 4 mg/kgKG.“ Mit 6 mg/kgKG Dato-DXd erlitten zudem deutlich mehr Teilnehmende unerwünschte Ereignisse vom Grad 3 oder höher (74 % vs. 49 %). Insgesamt traten aber keine neuen Sicherheitssignale auf.
Aus Sicht von Prof. Le stellen 6 mg/kgKG die bevorzugte Startdosis von Dato-DXd in Kombination mit 80 mg Osimertinib dar. Insgesamt habe das Duo vielversprechende Effizienz gezeigt. Das ADC werde somit beim fortgeschrittenen NSCLC mit und ohne Osimertinib weiter erforscht.
Herausforderungen bei biomarkerbasierten Ansätzen
Laut Prof. Saw gestaltet sich die Rekrutierung von ausreichend Teilnehmenden für klinische Studien, die auf spezifische Resistenzmechanismen abzielen, oft als schwierig. Zudem erfordert die Biomarkerbestimmung eine Biopsie mit den assoziierten Risiken. Nicht alle Erkrankten stimmen zu oder haben einen zugänglichen Tumor. Darüber hinaus müssten manche Patient:innen direkt mit der Therapie starten und könnten nicht erst auf das Ergebnis warten.
Bisher keine Relevanz für die klinische Praxis
Ohne weitere Daten hält die Diskutantin Prof. Dr. Stephanie P. L. Saw, National Cancer Centre Singapore, keine dieser Behandlungsoptionen für unmittelbar praxisverändernd.3 Hinsichtlich der SAVANNAH-Ergebnisse verwies sie auf Probleme bei der Etablierung biomarkerbasierter Ansätze (s. Kasten). Generell hätten verschiedene Studien belegt, dass man MET-Inhibitoren stets mit EGFR-TKI kombinieren sollte. „Im Allgemeinen wird die Hälfte oder mehr der Patient:innen ansprechen und ein medianes PFS von fünf bis sieben Monaten erreicht“, fasste die Expertin die Erfahrungen zusammen. Die typischen peripheren Ödeme seien lästig, aber meist nicht lebensbedrohlich.
Im Bezug auf Dato-DXd + Osimertinib erinnerte die Diskutantin an die hohe Rate von Dosisreduktionen und Toxizitäten, besonders mit 6 mg/kgKG des ADC. Bei dem Wirksamkeitsunterschied zwischen den Dosisleveln könnte es eine Rolle gespielt haben, dass mehr Personen in der 4-mg-Gruppe einen frühen Progress erlitten hatten oder Metastasen in Leber und ZNS aufwiesen. Offen bleibe zudem, inwiefern der EGFR-TKI einen Zusatznutzen bringt. Es gebe bereits Daten zu einer Monotherapie mit Dato-DXd, die sich allerdings aufgrund einer stärkeren Vorbehandlung der Teilnehmenden nur eingeschränkt vergleichen lassen. „Es scheint, dass zumindest die Toxizität höher ist, wenn man Dato-DXd mit Osimertinib kombiniert“, gab Prof. Saw zu bedenken.
Für beide vorgestellten Kombinationen bleibt zudem unklar, wie gut Betroffene intrakranial ansprechen. Nicht zuletzt müsse man überdenken, ob Cisplatin/Pemetrexed noch einen angemessenen Vergleichsstandard nach Osimertinibversagen darstelle. Mittlerweile hätten mindestens vier Protokolle diesen in Phase-3-Studien übertroffen. Der Stellenwert dieser neuen Regime bleibe demzufolge unklar, auch falls weitere Untersuchungen positiv ausfallen.
Quellen:
1. Ahn MJ et al. European Lung Cancer Congress 2025; Abstract 2O
2. Le X et al. European Lung Cancer Congress 2025; Abstract 1O
3. Saw PLS. European Lung Cancer Congress 2025; Invited Discussant 2O, 3O and 1O
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).