Infantiles Hämangiom: Leitlinie gibt konkreten Therapierahmen vor
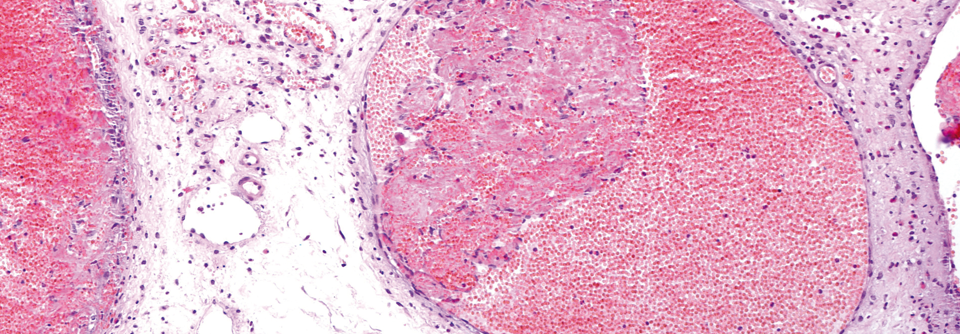 Infantile Hämangiome entstehen durch Proliferation von Endothelzellen.
© Science Photo Library/JOSE CALVO
Infantile Hämangiome entstehen durch Proliferation von Endothelzellen.
© Science Photo Library/JOSE CALVO
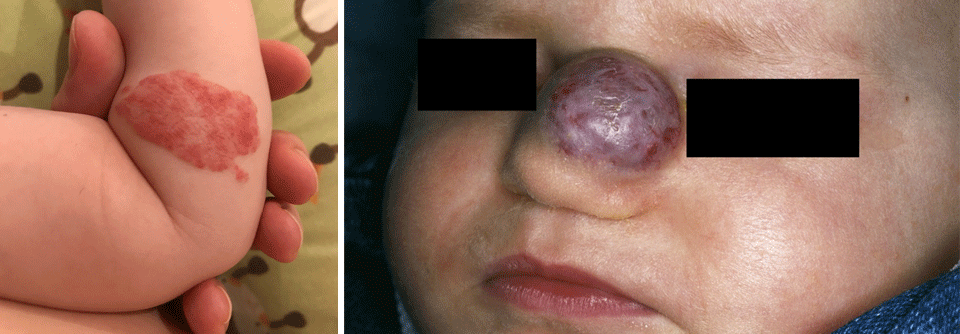
Generell durchlaufen infantile Hämangiome drei Phasen. Durch starke Proliferation findet zunächst das Wachstum statt. Dieser Prozess endet meist nach dem sechsten bis neunten Lebensmonat. Darauf folgen Übergangs- und Involutionsphase. Letztere kann sich je nach Größe des Hämangioms über acht bis zehn Jahre ausdehnen.
Hämangiome richtig einordnen
Während sich die kleinen kutanen Vertreter der benignen Tumoren i.d.R. wieder komplett zurückbilden, bleiben bei größeren in mehr als der Hälfte der Fälle Residuen zurück. Dies ist vor allem bei komplizierten Hämangiomen der Fall, schreiben die Autoren der neuen S2k-Leitlinie zum infantilen Hämangiom im Säuglings- und Kleinkindesalter unter der Leitung von Privatdozentin Dr. Bettina Lange von der Universitätsmedizin Mannheim. Als kompliziert wird der Blutschwamm eingestuft, wenn er
- zu funktionellen Beeinträchtigungen oder Ulzerationen führt,
- mit weiteren Komplikationen wie sekundärer Hypothyreose und extrakutanen Manifestationen oder Fehlbildungen verbunden ist bzw.
- für eine langfristige ästhetische Beeinträchtigung sorgt.
Differenzialdiagnostisch gilt es, andere vaskuläre Tumoren oder Malformationen auszuschließen. Für Letzteres sprechen z.B. Vorhandensein schon bei der Geburt und nur langsames, aber stetiges Wachstum in den ersten Monaten.
Differenzialdiagnosen
- kongenitales Hämangiom
- Granuloma pyogenicum
- kaposiformes Hämangioendotheliom
- Dermoidzyste
- nasales Gliom
- Myofibrom
- Sarkom
- arteriovenöse, venöse, lymphatische, kapilläre oder kombinierte Malformation des Gefäßsystems
- assoziierte Syndrome wie Sturge-Weber oder Proteus
Wie therapieren?
Therapeutisch lassen sich drei Ziele definieren:- früher Wachstumsstopp und Beschleunigen der Rückbildung des Hämangioms
- Prävention von Einschränkungen (funktionell und ästhetisch)
- Abheilen von Ulzerationen (z.B. im Anogenitalbereich oder in intertriginösen Regionen)
Steckbrief infantiles Hämangiom
- proliferierender benigner Gefäßtumor, der kutan, subkutan oder als Mischform vorkommen kann
- tritt bei 4–5 % aller Säuglinge auf
- betrifft meist Kopf- und Halsregion
- wird typischerweise erst postpartal in den ersten Tagen/Wochen sichtbar (imponiert bei der Geburt nie als Tumor)
- in ca. 90 % der Fälle lokalisiert, scharf begrenzt und von einem zentralen Fokus ausgehend
- Wachstum in den ersten Lebensmonaten schnell, danach langsam mit späterer Regression
- Risikofaktoren: weibliches Geschlecht, helle Hautfarbe, Frühgeburt mit Geburtsgewicht < 1000 g
Nebenwirkungen der Therapie sind i.d.R. passager
Die Einstellung erfolgt in der Regel von 1 mg/kgKG/d auf eine Zieldosis von 2(–3) mg/kgKG/d, verteilt auf zwei bzw. drei Einzeldosen. Die Aufdosierungsintervalle richten sich danach, ob die Therapie ambulant (wöchentliche Abstände) oder stationär (tägliche Steigerung) eingeleitet wird. Alle vier Wochen sollte die Wirkstoffmenge an das Körpergewicht des Patienten angepasst werden. Bei knapp jedem dritten Kind kann es durch die Therapie zu passageren Nebenwirkungen wie Schlafstörungen, kalten Extremitäten oder Durchfall kommen. Dies ist insbesondere bei sehr jungen Patienten (< 3 Monate) der Fall. Für einen negativen Einfluss auf die psychische beziehungsweise kognitive Entwicklung der Kinder gibt es bislang keine Belege – auch wenn Propranolol die Blut-Hirn-Schranke überwinden kann. Nach Ende der Gabe kommt es bei 15–20 % der Behandelten zu einem kurzzeitigen Rebound. Darauf sollte man die Eltern im Voraus hinweisen. Risikofaktoren sind weibliches Geschlecht, subkutan-kutane Hämangiom-Mischformen und eine zu kurze Therapiedauer (< 6 Monate). Präventiv wird daher die Behandlung oft bis auf zwölf Monate verlängert. Bleiben funktionell bzw. ästhetisch einschränkende Überbleibsel bis über das vierte Lebensjahr hinaus erhalten, können diese z.B. mittels Laser- oder Blitzlampentherapie angegangen werden. Bei Narben, Gewebeüberschuss oder Asymmetrien kommt ggf. eine chirurgische Korrektur infrage. Hämangiom und Therapiespuren sollten bis zur Einschulung des Kindes beseitigt worden sein, heißt es in der Leitlinie.Quelle: S2k-Leitlinie Infantile Hämangiome im Säuglings- und Kleinkindesalter, AWMF-Register-Nr. 006/100, www.awmf.org
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).