HFpEF Kraftwerke ohne Saft
 Die Mitochondrien funktionieren bei HFpEF schlechter.
© Dr_Microbe - stock.adobe.com
Die Mitochondrien funktionieren bei HFpEF schlechter.
© Dr_Microbe - stock.adobe.com
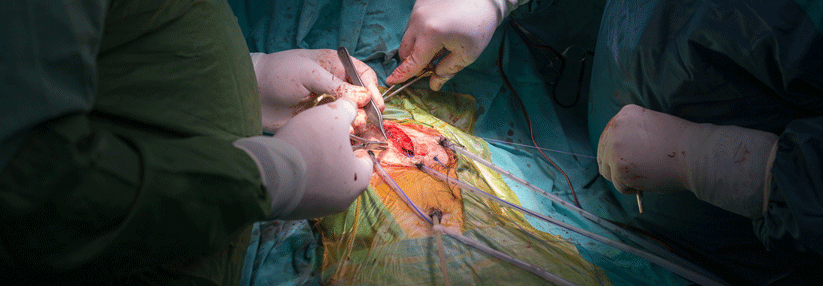
Warum sind Herzinsuffizienzpatienten mit erhaltener Pumpfunktion so stark in ihrer Belastbarkeit eingeschränkt? Der Grund dafür liegt offenbar nicht im Herzen, sondern in den Mitochondrien.
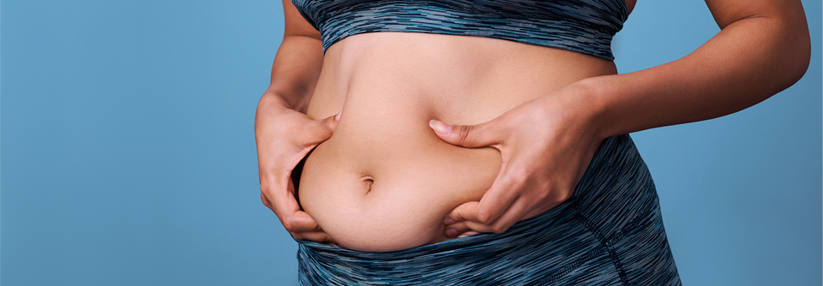
Die Herzinsuffizienz mit erhaltener linksventrikulärer Pumpfunktion (HFpEF) ist gerade bei älteren Patienten die häufigste Form der Herzschwäche. Dementsprechend nimmt ihre Prävalenz der demografischen Kurve folgend stetig zu. Wichtigstes klinisches Merkmal: die Belastungsintoleranz, die sich über Messung der maximalen Sauerstoffkapazität (VO2max) objektivieren lässt. Unklar war bisher, welche Mechanismen dieser Intoleranz zugrunde liegen. Es gibt aber Hinweise darauf, dass ein abnormer…
Bitte geben Sie Ihren Benutzernamen und Ihr Passwort ein, um sich an der Website anzumelden.