Krebstherapie fördert Autoimmunreaktionen gegen Bronchialgewebe
 Mancher Patient klagt
über Brustbeklemmung, Dyspnoe, Husten,
manchmal Fieber oder
asthmaähnliche Symptome.
© iStock/KatarzynaBialasiewicz
Mancher Patient klagt
über Brustbeklemmung, Dyspnoe, Husten,
manchmal Fieber oder
asthmaähnliche Symptome.
© iStock/KatarzynaBialasiewicz
Die Immuntherapie hat sich aufgrund deutlicher Verbesserungen bei Überlebenszeit und Lebensqualität innerhalb weniger Jahre zu einem wichtigen Therapieprinzip in der Onkologie etabliert. Bei Malignomen von Lunge, Niere und Schilddrüse sowie beim Melanom und Merkelzellkarzinom gehört sie schon heute mit zum Standardregime, schreiben Dr. Sawsan Rashdan von der Division of Hematology-Oncology der Universität Texas in Dallas und Kollegen.
Autoimmunreaktionen in Haut und Darm sind möglich
Eine wichtige Medikamentengruppe sind die Immuncheckpoint-Inhibitoren. Sie besetzen immunmodulierende Rezeptoren auf T-Lymphozyten und anderen Effektorzellen. Dadurch aktivieren sie die körpereigene Abwehr und erleichtern so die Attacken auf Krebszellen. Eingesetzt werden derzeit CTLA-4(Cytotoxic T-lymphocyte antigen 4)- und PD-1(Programmed death 1)- bzw. PD1-Liganden-Antikörper wie Ipilimumab, Pembrolizumab oder Nivolumab. Doch ganz spezifisch läuft der Ansatz nicht ab, bei einigen Patienten kommt es unter der Therapie zu Autoimmunreaktionen, z.B. in Haut oder Darm. Auch Zellen des Pulmonal-/Bronchialsystems stehen nun gehäuft im Visier.
Die Inzidenz pulmonaler Nebenwirkungen liegt bei 2–5 %, Männer, (Ex-)Raucher und Lungenkrebspatienten vor allem unter zusätzlicher Strahlentherapie trifft es häufiger und teilweise auch schwerer. Die Toxizitäten können sich praktisch zu jedem Therapiezeitpunkt manifestieren, typischerweise jedoch 2–3 Monate nach Behandlungsbeginn.
Klinisch präsentieren sich die toxischen Schäden an der Lunge eher unspezifisch. Die Patienten klagen über Dyspnoe, Brustbeklemmung, Husten und manchmal Fieber oder asthmaähnliche Beschwerden. Das Problem vor allem bei Lungenkarzinompatienten: Die Nebenwirkungen unterscheiden sich klinisch kaum von krankheitsbedingten Beschwerden und können auch durch behandlungsassoziierte Infektionen oder Anämien ausgelöst werden.
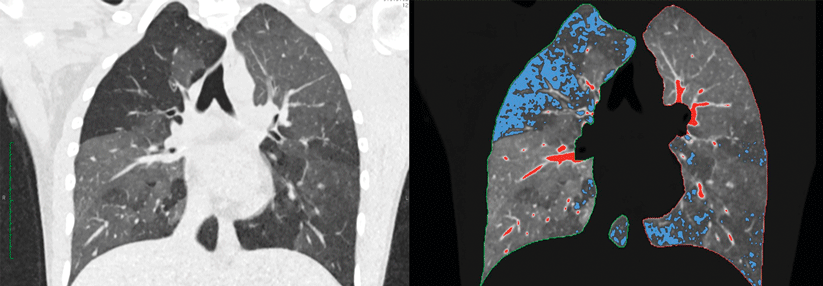
Die Lungenfunktionsprüfung ergibt in der Regel eine reduzierte Diffusionskapazität mit verschlechterten Werten in Pulsoxymetrie, Spirometrie und bei der Kohlenmonoxid-Diffusionskapazität. Im CT als Diagnostikum der ersten Wahl liefern Pneumonie- bzw. Pneumonitis- und in manchen Fällen auch Bronchiolitis-Zeichen weitere Hinweise. Allerdings lassen sich die Auffälligkeiten nicht immer hinreichend von krebsbedingten Veränderungen unterscheiden.
Die Bronchoskopie hilft bei der Abgrenzung einer Checkpoint-Inhibitor-induzierten Pneumonitis gegen pulmonale Infektionen bzw. eine Lymphangitis carcinomatosa. In der bronchoalveolären Lavage findet man häufig eine erhöhte Zahl von Entzündungszellen. Geeignete Biomarker existieren derzeit noch nicht.
Trotz möglicher Unsicherheiten in der Diagnostik muss man bei klinisch manifesten pulmonalen Reaktionen sofort handeln – bei hinreichendem Verdacht schon vor Bekanntwerden der Untersuchungsergebnisse, mahnen die Onkologen. Wichtigste Maßnahme ist das sofortige Absetzen der Immuntherapie. Eine Dosisreduktion wie bei der konventionellen Chemo- oder bei zielgerichteten Therapien bringt bei den Checkpoint-Inhibitoren nichts.
Steroidstoß bei klinisch manifester Pneumonitis
Bei asymptomatischer Pneumonitis reicht der Therapiestopp alleine meist aus. Patienten mit klinisch manifester Entzündung benötigen zusätzlich Kortikosteroide in Anfangsdosierungen von 1 mg/kg/d Prednisolon-Äquivalent, erst nach deutlicher Beschwerdebesserung wird langsam zurücktitriert. Eine solche Kortikosteroidtherapie kann sich über Monate hinziehen und die Kranken entsprechend belasten, neue verkürzte Regimes zur Minimierung von Nebenwirkungen befinden sich in Erprobung.
Reexposition nur nach leichter Symptomatik wagen
Bei Steroidrefraktärität kommen zusätzlich Immunsuppressiva wie Infliximab oder Cyclophosphamid zum Einsatz. Biologika erhöhen zwar das Risiko für Krebs und chronische Infektionen, die Nutzen-Risiko-Abwägung fällt bei den meisten Patienten dennoch positiv aus. Ein erneuter Checkpoint-Inhibitor-Einsatz sollte nach bisherigem Kenntnisstand vor allem nach einer schweren, d.h. in der Regel intensivmedizinisch betreuten Pneumonitis unterbleiben. Bei Patienten mit nur leichter Symptomatik kann man eine vorsichtige Reexposition wagen. Hatte sich unter der Behandlung der Tumor schon deutlich zurückgebildet, bleibt dieser Effekt auch ohne Wiederaufnahme der Behandlung lange Zeit erhalten, so die Ergebnisse einiger retrospektiver Studienauswertungen. In diesen Fällen sollte ebenfalls auf eine Wiederaufnahme der Immuntherapie verzichtet werden.
Quelle: Rashdan S et al. Lancet Respir Med 2018; 6: 472-478
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).