Metformin schützend, Sulfonylharnstoffe gefährlich?
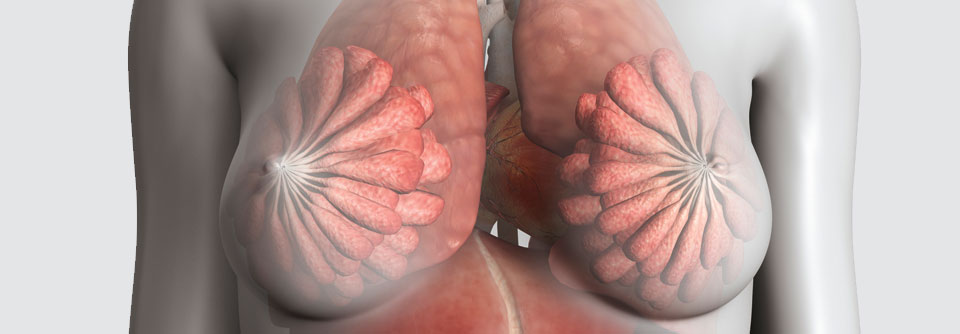
 Experimentelle Modelle haben gezeigt, dass erhöhte Spiegel von Insulin und insulin-like growth factor die Tumorgenese fördern.
© Marazzi, Dr. P - stock.adobe.com
Experimentelle Modelle haben gezeigt, dass erhöhte Spiegel von Insulin und insulin-like growth factor die Tumorgenese fördern.
© Marazzi, Dr. P - stock.adobe.com
Diabetes mellitus kann auf unterschiedlichen Wegen die Neubildung von Malignomen fördern. Dazu zählen Hyperinsulinämie, Hyperglykämie und chronische Entzündungen. Epidemiologischen Studien zufolge erhöht die Stoffwechselstörung die Inzidenz diverser Krebsarten, darunter auch die des Mammakarzinoms. 16 % der Patientinnen mit Brustkrebs sind gleichzeitig zuckerkrank. Die steigende Brustkrebsinzidenz in westlichen Ländern wird vornehmlich auf Faktoren wie sedentären Lebensstil und ungesunde Ernährung zurückgeführt, schreiben Prof. Dr. Wojciech Garczorz von der Medical University of Silesia in Katowice und Kollegen.
Eine Adipositas, die häufig mit einer derartigen Lebensweise einhergeht, begünstigt ihrerseits die Entstehung von Mammakarzinomen, insbesondere bei postmenopausalen Frauen. Große Bedeutung kommt dabei der hormonellen Aktivität des Fettgewebes zu.
Die Interaktion zwischen Diabetes und Brustkrebs bzw. dessen Behandlung betreffen auch die medikamentöse Tumortherapie: Verschiedene Wirkstoffe können eine Hyperglykämie auslösen. Als Reaktion darauf wird unter Umständen die Krebsmedikation reduziert. Allerdings kommen diese Substanzen üblicherweise nicht in der Erstlinientherapie des Mammakarzinoms zum Zuge. Die potenziellen Auswirkungen von Antidiabetika auf das Brustkrebsrisiko sind wiederum unterschiedlich.
Insulin
Experimentelle Modelle haben gezeigt, dass erhöhte Spiegel von Insulin und insulin-like growth factor die Tumorgenese fördern. Die Peptide beeinflussen neben dem Blutzuckerspiegel auch Proliferation und Differenzierung von Zellen sowie die Apoptose. Insulin und seine Analoga erhöhen den Insulinspiegel und steigern das Risiko für Pankreas- und Darmkrebs. Bedenken hinsichtlich der Entwicklung von Karzinomen bestehen vor allem bei den langwirksamen Analoga Insulin glargin, Insulin detemir und Insulin degludec. Allerdings wurde ein möglicher Zusammenhang überwiegend in Studien mit relativ kurzer Laufzeit (< 5 Jahre) geprüft, Langzeitdaten gibt es kaum. Zudem sind die Studienergebnisse uneinheitlich.
So ergab eine retrospektive Untersuchung für Brustkrebspatientinnen, die Insulin erhielten, eine Reduktion sowohl des krankheitsfreien Fünf-Jahres- als auch des Gesamtüberlebens – im Vergleich zu Teilnehmerinnen ohne Diabtes. Eine weitere gepoolte Auswertung kam zu dem Ergebnis, dass die Brustkrebssterblichkeit unter Insulin erhöht ist. Die Rezidivate wurde in vier der elf einbezogenen Studien beeinflusst.
Eine Metaanalyse hingegen ermittelte für Insulin zwar eine Assoziation zu Malignomen allgemein, nicht aber zum Mammakarzinom. Und eine weitere Metaanalyse aus dem vergangenen Jahr zeigte sogar, dass mit Insulinen behandelte Diabetikerinnen im Vergleich zu Patientinnen ohne diese Therapie ein geringeres Brustkrebsrisiko tragen. Für Insulin glargin konnte in einer gemeinsamen Auswertung von 13 epidemiologischen Studien kein Zusammenhang mit dem Mammakarzinom gefunden werden.
Sulfonylharnstoffe
In einer retrospektiven Kohortenstudie zu Sulfonylharnstoffen wurden die Daten von mehr als 16.000 Frauen zwischen 60 und 80 Jahren ausgewertet. Alle litten an einem Mammakarzinom im Stadium 1 oder 2. Die Behandlung mit Sulfonylharnstoffen war mit einer erhöhten brustkrebsbedingten Mortalität verbunden (Hazard Ratio, HR, 1,49).
Jedoch zeigte sich hinsichtlich des kombinierten Endpunkts aus Rezidiv und Tod kein Unterschied zwischen Patientinnen mit und ohne eine Therapie mit Sulfonylharnstoffen. In einer neueren Arbeit mit 9.221 Teilnehmerinnen war die Gesamtmortalität unter dieser Therapie höher als unter Metformin (HR 1,44). Daten aus qualitativ hochwertigen prospektiven Untersuchungen (beispielsweise ZODIAC 55) stehen trotz des weitverbreiteten Einsatzes der Sulfonylharnstoffe noch aus.
Metformin
Die Therapie mit Metformin hat möglicherweise einen antikanzerogenen Effekt. Studienergebnisse sprechen dafür, dass Frauen unter dem Biguanid verglichen mit anderen Wirkstoffklassen (z.B. Sulfonylharnstoffe) seltener ein invasives Mammakarzinom entwickeln (HR 0,75). Diese Assoziation gilt auch für Malignome, die östrogen- und progesteronrezeptorpositiv sind. Patientinnen mit HER2*-positivem Tumor zeigten unter Metformin sowohl ein längeres krankheitsfreies als auch Gesamtüberleben. In einer Metaanalyse mit mehr als 31.000 Brustkrebspatientinnen waren diejenigen, die Metformin erhielten, signifikant im Vorteil hinsichtlich der allgemeinen Sterblichkeit und des progressionsfreien Überlebens (HR 0,77 bzw. 0,64).
GLP1-Rezeptoragonisten
Hinweise aus tierexperimentellen und In-vitro-Studien, wonach GLP1-Rezeptoragonisten möglicherweise die Karzinogenese in Betazellen fördern, konnten für Menschen mit Diabetes Typ 2 klar widerlegt werden. Studienergebnisse zeigen eindeutig, dass die Inkretinmimetika das Brustkrebsrisiko nicht erhöhen. In einer Metaanalyse mit über 48.000 Teilnehmerinnen entwickelten 130 Frauen, die einen GLP-1-Rezeptoragonisten erhalten hatten, ein Mammakarzinom. Ohne das waren es 107. Somit bestand kein signifikanter Unterschied. Auch benigne Neoplasien traten nicht vermehrt auf.
Glitazone
In-vitro-Daten sprechen dafür, dass Glitazone die Proliferation maligner Zellen hemmen könnten. Die Studienlage zu diesen auch als Insulinsensitizer bezeichneten Wirkstoffen ist jedoch widersprüchlich: Eine Metaanalyse zum Mammakarzinom ergab keine Assoziation mit der Einnahme von Glitazonen. Eine neuere gepoolte Analyse fand zumindest ein geringeres Risiko (RR 0,87).
DPP4-Inhibitoren
Bedenken gab es zudem zunächst gegenüber Dipeptidylpeptidase-4(DPP4)-Hemmern. Was das Risiko für Pankreas- und Schilddrüsenkarzinome angeht, zeigte eine Metaanalyse jedoch keine signifikanten Veränderungen. Auch Brustkrebs wurde unter Gliptinen in randomisierten kontrollierten Untersuchungen nicht vermehrt dokumentiert, in Beobachtungsstudien trat er sogar seltener auf. Die durchschnittliche Laufzeit der eingeschlossenen Arbeiten war allerdings mit 1,5 Jahren zu kurz für eine endgültige Einschätzung, schreiben Prof. Garczorz und Kollegen.
SGLT2-Inhibitoren
In einer Metaanalyse randomisierter Studien mit knapp 50.000 Teilnehmern konnte für Gliflozine hinsichtlich der Malignominzidenz kein Unterschied zu Vergleichssubstanzen gezeigt werden (Odds Ratio 0,98). Eine neuere gepoolte Auswertung berücksichtigte die Daten von fast 100.000 Erwachsenen. Den Studienautoren zufolge zeigten SGLT2-Hemmer bei einer Mindestbeobachtungszeit von 48 Wochen nur einen geringen bis gar keinen Einfluss auf das Brustkrebsrisiko (relatives Risiko 1,01). Für eine zuverlässige Einschätzung müssen den Autoren zufolge jedoch die Ergebnisse aktuell laufender Studien abgewartet werden.
* human epidermal growth factor receptor 2
Quelle: Garczorz W et al. Cancers 2024; 16: 299; DOI: 10.3390/cancers16020299
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).