PD(-L)1-Inhibitoren benötigen anscheinend Kombinationspartner
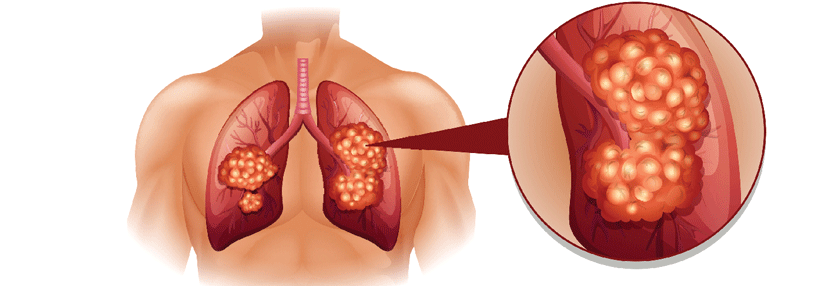
 Obwohl die Tumormutationslast beim SCLC sehr hoch ist, zeigt dieser Tumor insgesamt paradoxerweise eine geringe Expression von PD-L1.
© iStock/peterschreiber.media
Obwohl die Tumormutationslast beim SCLC sehr hoch ist, zeigt dieser Tumor insgesamt paradoxerweise eine geringe Expression von PD-L1.
© iStock/peterschreiber.media
In einer Cochrane-Analyse von 32 Studien mit über 6.000 SCLC-Patienten mit meist fortgeschrittener Erkrankung betrug die Überlebensrate nach einem Jahr 29,4 % und nach zwei Jahren 6,9 %. Für weniger fortgeschrittene Fälle betrug sie auch nur 21,1 %. In bisherigen Studien mit PD(-L)1-Inhibitoren brachten es Atezolizumab, Durvalumab und Pembrolizumab zusätzlich zu einer platinbasierten Chemotherapie auf etwa 50 % nach einem Jahr und über 20 % nach zwei Jahren.
Professor Dr. Luis Paz-Ares, Hospital Universitario, Madrid, präsentierte die Daten der CASPIAN-Studie nach drei Jahren Beobachtung. Die Überlebensrate unter Durvalumab plus Etoposid/Platin war mit 17,6 % dreimal so hoch wie unter alleiniger Chemo (5,8 %). Dieses Regime gilt mittlerweile als Erstlinienstandard beim fortgeschrittenen SCLC.
Im Vergleich zu anderen Tumoren wird PARP1 in Zellen des SCLC stark exprimiert, weshalb PARP-Inhibitoren hier ebenfalls greifen, berichtete Dr. Catherine Meador, Dana-Farber Cancer Institute, Boston. Darüber hinaus wirken PARP-Hemmer in präklinischen Modellen synergistisch mit Medikamenten, die Einzelstrangbrüche in der DNA verursachen wie Temozolomid.
T-Zell-Engager als Zusatz
Ansprechrate überzeugt zwar, Gesamtüberleben aber nicht
In einer Phase-2-Studie konnten Veliparib und Temozolomid beim rezidivierten SCLC das Ansprechen, aber nicht das PFS nach vier Monaten verbessern. Da Olaparib eine stärkere PARP-inhibierende Wirkung aufweist als Veliparib, wird dieser in einer Phase-1/2-Studie kombiniert mit Temozolomid nun geprüft. Die Ansprechrate von 41,7 % in der Phase 1 „war vielversprechend“. Die Dosis in Phase 2 umfasste 200 mg Olaparib zweimal täglich mit kontinuierlicher Gabe und Temozolomid à 75 mg/m2 an den Tagen 1–7 eines dreiwöchigen Zyklus. Die Ansprechrate überzeugte erneut, wobei eine intermittierende Gabe beider Medikamente an den Tagen 1–7 jedes Zyklus mit höheren Raten assoziiert war als kontinuierliches Olaparib. Das OS ähnelte sich in beiden Armen. Obwohl die Tumormutationslast beim SCLC sehr hoch ist, zeigt dieser Tumor insgesamt paradoxerweise eine geringe Expression von PD-L1 und ein relativ immunsuppressives Tumor-Microenvironment mit weniger infiltrierenden T-Zellen. In-vitro-Versuche ergaben, dass zusätzliche PARP-Inhibitoren die Expression von PD-L1 stimulieren, die sich bei Kombination mit PD-L1-Hemmern noch verstärkt. Erste klinische Daten legen nahe, dass das Regime bei manchen Patienten hochwirksam ist. Angesichts des Erfolgs von Durvalumab/Chemotherapie beim fortgeschrittenen SCLC und einer Durvalumab-Konsolidierung beim inoperablen NSCLC im Stadium III wird in der ADRIATIC-Studie letzterer Ansatz nun auch beim limitierten SCLC getestet: Patienten, die nach einer Chemoradiotherapie nicht progredient sind, erhalten eine Konsolidierung mit Placebo und Durvalumab oder eine Kombination aus Durvalumab und dem CTLA4-Antikörper Tremelimumab. Eine weitere neue Substanz ist Lurbinectedin, das die Transkription von Proteinen in Tumorzellen hemmt und ihren immunogenen Tod provoziert. Die Kombination mit CPI scheint synergistisch zu wirken, indem Lurbinectedin die Krebszellen gegenüber der Immuntherapie sensibilisiert. In der Phase-3-Studie IMFORTE wird Atezolizumab und Lurbinectedin bei limitiertem SCLC als Erhaltung nach Immunchemotherapie getestet.Quelle:
Paz-Ares L, Meadro C. IASLC 2021 Hot Topic Meeting: Small Cell Lung Cancer, Session „Clinical Trials in SCLC“
IASLC 2021 Hot Topic Meeting: Small Cell Lung Cancer
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).