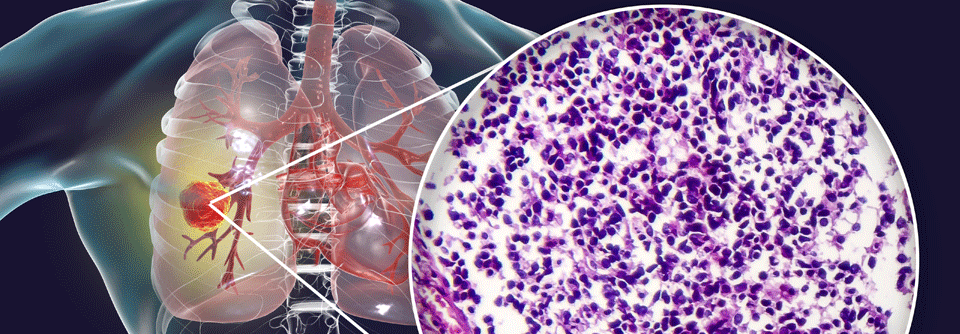
Checkpoint-Inhibition eröffnet neue Therapiedimensionen bei SCLC
 Die Immuntherapie schlägt beim Lungenkrebs Wurzeln.
© iStock/blueringmedia
Die Immuntherapie schlägt beim Lungenkrebs Wurzeln.
© iStock/blueringmedia
Eine aktualisierte Analyse der Studie IMpower133 nach median 22,9 Monaten bestätigt: Patienten mit fortgeschrittenem kleinzelligem Lungenkarzinom (SCLC) profititieren mit einem stabilen Überlebensvorteil von der Addition des Checkpoint-Inhibitors Atezolizumab zur Standard-Erstlinientherapie mit Carboplatin plus Etoposid. Nach 18 Monaten lebten unter dem Einfluss der Dreifachkombination noch 34 % der Teilnehmer im Vergleich zu 21 % unter der alleinigen Chemotherapie, so Professor Dr. Michael Thomas, Universitätsklinikum Heidelberg.
Ähnliche Überlebensdaten wurden laut dem Referenten auch in der CASPIAN-Studie mit Chemotherapie plus Durvalumab im Vergleich zur alleinigen Chemo erreicht (medianes Gesamtüberleben [OS] 13,0 Monate vs. 10,3 Monate; HR 0,73). Insgesamt sei der Überlebensvorteil durch Addition eines Checkpoint-Inhibitors in beiden Erstlinienstudien beim SCLC „statistisch signifikant, aber klinisch moderat“, gab Prof. Thomas zu bedenken.
Chemofreie Kombination auf dem Weg in die Erstlinie
Beim nicht-kleinzelligen Lungenkrebs (NSCLC) hat die Immunonkologie in der Erstlinienbehandlung als Monotherapie bei Patienten mit hoher PD-L1-Expression oder in Kombination zusammen mit Chemotherapie bereits einen festen Platz. Und regelmäßig kommen neue Studiendaten und -updates hinzu, die den Stellenwert von Checkpoint-Inhibitoren für Betroffene, die nicht für eine zielgerichtete Therapie infrage kommen, weiter untermauern, betonte der Experte.
So zeigen aktualisierte Daten der KEYNOTE-189-Studie, dass die Kombination von Pembrolizumab mit Chemotherapie in der Erstlinie, auch nach einer verlängerten Nachbeobachtungszeit von rund 19 Monaten, nahezu zu einer Verdopplung des medianen Gesamtüberlebens beim NSCLC ohne Plattenepithelhistologie im Vergleich zur Chemotherapie führte (22,0 Monate vs. 10,7 Monate; HR 0,56).
Weiterhin könnte demnächst eine „chemofreie“ Option aus den beiden Checkpoint-Inhibitoren Nivolumab und Ipilimumab das Therapieangebot für Patienten in der Erstlinie erweitern. In die sechsarmige Phase-3-Studie CheckMate 227 wurden Personen mit PD-L1-positiven (Expression ≥ 1 %) oder PD-L1-negativen Tumoren eingeschlossen.
Nach 1:1:1-Randomisierung erhielten die PD-L1-positiven Teilnehmer entweder Nivolumab mit niedrig dosiertem Ipilimumab, Nivolumab alleine oder eine Chemotherapie. PD-L1-negative Patienten erhielten Nivolumab mit niedrig dosiertem Ipilimumab, Nivolumab mit Chemo oder nur die Chemotherapie.
Auch PD-L1-negative Tumoren zeigen Ansprechen
Laut Prof. Thomas wurde bei den PD-L1-positiven Tumoren unter Nivolumab/Ipilimumab ein längeres OS als unter Chemotherapie erreicht (17,1 Monate vs. 14,9 Monate; HR 0,79; p = 0,007). Die Studie erreichte somit ihren primären Endpunkt. Darüber hinaus war die Kombination der Chemotherapie auch bei Patienten mit PD-L1-negativen Tumoren hinsichtlich des OS überlegen. Nivolumab/Ipilimumab könnte somit das therapeutische Erstlinien-Armamentarium beim NSCLC zukünftig noch weiter ausbauen, lautete das Fazit des Experten.
Quelle: DGHO-Jahrestagung 2019
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).