Prognostische Genexpressionspanel sind beim frühen Melanom bislang zu ungenau
 Das Rezidivrisiko wurde für fast jeden zehnten Melanom-Patienten zu hoch angesetzt.
© Alexander Raths – stock.adobe.com
Das Rezidivrisiko wurde für fast jeden zehnten Melanom-Patienten zu hoch angesetzt.
© Alexander Raths – stock.adobe.com
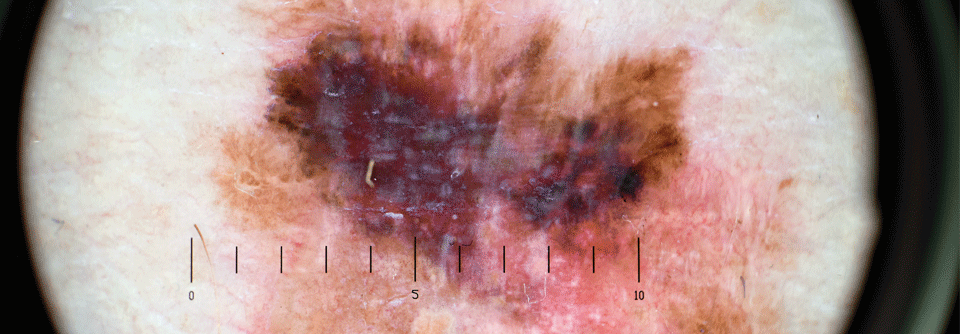
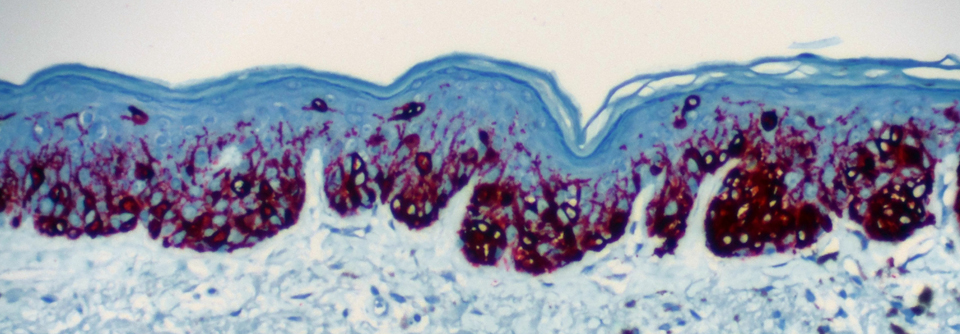
Die prognostische Relevanz von Genexpressionspanel (GEP) für das Melanom hängt vom Stadium ab, ihr klinischer Nutzen in Stadium I ist fraglich, berichten Dr. Michael A. Marchetti vom Memorial Sloan Kettering Center in New York und Kollegen.1 Im Rahmen ihrer systematischen Übersichtsarbeit und Metaanalyse identifizierten sie nur sieben Studien, in denen bei insgesamt 1450 Patienten mit lokal begrenztem Melanom GEP extern validiert wurden und die den Einschlusskriterien entsprachen.
Fünf waren mit dem 31 Gene umfassenden GEP DecisionDx-Melanoma (Panel 1) und zwei mit dem GEP MelaGenix (Panel 2) durchgeführt worden, der auf Veränderungen von acht prognostischen Genen beruht. Anhand der Genexpression im Tumorgewebe werden Melanome dabei in zwei Gruppen unterteilt, mit einer hohen bzw. niedrigen Wahrscheinlichkeit für eine Progression oder Metastasierung. Die Qualität der analysierten Studien bezeichnen die Wissenschaftler als mäßig. Die Zuverlässigkeit der GEP-Tests hing vom AJCC*-Stadium ab.
Ergebnisse Panel 1:
Mit dem ersten Panel wurden 61 von 623 Patienten im Stadium I falsch positiv eingestuft. Dadurch ergab sich für fast jeden zehnten Teilnehmer ein zu hohes Rezidivrisiko. Falsch negativ fielen 15 von 623 Ergebnissen aus, in diesen Fällen wurde die Wahrscheinlichkeit zu niedrig eingestuft. Sechs Erkrankte erhielten mit dem GEP die korrekte Vorhersage einer hohen Gefahr für Rezidive, 541 wurde richtigerweise eine niedrige Wahrscheinlichkeit prognostiziert. Für die 212 Teilnehmer mit einem Melanom im Stadium II ergab das erste Panel 78 falsch positive und 13 falsch negative Ergebnisse, schreiben die Autoren.
Prozentual gesehen hatte diese Variante beim Melanom im Stadium I Rezidive zu 29 %, im Stadium II zu 82 % prädiziert. Ein niedriges Risiko nannte der Test bei rezidivfreien Patienten in 90 % der Fälle mit einem Stadium-I-Melanom und in 44 % mit Stadium-II-Melanom korrekt.
Ergebnisse Panel 2:
Mit dem Panel 2 erhielten von 88 Patienten mit Stadium-I-Tumor 15 ein falsch negatives und 15 ein falsch positives Ergebnis. Von den 245 Teilnehmern mit Stadium-II-Tumor erfolgte die Einstufung bei 19 falsch negativ und bei 95 falsch positiv. Eine hohe Rezidivgefahr hatte das Panel 2 also für 32 % derer mit Stadium-I-Melanom, die ein Rezidiv entwickelten, vorausgesagt, beim Stadium-II-Melanom mit Rezidiv in 76 % der Fälle. Die Einschätzung einer geringen Rückfallwahrscheinlichkeit bewahrheitete sich mit dem Panel 2 bei 77 % derjenigen mit Stadium-I-Tumor und bei 43 % derjenigen mit Stadium-II-Tumor; sie blieben in Remission.
Aussagekraft bei Melanomen in Stadium I zu gering
Damit ist die prognostische Aussagekraft der Panel gerade für Patienten mit Melanomen in frühen Stadien, die niedergelassene Dermatologen häufig sehen, gering, schlussfolgern Dr. Marchetti und Kollegen. Die meisten der Betroffenen, die ein Rezidiv entwickelten, wurden fälschlicherweise als Niedrigrisikofälle eingestuft, sodass die Testergebnisse das übliche therapeutische Vorgehen nicht veränderten. Die Panel können die Mortalität auf Populationsebene folglich aber auch nicht reduzieren, schreiben die Forscher. Welchen Schaden die falsch positiven Resultate ausrichteten, welche zehnmal häufiger auftraten als korrekte positive Einstufungen, sei nicht bekannt.
Einen eingeschränkten klinischen Nutzen der aktuell verfügbaren Panel insbesondere bei Patienten mit einem kutanen Melanom des Stadiums I konstatierte auch eine US-amerikanische Konsensusgruppe um Professor Dr. Dr. Douglas Grossman vom Huntsman Cancer Institute der City of Hope in Salt Lake City.2 Zusammen mit Experten der nationalen Melanoma-Prevention Working Group (MPWG) hatte er nach einer Umfrage unter den Teilnehmern ebenfalls systematisch publizierte und auf Kongressen vorgestellte Studien zu Genexpressionspanels ausgewertet. Dabei wurde neben den beiden zuvor genannten Produkten auch ein CP(clinicopathologic)-GEP-Modell einbezogen, das klinisch-pathologische Parameter wie Alter und Tumordicke zusammen mit der Analyse der Expression von acht Genen bewertet, um die Wahrscheinlichkeit für Lymphknotenmetastasen vorherzusagen (Panel 3).
Zusätzlich Status der Wächterlymphknoten berücksichtigen
Die Arbeitsgruppe kritisiert, dass Panel 1 und 2 die für die Lokalrezidivgefahr relevanten klinischen und pathologischen Charakteristika nicht genügend in die Analyse integrieren. So könne die Genauigkeit des Panel 2 durch Kombination mit der Wächterlymphknotenbiopsie erheblich gesteigert werden: Die Sensitivität läge dann bei 67,7 % statt zuvor 38,7 %. Zudem kritisieren die Wissenschaftler, dass in den Studien zu wenige Patienten in den einzelnen Stadien einschlossen und diese zudem zu kurz beobachtet wurden.
Prof. Grossman und Kollegen betonen aber, dass sie sehr optimistisch sind, dass prognostische GEP in Zukunft die Risikostratifizierung von frühen kutanen Melanomen verbessern und die klinische Entscheidung unterstützen werden. Das sei umso wichtiger, als T1-Tumoren bis zu einem Drittel aller Todesfälle beim kutanen Melanom verursachen.
Da prospektive Studien teuer und aufwendig sind, empfiehlt die Arbeitsgruppe, zunächst einmal umfangreiche retrospektive Studien mit verschiedenen GEP-Testplattformen an gut dokumentiertem Material aus Tumorbiobanken durchzuführen. Möglicherweise werden zukünftige Plattformen mit weniger Gewebe auskommen und so die gleichzeitige Analyse mit verschiedenen GEP möglich machen, vermuten sie.
Wichtig wäre auch, die Bewertung durch ein internationales Konsortium einheitlich vorzunehmen, betonten Dr. Grossman und sein Team. Außerdem sei für den Einsatz in der klinischen Routine von Bedeutung, in den Studien neben Sensitivität, Spezifität und anderen statistischen Eckdaten auch patientenberichtete Endpunkte und Lebensqualitätsparameter zu erfassen.
Fazit:
Die Arbeitsgruppe erklärt, dass sich aktuell die kommerziell verfügbaren GEP nicht zur Unterstützung der Therapieentscheidung beim frühen malignen Melanom in der klinischen Routine eignen. Dafür müsste erst in prospektiven Studien der klinische Nutzen eindeutig belegt werden. Wenn dennoch Genexpressionspanels eingesetzt werden, ist es ihrer Ansicht nach geboten, in einem multidisziplinären Team die Limitationen der Varianten zu diskutieren bzw. die Unsicherheit der Testergebnisse mit dem Patienten zu besprechen.
* American Joint Committee on Cancer
1. Marchetti MA et al. JAMA Dermatol 2020; DOI: 10.1001/jamadermatol.2020.1731
2. Grossman D et al. A.a.O; DOI: 10.1001/jamadermatol.2020.1729
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).