Glioblastom Erste behandelte Patient:innen erzielten signifikante Remissionen
 Eine neue CAR-T-Zell-Strategie weckt Hoffnung in der Therapie des Glioblastoms.
© MQ-Illustrations – stock.adobe.com
Eine neue CAR-T-Zell-Strategie weckt Hoffnung in der Therapie des Glioblastoms.
© MQ-Illustrations – stock.adobe.com
Der Erfolg von CAR-T-Zellen bei hämatologischen Erkrankungen konnte bisher in der Gruppe der soliden Tumoren nicht wiederholt werden. Denn deren genetische Wandlungsfähigkeit und Heterogenität führen sehr häufig zum Verlust des anvisierten Antigens und fördern immunologische Escape-Mechanismen. Das Team um Prof. Dr. Dr. Bryan D. Choi, Massachusetts General Hospital und Harvard University, Boston, scheint nun eine neue Strategie gefunden zu haben, die bei Erkrankten mit Glioblastom wirkt.
Einige dieser Tumoren exprimieren eine Variante des Rezeptors für den epidermalen Wachstumsfaktor (EGFRvIII), die als tumorspezifisches Antigen anzusehen ist und von entsprechend konstruierten CAR-T-Zellen angegriffen wird. Der Krebs verliert aber unter dem Selektionsdruck dieser Behandlung das Antigen sehr schnell und spricht radiologisch nicht an; die Rezidive exprimieren den EGFR-Wildtyp und sind außerdem mit suppressiven regulatorischen T-Zellen infiltriert.
Die Mediziner:innen entwickelten daher eine autologe CAR-T-Zell-Variante, die nicht nur den gegen EGFRvIII gerichteten Antigenrezeptor exprimiert, sondern darüber hinaus Antikörper-Moleküle – TEAMs* – ausschüttet. Diese binden wildtypisches EGFR und können darüber hinaus regulatorische T-Zellen zum Tumor leiten. EGFR wird im Gehirn außer von Glioblastomen nicht exprimiert.
Lokale und gezielte Therapie im ZNS
CAR-T-Zellen mit daran gebundenen TEAMs wurden im peripheren Blut nur in verschwindend niedrigen Konzentrationen nachgewiesen. Laut den Autor:innen ist das ein weiterer Hinweis darauf, dass die CARv3-TEAM-Plattform eine sichere, lokale und gezielte Behandlung des wildtypischen EGFR im ZNS ermöglicht.
Keine schweren Toxizitäten
Die CAR-T-Zellen werden über ein bei der Operation des Tumors eingesetztes Ommaya-Reservoir in den Liquorraum appliziert. Nach vielversprechenden Tierversuchen starteten die Forschenden eine Phase-1-Studie, über deren erste drei Patient:innen sie nun berichteten.
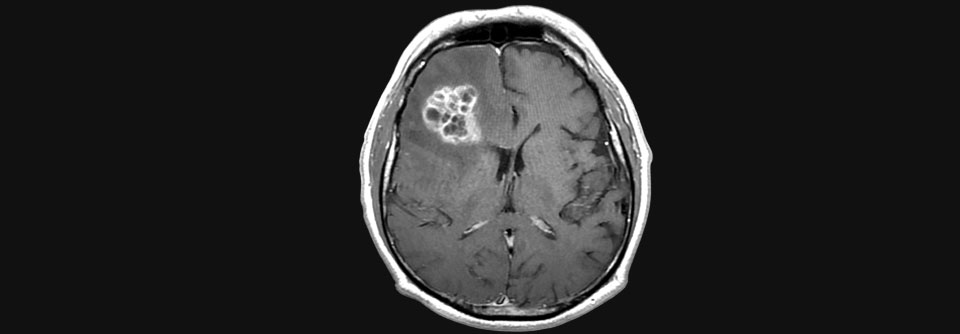
Keine Es traten keine schweren Nebenwirkungen (> Grad 3) oder dosislimitierenden Toxizitäten auf. Vor allem aber erzielten alle drei Erkrankten binnen Tagen eine dramatische radiologisch dokumentierte Remission, die allerdings in zwei Fällen nur wenige Wochen andauerte. Bei einem Teilnehmenden war die Wirkung trotz fehlender EGFRvIII-Expression zu beobachten – ein Hinweis darauf, dass die Therapie Tumorzellen mit Wildtyp-EGFR angreift.
Die aufgetretenen Rezidive sind vermutlich auf die limitierte Persistenz der CAR-T-Zellen zurückzuführen. Um diese zu verlängern, diskutieren die Autor:innen weitere Maßnahmen wie eine Präkonditionierung mit Chemotherapie und zusätzliche Infusionen der therapeutischen Zellen.
* T-cell–engaging antibody molecules
Quelle:
Choi BD et al. N Engl J Med 2024; 390: 1290-1298; DOI: 10.1056/NEJMoa2314390