Parkinson: Tiefe Hirnstimulation liefert wichtige Informationen
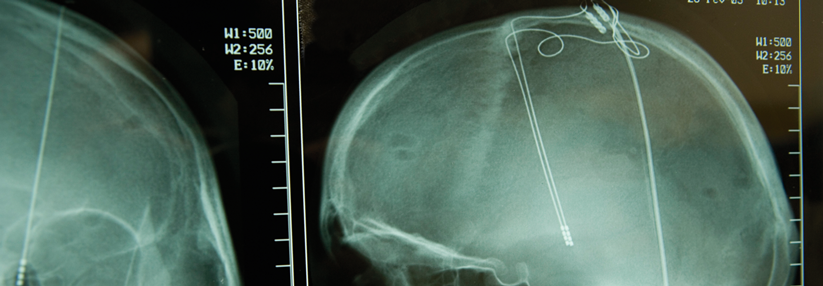 Die THS erfolgte bei diesem Patienten wegen einer Dystonie.
© RFBSIP – stock.adobe.com
Die THS erfolgte bei diesem Patienten wegen einer Dystonie.
© RFBSIP – stock.adobe.com
„Wir haben in vielen Studien zeigen können, dass es eine Klasse-I-Evidenz für die tiefe Hirnstimulation gibt“, betonte Professor Dr. Andrea Kühn, Charité – Universitätsmedizin Berlin. So ist die Wirkfluktuation beim M. Parkinson unter der THS deutlich geringer als bei medikamentöser Therapie und die Lebensqualität erheblich gesteigert.1 Ähnliche Studien gibt es für den essenziellen Tremor und die primäre Dystonie.2,3
Noch viele ungelöste Probleme bei der THS
Der Schönheitsfehler: Die Therapie funktioniert bisher nach dem Prinzip Gießkanne. Stimuliert wird mit 130 Hz über 24 Stunden am Tag, ohne Frequenz und Dauer auf den Patienten individuell abzustimmen. Auch andere Probleme sind noch nicht gelöst, etwa die optimale Zielpunktfindung, Nebenwirkungen wie Dysarthrie und Dyskinesien, die durch Synergismus von THS und Medikation entstehen können, oder unerwünschte Langzeiteffekte der Stimulation in Form von Bradykinese und Ataxie.
Die THS zeichnet sich durch multiple Effekte aus, die sich zu unterschiedlichen Zeitpunkten manifestieren – manche binnen Millisekunden auf zellulärer Ebene, andere langfristig in ganzen Netzwerken bis hin zu den Basalganglien, erläuterte Prof. Kühn. Auch zum Verständnis neuromotorischer Erkrankungen hat das Verfahren viel beigetragen. Die Ableitung lokaler Feldpotenziale über die Stimulationselektroden erlaubt im Zusammenspiel mit der Elektro- oder Magnetenzephalographie, die funktionellen Interaktionen innerhalb der neuronalen Netzwerke im einzelnen Patienten darzustellen. Ergänzend lassen sich die Fasertrakte, die durch die THS moduliert werden, darstellen.
Mit diesen Methoden kann man die THS den individuellen Bedürfnissen des Patienten wesentlich besser anpassen, als dies bisher möglich war. Als Feedbacksignal für die adaptive Stimulation beim M. Parkinson hat Prof. Kühns Arbeitsgruppe die Aktivität im Betafrequenzband um 20 Hz identifiziert.4 Diese korreliert eng mit der klinischen Symptomatik. Bei Dystonien liegt die Aktivität vor allem im niederfrequenten Spektrum unter 10 Hz, auch hier korrelieren Stärke der Aktivität und Symptomatik.
Beim einzelnen Patienten lassen sich On-Off-Fluktuationen am EEG ablesen. Den neuronalen Aktivitätsmustern kann man überdies bestimmte Symptome zuordnen: Betaaktivität ist mit Akinese und Rigor assoziiert, Thetaaktivität mit Dys- und Hyperkinesen, Gammaaktivität mit Peak-Dose-Dyskinesien. „Durch die Stimulation können wir diese neuronalen Muster verändern“, berichtete die Neurologin. Die Suppression pathologischer Betaaktivität durch Stimulation geht mit einer verbesserten Motorik einher.
Kehren die Symptome kurz nach Ende der Stimulation wieder, nimmt auch die Betaaktivität wieder zu. Vorstellbar ist also ein System, das diesen Biomarker registriert und die Stimulation prozessorgesteuert anpasst.
Im experimentellen Setting konnte bereits gezeigt werden, dass dies funktioniert – bis zur breiten klinischen Anwendung dürfte es aber noch dauern. Die Hoffnung geht dahin, dass sich durch adaptive Stimulation Nebenwirkungen der Therapie vermeiden lassen. Seit Januar steht ein implantierbarer Pulsgenerator zur Verfügung, der eine chronische Ableitung der neuronalen Aktivität ermöglicht. Für 2021 ist die erste klinische Studie zur adaptiven THS bei M. Parkinson geplant, primärer Endpunkt: die ON-Zeit ohne Dyskinesien.
Das zu stimulierende Netzwerk charakterisieren
Als Technik der Zukunft betrachtet Prof. Kühn die konnektivitätsbasierte THS. Sie stützt sich darauf, dass die Stimulation eben nicht nur lokale Effekte ausübt, sondern auf neuronale Netzwerke wirkt. Dabei ist die Kombination mit der Bildgebung entscheidend: „Wir müssen die Elektroden lokalisieren, die optimalen Stimulationsparameter einstellen und das stimulierte Volumen bestimmen, um dann im zweiten Schritt das Netzwerk zu charakterisieren, das stimuliert wird“, so die Referentin.
Prinzipiell kommen dafür zwei MRT-Techniken infrage. Um die funktionelle Konnektivität zu bestimmen, wird das Ruhe-MRT mit dem nach der Stimulation abgeglichen. So lassen sich die Areale auffinden, die auf die THS ansprechen. Für die strukturelle Konnektivität können die aktivierten Fasertrakte per Traktographie im diffusionsgewichteten MRT nachverfolgt werden. Mit beiden Methoden kann man vorhersagen, wie ein Patient auf die Stimulation ansprechen wird.5 „Das lässt sich in Zukunft nutzen, um für jeden einzelnen Patienten die optimale Netzwerkaktivierung zu bestimmen und so die Feinjustierung von Stimulationsort und -parametern vorzunehmen“, meinte Prof. Kühn.
Quellen:
1. Schuepbach WMM et al. N Engl J Med 2013; 368: 610-622; DOI: 10.1056/NEJMoa1205158
2. Limousin P et al. J Neurol Neurosurg Psychiatry 1999; 66: 289-296; DOI: 10.1136/jnnp.66.3.289
3. Volkmann J et al. Lancet Neurol 2012; 11: 1029-1038; DOI: 10.1016/S1474-4422(12)70257-0
4. Neumann WJ et al. Brain 2018; 141: 2655-2669; DOI: 10.1093/brain/awy206
5. Horn A et al. Annals of Neurology 2017; 82: 67-78; DOI: 10.1002/ana.24974
Kongressbericht: 93. Kongress der Deutschen Gesellschaft für Neurologie (Online-Veranstaltung)