Biomarker gesucht Beim Parkinson ist einiges im Fluss
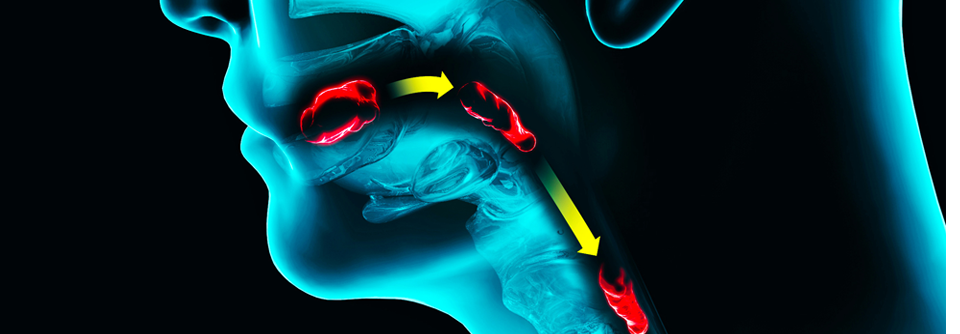
 α-Synuclein lässt sich u.a. in Magenmukosa, Speicheldrüsen, Hautbiopsien und Liquor nachweisen.
© Lars Neumann – stock.adobe.com
α-Synuclein lässt sich u.a. in Magenmukosa, Speicheldrüsen, Hautbiopsien und Liquor nachweisen.
© Lars Neumann – stock.adobe.com
Der natürliche Kandidat für einen Parkinson-Biomarker ist natürlich α-Synuclein, das sich u. a. in Magenmukosa, Speicheldrüsen, Hautbiopsien und Liquor nachweisen lässt. Für Bluttests dürfte es sich weniger eignen, weil Erythrozyten große Mengen davon enthalten und Spiegelveränderungen eher mit der Hämatopoese korrelieren als mit pathologischen Prozessen im Gehirn. Zurzeit befinden sich Assays in Entwicklung, die α-Synuclein-haltige neuronale Exosomen im Serum nachweisen – das könnte eine Alternative werden, meinte Professor Dr. Per Svenningsson, Karolinska Institut Stockholm.
Phosphoryliertes α-Synuclein im Liquor nachweisen
Jeder der anderen erwähnten Nachweisorte hat Vor- und Nachteile. Hautbiopsien lassen sich wenig invasiv gewinnen und erreichen eine gute Spezifität. Was fehlt ist die Standardisierung der Entnahme. Liquor bildet neurochemische Prozesse im ZNS gut ab, die Materialgewinnung erfolgt jedoch invasiv und birgt das Risiko der Kontamination mit Blut. Die Biopsie aus den Speicheldrüsen gelingt nicht immer treffsicher, im gewonnenen Gewebe lässt sich aber möglicherweise eine Progression dokumentieren. Treffsicherheit ist bei der ebenfalls invasiven Magenschleimhautbiopsie kein Problem, ihre mangelnde Spezifität sehr wohl.
Die Liquordiagnostik hat Fortschritte gemacht, seit klar ist, dass monomeres α-Synuclein zu inkonsistente Ergebnisse liefert, um klinisch genutzt zu werden. Besser geeignet scheint das phosphorylierte α-Synuclein (PS-129) zu sein. Bei Parkinsonpatienten sind die Liquorspiegel deutlich erhöht, bei Alzheimerkranken liegen sie in der gleichen Größenordnung wie bei Gesunden.
Erniedrigte Spiegel finden sich bei Multisystematrophie (MSA) und progressiver supranukleärer Paralyse (PSP). „Das ist vielversprechend, aber die Assays müssen noch besser werden“, urteilte Prof. Svenningsson. Ein Problem liegt darin, dass α-Synuclein zu einem erheblichen Teil in Lipoproteinpartikeln transportiert wird. ApoE beispielsweise absorbiert bis zu 40 % des α-Synucleins, sodass die Messwerte zu niedrig ausfallen.
Die in der Diagnostik von Prionenerkrankungen eingesetzte Real-Time Quaking-Induced Conversion (RT-QuIC) könnte auch für die Parkinson-Biomarkerdiagnostik hilfreich sein. Verkürzt gesagt weist sie die pathologische Aggregationsneigung fehlgefalteter α-Synuclein-Proteine nach, indem sie den Aggregationsprozess anstößt und zu einem exponentiellen Zuwachs von Fibrillen führt. Damit lassen sich auch kleinste Mengen fehlgefalteter Proteine nachweisen. Sensitivität und Spezifität der Methode sind sehr gut. In einer kleinen Testreihe waren 19 von 20 Parkinsonpatienten positiv, aber keine der gesunden Kontrollen. Die Ergebnisse sind inzwischen mehrfach bestätigt und belegen eine gute Trennschärfe etwa gegen die MSA.
Auf der Suche nach Biomarkern, die anzeigen, welche Parkinsonpatienten demenzgefährdet sind, hat die Forschung zurzeit Aß1-42 und Neurofilament(NFL)-Leichtketten im Visier. Vor allem niedrige Spiegel von Aß1-42 zeigen ein erhöhtes Demenzrisiko an, berichtete Prof. Svenningsson. NFL können genutzt werden, um die klassische Parkinsonkrankheit von atypischen Formen zu diskriminieren, bei denen die Messwerte noch deutlich höher ausfallen. Allerdings sind Neurofilament-Leichtketten auch bei anderen neurodegnerativen Erkrankungen, etwa der Multiplen Sklerose, erhöht. Wie eine klare Abgrenzung erfolgen kann, bleibt zu untersuchen. Positiv immerhin: NFL-Blutspiegel korrelieren linear mit denen im Liquor, was die Diagnostik vereinfachen würde.
Kongressbericht: European Academy for Neurology EAN Congress 2021 – Virtual Meeting