Blasentumor: Was tun, wenn Cisplatin keine Option ist?
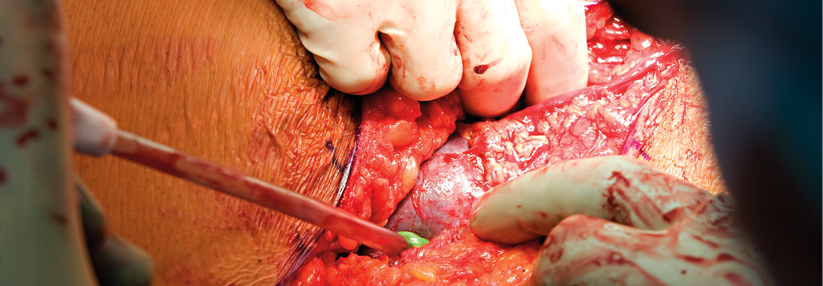
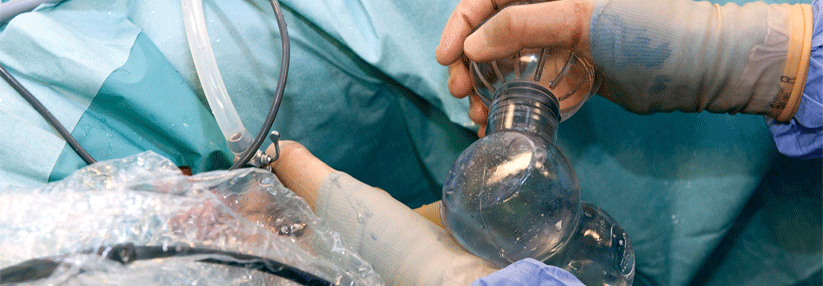
 Patienten mit Urothelkarzinom eignen sich nicht für Cisplatin bei: Status im ECOG von mind. 2 oder Karnofsky von mind. 70 %, Hörverlust in der Audiometrie, peripherer Neuropathie und/oder Herzinsuffizienz ab NYHA IV.
© Science Photo Library/Steger, Volker
Patienten mit Urothelkarzinom eignen sich nicht für Cisplatin bei: Status im ECOG von mind. 2 oder Karnofsky von mind. 70 %, Hörverlust in der Audiometrie, peripherer Neuropathie und/oder Herzinsuffizienz ab NYHA IV.
© Science Photo Library/Steger, Volker
Enfortumab-Vedotin richtet sich gegen Nectin4. Das Antikörper-Wirkstoff-Konjugat bewirkt hohe Ansprechraten bei Patienten mit lokal fortgeschrittenem oder metastasiertem Blasenkarzinom, die im fortgeschrittenen Setting bereits mit Cisplatin und einem Checkpoint-Inhibitor vorbehandelt wurden. Deshalb hat die FDA es in dieser Indikation zugelassen.1,2
Studie EV-301
Erste Daten einer randomisierten Phase-3-Studie stellte Professor Dr. Thomas Powles, Barts Cancer Centre, Queen Mary University of London, nun vor.3 In der unverblindeten Studie EV-301 vergleichen Forscher um den Onkologen Enfortumab-Vedotin mit einer Standard-Chemotherapie bei Platin-vorbehandelten Patienten. Ihr Tumor wurde nach der Behandlung mit einem PD1/-L1-Antikörper progredient. Primärer Endpunkt bildete das Gesamtüberleben (OS). Die Teilnehmer waren im Schnitt 68 Jahre alt.
Gesamtüberleben stieg um vier Monate
608 Patienten erhielten in einer 1:1-Randomisierung entweder Enfortumab-Vedotin in einer Dosierung von 1,25 mg/kgKG an Tag 1, 8 und 15 jedes Zyklus oder eine vorab ausgewählte Chemotherapie mit Docetaxel, Paclitaxel oder Vinflunine. Prof. Powles bewertete die Daten als „beeindruckend“. Nach einer medianen Beobachtungszeit von 11,1 Monaten verlängerte sich das mediane OS signifikant von 8,97 Monaten in der Kontrolle auf 12,88 Monate im Prüfarm (Hazard Ratio [HR] 0,70; 95%-KI 0,56–0,89; p = 0,00142). Insgesamt starben unter Enfortumab-Vedotin bislang 134 Patienten, unter Chemotherapie 167. „Als erste Substanz zeigt Enfortumab-Vedotin einen Überlebensvorteil bei vorbehandelten Patienten mit fortgeschrittenem Blasenkarzinom“, kommentierte der Experte die Ergebnisse.
Auch das progressionsfreie Überleben (PFS) fiel mit 5,55 Monaten im Vergleich zu 3,71 Monaten signifikant länger aus (HR 0,62; p < 0,00001). Die objektive Ansprechrate (ORR) war mit 40,6 % versus 17,9 % mehr als doppelt so hoch. Dabei traten im ersten Arm 35,8 % partielle und 4,9 % Komplettremissionen auf, in der Chemotherapiegruppe nur 15,2 % und 2,7 % (p < 0,001).
Das Sicherheitsprofil bezeichnete Prof. Powles als handhabbar. Schwere Nebenwirkungen traten in beiden Gruppen mit 22,6 % und 23,4 % ähnlich häufig auf. Jeder zweite Patient entwickelte ein Ereignis von mindestens Grad 3. Toxizitäten, die zu einem Therapieabbruch führten, traten bei 14 % bzw. 11 % der Teilnehmer auf, solche, die im Tod mündeten, bei 2,4 % bzw. 1 %.
Drei typische Toxizitäten unter Antikörper-Wirkstoff-Konjugat
Als typische Nebenwirkung unter Enfortumab-Vedotin gelten Hautreaktionen. So wiesen 44 % der Patienten einen Ausschlag auf, bei 15 % erreichte er einen Schweregrad von mindestens 3. An peripheren Neuropathien litten 46 % der Patienten (5 % Grad ≥ 3). Auch Hyperglykämien gehören zu den typischen Nebenwirkungen des Antikörper-Wirkstoff-Konjugats. In dieser Studie entwickelten sie 6 % der Patienten, 4 % davon erreichten mindestens Schweregrad 3. Unter der Chemotherapie kam es hingegen häufiger zu Neutrophilie, Leukopenie und febriler Neutropenie.
Insgesamt wertete Prof. Powles die Daten als vielversprechend: „Mit Blick auf die eingeschränkten Optionen, die Patienten in dieser Situation noch haben, sind diese Studienergebnisse ein großer Schritt in die richtige Richtung.“
Atezolizumab bei erhöhter PD-L1-Expression
- Arm A: Atezolizumab plus Platin plus Gemcitabin
- Arm B: alleinige Immuntherapie
- Arm C: Placebo plus Platin plus Gemcitabin
Quellen:
1. Galsky MD et al. Lancet 2020; 395: 1547-1557; DOI: 10.1016/S0140-6736(20)30230-0
2. Galsky MD et al. 2021 Genitourinary Cancers Symp.; Poster Highlight Session; Abstract 434
Studie EV-201
Quellen:
1. Rosenberg J et al. J Clin Oncol 2020; 38: 1041-1049; DOI: 10.1200/JCO.19.02044
2. Chang E et al. Clin Cancer Res 2021; 27: 922-927; DOI: 10.1158/1078-0432.CCR-20-2275
3. Powles T et al. 2021 Genitourinary Cancers Symposium (virtual); Oral Abstract Session; Abstract 393
4. Balar AV et al. A.a.O; Abstract 394
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).