Immuncheckpoint-Blockade beim fortgeschrittenen Urothelkarzinom
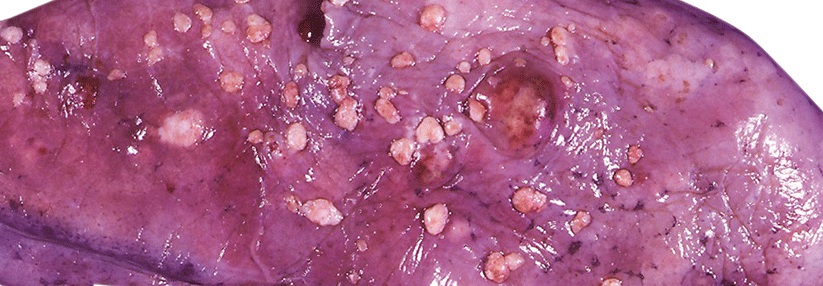
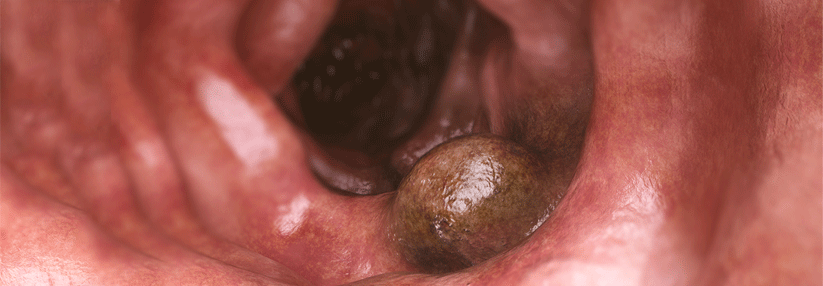
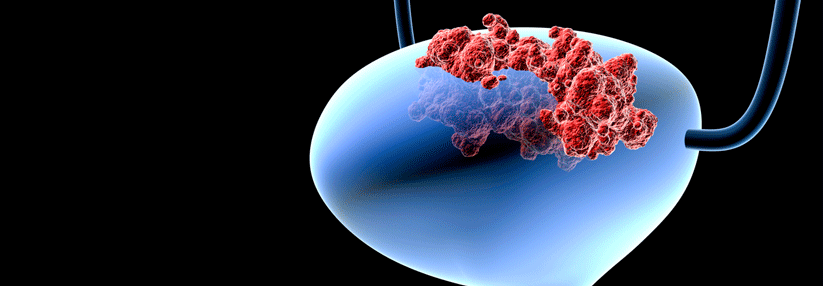
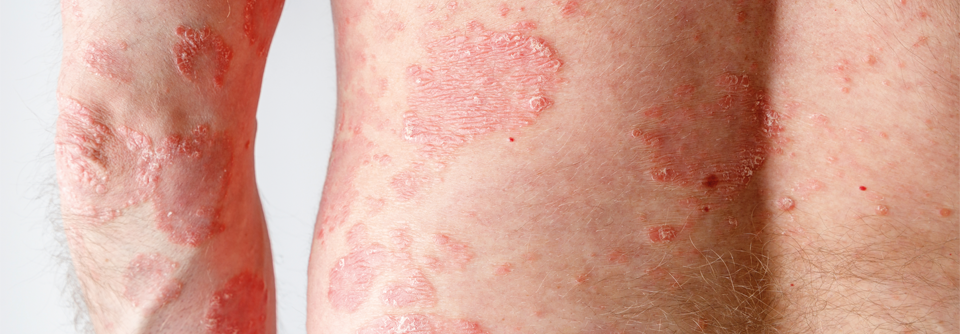
 Fortgeschrittene Urothelkarzinome haben eine sehr schlechte Prognose.
© Science Photo Library/ Dr. Marazzi P.
Fortgeschrittene Urothelkarzinome haben eine sehr schlechte Prognose.
© Science Photo Library/ Dr. Marazzi P.
Urothelkarzinome gehören, sobald sie sich in einem fortgeschrittenen Stadium befinden, zu den am schwierigsten zu behandelnden malignen Tumoren. Selbst mit platinbasierten Kombinationstherapien liegen die medianen Überlebenszeiten lediglich knapp über einem Jahr. In der Zweitlinie überleben die Patienten nur noch etwa halb so lang. Zudem gibt es für die Zweitlinie bei dieser Indikation bisher keinen international akzeptierten Standard.
Jedoch gehören diese Tumoren zu denjenigen mit den höchsten Mutationsraten und sollten deshalb ausgesprochen immunogen sein. Da Immunreaktionen gegen maligne Zellen häufig durch Immuncheckpoint-Mechanismen unterdrückt werden, laufen aktuell vielfältige Bemühungen, durch Hemmung dieser Checkpoints eine stärkere Anti-Tumor-Wirksamkeit zu erreichen.
Für Pembrolizumab legten Dr. Joaquin Bellmunt, Dana Farber Cancer Institut, Boston, und Kollegen nun die ersten Daten der Phase-III-Studie KEYNOTE-045 vor2: Darin wurde der Antikörper (in einer Dosierung von 200 mg alle drei Wochen) bei 542 Patienten mit fortgeschrittenem Urothelkarzinom, die nach einer platinhaltigen Therapie progredient waren, randomisiert gegen eine Chemotherapie nach Wahl der behandelnden Ärzte (Paclitaxel, Docetaxel oder Vinflunin) getestet. Koprimäre Endpunkte waren Gesamt- und progressionsfreies Überleben bei allen Patienten sowie bei denjenigen, die auf mindestens 10 % der Tumor- bzw. der infiltrierenden Immunzellen den PD-1-Liganden PD-L1 exprimierten.
Beim progressionsfreien Überleben hingegen fand sich kein signifikanter Unterschied zwischen den Armen (HR 0,98 insgesamt; p = 0,42 bzw. HR 0,89 bei den PD-L1-Exprimierern; p = 0,24). Der Checkpoint-Inhibitor war besser verträglich als die Chemotherapie mit Nebenwirkungsraten von insgesamt 60,9 versus 90,2 % und von 15,0 versus 49,4 % (unerwünschte Wirkungen vom Grad ≥ 3).
Jedoch gehören diese Tumoren zu denjenigen mit den höchsten Mutationsraten und sollten deshalb ausgesprochen immunogen sein. Da Immunreaktionen gegen maligne Zellen häufig durch Immuncheckpoint-Mechanismen unterdrückt werden, laufen aktuell vielfältige Bemühungen, durch Hemmung dieser Checkpoints eine stärkere Anti-Tumor-Wirksamkeit zu erreichen.
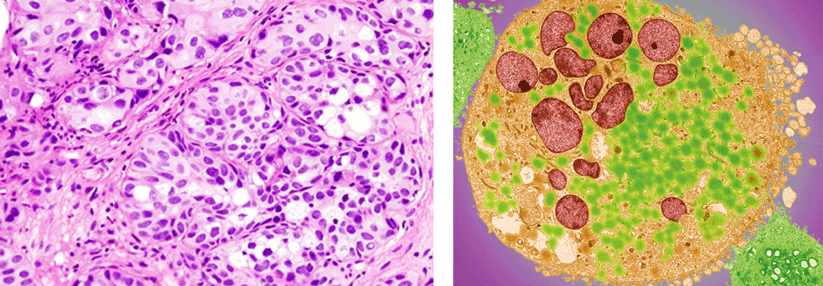
Urothelkarzinome gehören zu den Tumoren mit den höchsten Mutationsraten
Zwei bereits für andere Indikationen zugelassene Antikörper gegen das Checkpoint-Protein PD1 – Pembrolizumab und Nivolumab – haben in frühen Studien auch Aktivität gegen Blasentumoren gezeigt. Darüber hinaus war mit Atezolizumab ein Anti-PD-L1-Inhibitor in einer bereits 2016 vorgestellten Phase-II-Studie bei Patienten mit fortgeschrittenem bzw. metastasiertem Urothelkarzinom wirksam.1Für Pembrolizumab legten Dr. Joaquin Bellmunt, Dana Farber Cancer Institut, Boston, und Kollegen nun die ersten Daten der Phase-III-Studie KEYNOTE-045 vor2: Darin wurde der Antikörper (in einer Dosierung von 200 mg alle drei Wochen) bei 542 Patienten mit fortgeschrittenem Urothelkarzinom, die nach einer platinhaltigen Therapie progredient waren, randomisiert gegen eine Chemotherapie nach Wahl der behandelnden Ärzte (Paclitaxel, Docetaxel oder Vinflunin) getestet. Koprimäre Endpunkte waren Gesamt- und progressionsfreies Überleben bei allen Patienten sowie bei denjenigen, die auf mindestens 10 % der Tumor- bzw. der infiltrierenden Immunzellen den PD-1-Liganden PD-L1 exprimierten.
Unterschiedliche Ergebnisse je nach Grad der PD-L1-Expression der Tumoren
In der Gesamtpopulation war das Gesamtüberleben im Pembrolizumab-Arm signifikant um fast drei Monate von median 7,4 Monaten unter der Chemotherapie auf 10,3 Monate verlängert (Hazard Ratio 0,73; p = 0,002). Interessanterweise waren die Werte bei den Patienten mit PD-L1-Expression ≥ 10 % insgesamt niedriger, aber der Vorteil durch den PD-1-Antikörper war ähnlich groß mit median 8,0 versus 5,2 Monaten (HR 0,57; p = 0,005).Beim progressionsfreien Überleben hingegen fand sich kein signifikanter Unterschied zwischen den Armen (HR 0,98 insgesamt; p = 0,42 bzw. HR 0,89 bei den PD-L1-Exprimierern; p = 0,24). Der Checkpoint-Inhibitor war besser verträglich als die Chemotherapie mit Nebenwirkungsraten von insgesamt 60,9 versus 90,2 % und von 15,0 versus 49,4 % (unerwünschte Wirkungen vom Grad ≥ 3).
Zulassungen werden erwartet
Beide Antikörper zeigen damit bei diesen schwierig zu behandelnden Patienten Wirksamkeit, wobei die Datenlage zum PD-1-Inhibitor Pembrolizumab aufgrund der Phase-III-Natur der Studie besser gesichert ist. Vermutlich sind auf dem Gebiet der Immuntherapie beim Urothelkarzinom demnächst einige dringend erwünschte Neuzulassungen zu erwarten. So wurde der PD-L1-Antikörper Atezolizumab in den USA bereits im Mai 2016 zur Therapie fortgeschrittener Urothelkarzinome zugelassen. Der Antrag auf eine EU-Zulassung wurde bereits eingereicht.
Der zweite PD-1-Antikörper, Nivolumab, wurde nach vorausgegangenen positiven Phase-I/II-Daten bei Patienten mit vorbehandeltem Urothelkarzinom in der einarmigen multizentrischen Phase-II-Studie CheckMate-275 getestet.3 Wie Professor Dr. Padmanee Sharma, MD Anderson Cancer Center, Houston, und Kollegen berichten, erhielten in 63 Zentren in elf Ländern insgesamt 270 Patienten 3 mg/kg Nivolumab alle zwei Wochen.
Primärer Endpunkt war hier die objektive Gesamtansprechrate insgesamt und bei Patienten mit einer PD-L1-Expression von ≥ 5 bzw. ≥ 1 %. Nach median sieben Monaten Nachbeobachtungsdauer lag die Rate insgesamt bei 19,6 % und bei 28,4 % bzw. 23,8 % in den beiden Subgruppen mit ≥ 5 bzw. ≥ 1 % PD-L1-Expression. Die Verträglichkeit war auch hier gut: Grad-3/4-Nebenwirkungen wurden bei 18 % der Patienten registriert, am häufigsten Fatigue und Diarrhö vom Grad 3, die bei jeweils fünf Patienten auftraten. Allerdings wurden auch drei behandlungsbedingte Todesfälle beobachtet (durch Pneumonitis, akutes Atemversagen und Herz-Kreislauf-Versagen).
Primärer Endpunkt war hier die objektive Gesamtansprechrate insgesamt und bei Patienten mit einer PD-L1-Expression von ≥ 5 bzw. ≥ 1 %. Nach median sieben Monaten Nachbeobachtungsdauer lag die Rate insgesamt bei 19,6 % und bei 28,4 % bzw. 23,8 % in den beiden Subgruppen mit ≥ 5 bzw. ≥ 1 % PD-L1-Expression. Die Verträglichkeit war auch hier gut: Grad-3/4-Nebenwirkungen wurden bei 18 % der Patienten registriert, am häufigsten Fatigue und Diarrhö vom Grad 3, die bei jeweils fünf Patienten auftraten. Allerdings wurden auch drei behandlungsbedingte Todesfälle beobachtet (durch Pneumonitis, akutes Atemversagen und Herz-Kreislauf-Versagen).
Quelle:
1. Rosenberg JE et al. Lancet 2016; 387: 1909–1920
2. Bellmunt J et al. N Engl J Med 2017, Feb 17 [prepub ahead of print, DOI 10.1056/NEJMoa1613683]
3. Sharma P et al. Lancet Oncol 2017; 18: 312–322
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).