DLBCL: Lenalidomid-Erhaltung bremst Progression
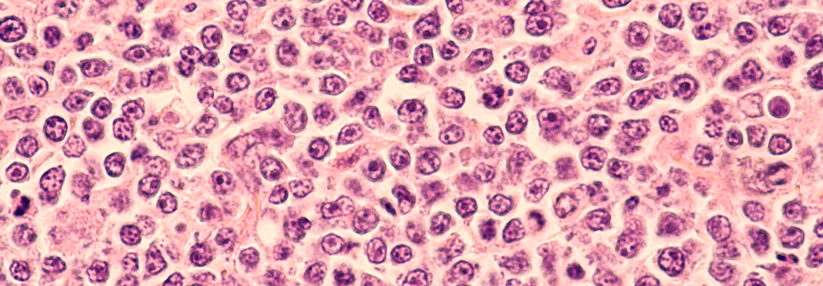
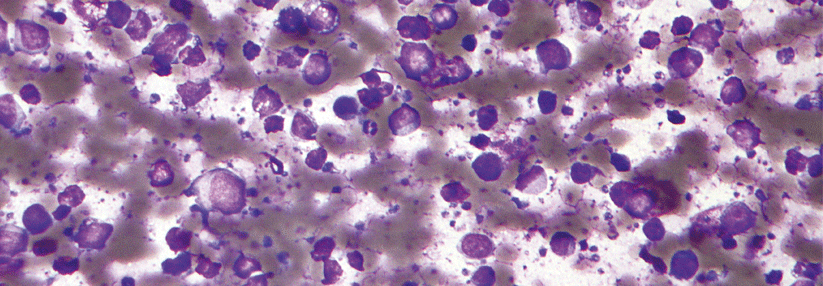 Die mikroskopische Aufnahme zeigt angefärbte DLBCL-Zellen in einem Lymphknoten.
© Wikimedia/Nephron
Die mikroskopische Aufnahme zeigt angefärbte DLBCL-Zellen in einem Lymphknoten.
© Wikimedia/Nephron
Die Drei-Jahres-Raten für progressionsfreies und Gesamtüberleben unter der Standardtherapie mit Rituximab und einer CHOP-Chemotherapie liegen zwischen 60 und 70 % – mit einer deutlich schlechteren Prognose für den Subtyp des activated B-cell-like (ABC) gegenüber dem Germinal Center B-cell-like (GBC) DLBCL.
Die Intensivierung der Therapie – beispielsweise auch eine Erhaltungstherapie mit Rituximab – hat bisher keine Steigerung der Heilungsraten gebracht, sodass weltweit über die Einführung neuer Substanzen in das Standardschema nachgedacht wird. So hat der Immunmodulator Lenalidomid sich alleine oder in Kombination mit Rituximab in der rezidivierten Situation – die bislang mit einer schlechten Prognose assoziiert ist – als wirksam erwiesen.
Lenalidomid besser zur Induktion oder Erhaltung?
Bezüglich der Primärtherapie ist die Frage bisher, ob man Lenalidomid direkt zur Induktionstherapie oder danach als Erhaltungstherapie gibt. Die französische Lymphom-Studiengruppe LYSA hat in Zusammenarbeit mit einigen Gruppen in anderen Ländern letzteres in einer Phase-III-Studie getestet. In dieser bekamen 650 Patienten mit DLBCL, die mit sechs bis acht Zyklen R-CHOP mindestens eine partielle Remission erzielt hatten, randomisiert zwei Jahre lang entweder Lenalidomid (25 mg/d an 21 Tagen eines vierwöchigen Zyklus) oder Placebo. Primärer Endpunkt war das progressionsfreie Überleben. Nach 39 Monaten Nachbeobachtung war in der Lenalidomid-Gruppe beim progressionsfreien Überleben der Medianwert noch nicht erreicht, während er im Placeboarm 58,9 Monate betrug (Hazard Ratio 0,708; p = 0,01). Dieser Vorteil der Erhaltungstherapie war mehr oder weniger in allen untersuchten Subgruppen zu sehen – unabhängig von Geschlecht, altersadjustiertem International Prognostic Index, Alter, Ansprechen auf die Induktionstherapie oder PET-Status nach der Induktion.
Enttäuschende Ergebnisse zum Gesamtüberleben
Mit einer längeren Nachbeobachtungszeit von median 52 Monaten gibt es auch Daten zum Gesamt-überleben, aber hier zeigt sich mit einer Hazard Ratio von 1,218 (p = 0,26) kein signifikanter Unterschied zwischen den beiden Armen. Die häufigste Nebenwirkung vom Grad 3 oder 4 war eine Neutropenie, die unter Lenalidomid deutlich häufiger war als unter Placebo (56 vs. 22 %); daneben waren auch Hautreaktionen zu sehen (5 vs. 1 %).
Details der Auswertung sowie die Ergebnisse einer anderen Studie, in der Everolimus als Erhaltungstherapie gegeben wurde, zeigen nach Ansicht von Dr. Thomas Witzig von der Mayo Clinic in Rochester, dass offenbar vor allem die Patienten von einer Erhaltung profitieren, die nach der Induktionstherapie noch ein positives PET-Ergebnis aufweisen. Diese Patienten würden nach bisheriger Vorgehensweise, sofern sie dafür fit genug sind, eher eine pla- tinhaltige Salvagetherapie mit autologer Stammzelltransplantation als eine Erhaltungstherapie bekommen.
Integration von Lenalidomid in die Induktion sinnvoller?
Thieblemont C et al. J Clin Oncol 2017, April 20 [Prepub ahead of print, DOI: 10.1200/JCO.2017.72.6984]
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).