Zwei Jahre mehr Progressionsfreiheit mit Ibrutinib plus Bendamustin-Rituximab
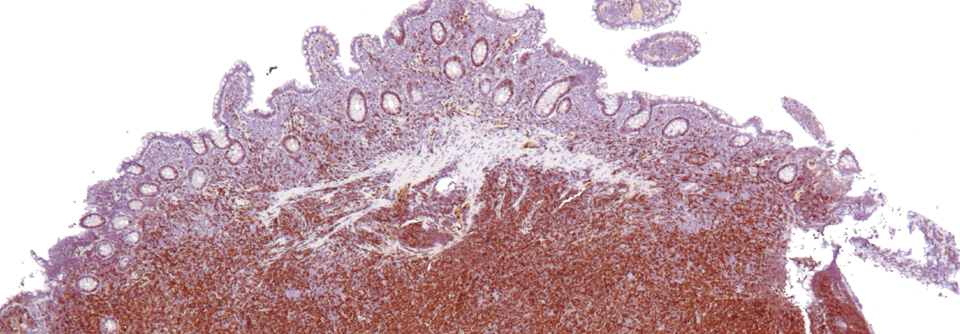
 In der SHINE-Studie wurden 523 Teilnehmende mit unbehandeltem Mantelzell-Lymphom eingeschlossen, die für eine Stammzelltransplantation nicht infrage kamen.
© Zhanna - stock.adobe.com
In der SHINE-Studie wurden 523 Teilnehmende mit unbehandeltem Mantelzell-Lymphom eingeschlossen, die für eine Stammzelltransplantation nicht infrage kamen.
© Zhanna - stock.adobe.com
Ältere Patient:innen mit neu diagnostiziertem Mantelzell-Lymphom (MCL) erhalten meist eine Chemoimmuntherapie, erinnerte Prof. Dr. Michael Wang vom MD Anderson Cancer Center, Houston. Die Gabe von alleinigem Bendamustin-Rituximab (BR) verlängerte im Vergleich zu R-CHOP das PFS – bei einem gleichzeitig besseren Sicherheitsprofil. Die Ergebnisse zweier Real-World-Studien weisen zudem darauf hin, dass Erkrankte von einer Rituximab-Erhaltung nach BR profitieren. In der rezidivierten/refraktären Situation wiederum kommt Ibrutinib zum Einsatz.
Progressionsrisiko sinkt um ein Viertel
Die Autor:innen einer Phase-1b-Studie hatten bereits die Wirksamkeit einer Kombination aus dem BTK-Inhibitor und BR in der Erstlinie demonstriert. Die Phase-3-Studie SHINE schließt hier an: 523 Teilnehmende ≥ 65 Jahre mit unbehandeltem MCL, die für eine Stammzelltransplantation nicht geeignet waren, bekamen eine BR-Induktion plus Ibrutinib oder Placebo und (im Fall einer kompletten oder partiellen Remission) eine Rituximab-Erhaltung. Das mediane Follow-up betrug 84,7 Monate.
Die Studie erreichte ihren primären Endpunkt: Das PFS verbesserte sich im experimentellen Arm signifikant um 2,3 Jahre im Vergleich zur Kontrolle, mit einer 25%igen Reduktion des Risikos für Progression oder Tod (median 80,6 Monate vs. 52,9 Monate; HR 0,75; p = 0,011). Das OS unterschied sich nicht. Bis auf Hochrisiko-Personen profitierten alle untersuchten Subgruppen von der Prüfkombination.
Knapp zwei Drittel erreichen ein Komplettansprechen
Die Gesamtansprechrate ähnelte sich mit 89,7 % vs. 88,5 %, allerdings erzielten Teilnehmende des Interventionsarms zumindest numerisch häufiger eine Komplettremission (CR; 65,5 % vs. 57,6 %). Die mediane Zeit bis zur nächsten Behandlung wurde unter Ibrutinib + BR nicht erreicht und betrug unter Placebo 92 Monate (HR 0,48). 19,9 % vs. 40,5 % erhielten eine anschließende Anti-Lymphomtherapie, 38,7 % der Placebo-Patient:innen einen BTK-Inhibitor.
81,5 % vs. 77,3 % der Betroffenen entwickelten behandlungsbedingte Nebenwirkungen vom Grad 3–4. Eine Neutropenie war das häufigste unerwünschte Ereignis in beiden Armen. Zu den Nebenwirkungen vom speziellen Interesse zählte ein Vorhofflimmern, unter dem 13,9 % vs. 6,5 % der Teilnehmenden litten (Grad 3/4: 3,9 % vs. 0,8 %).
"Klinisch bedeutsamer Effekt"
SHINE sei die erste Phase-3-Studie, in der die Wirksamkeit von Ibrutinib plus Chemoimmuntherapie bei Erkrankten mit unbehandeltem MCL gezeigt wurde. Der beobachtete PFS-Vorteil sei klinisch bedeutsam, betonte Prof. Wang. Dies setze einen neuen Maßstab für die Erstlinientherapie älterer Personen oder solcher, die für eine Stammzelltransplantation nicht infrage kommen.
Die Daten unterstützen den Einsatz der Kombination als Erstlinienoption für neu diagnostizierte MCL-Betroffene, sagte Diskutantin Prof. Dr. Kerry J. Savage, The University of British Columbia, Vancouver. Allerdings sei eine gute Patient:innenselektion notwendig, da es in SHINE zu u.a. erhöhten Raten von Neutropenien und kardialen Komplikationen gekommen war. Ein individuelles Vorgehen je nach Risikokategorie sei beim MCL angebracht.
Quelle: Wang M. 2022 ASCO Annual Meeting; Abstract LBA7502
Kongressbericht: 2022 ASCO Annual Meeting
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).