Immuntherapie wird Nr. 1
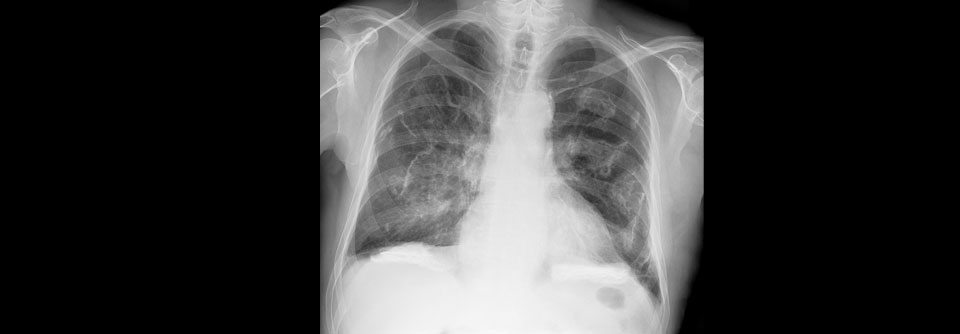
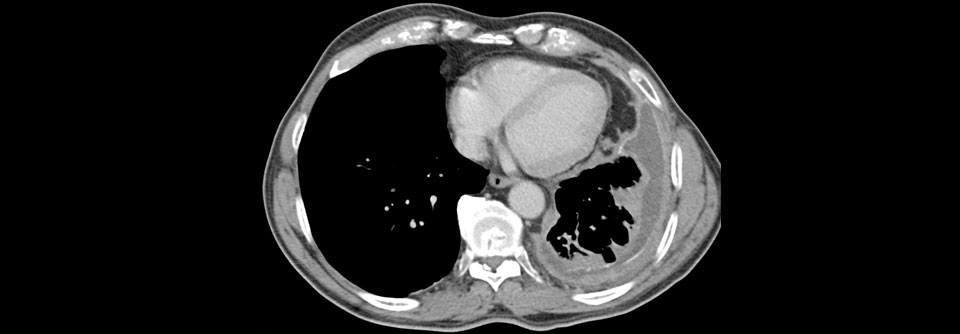
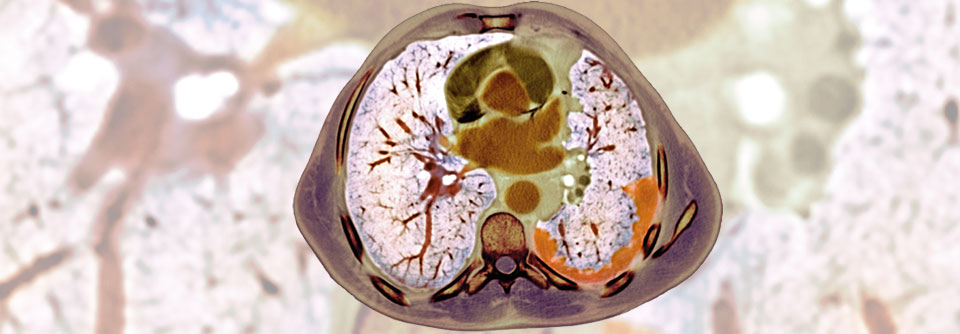 Das Thorax-CT eines 69 Jahre alten Patienten mit Mesotheliom (orange).
© Science Photo Library/Du Cane Medical Imaging
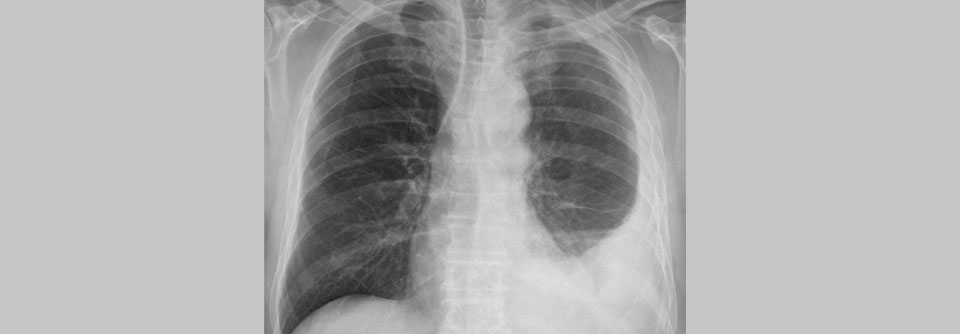
Das Thorax-CT eines 69 Jahre alten Patienten mit Mesotheliom (orange).
© Science Photo Library/Du Cane Medical Imaging
Das Konzept der onkologischen Immuntherapie basiert bekanntlich darauf, über die Inhibition von Immuncheckpoints auf der Oberfläche von T-Zellen die Immunbremse zu lösen, die der Tumor ihnen mithilfe spezifischer Liganden angelegt hat. Die entfesselten T-Zellen attackieren daraufhin die Tumorzellen und schicken sie in den Zelltod. Als Targets der Checkpoint-Inhibition dienen CTLA-4 und PD-1 bzw. dessen Ligand PD-L1, erklärte Dr. Selina Tsim, Universitätsklinikum Glasgow.
Patienten mit inoperablem Mesotheliom bringt die kombinierte Immuntherapie mit dem PD-1-Inhibitor Nivolumab und dem CTLA-4-Inhibitor Ipilimumab ein signifikant besseres Gesamtüberleben im Vergleich zur Chemotherapie. Das hat die Studie CheckMate 743 gezeigt.1 An der offenen randomisierten Phase-3-Studie mit verblindeter Endpunktauswertung nahmen 605 therapienaive Patienten mit Pleuramesotheliom teil. Die eine Hälfte erhielt Nivolumab (3 mg/kgKG alle zwei Wochen) plus Ipilimumab (1 mg/kgKG alle sechs Wochen) über bis zu zwei Jahre, die andere Hälfte bekam sechs Zyklen einer Kombination aus Cis- oder Carboplatin plus Pemetrexed.
Sterberisiko um mehr als 25 % reduziert
Die Immunkombi steigerte das mediane Gesamtüberleben auf 18,1 Monate versus 14,1 Monate unter der Chemotherapie (p = 0,002). Nach zwei Jahren lebten noch mehr als 40 % der Patienten unter Checkpoint-Blockade und 27 % unter Chemotherapie. Die entsprach einer Reduktion des Sterberisikos um mehr als 25 %. Patienten mit epitheloiden Tumoren profitierten kaum von der Immuntherapie, was vor allem daran lag, dass die Chemotherapie bei ihnen besonders gut abschnitt. Beim nicht-epitheloiden Mesotheliom war das Gesamtüberleben unter Immuntherapie mehr als doppelt so lang (18,1 vs. 8,8 Monate). Ein beträchtlicher Unterschied zwischen den beiden Behandlungsoptionen bestand außerdem bei der Responsedauer, die unter Nivo/Ipi 11,0 Monate betrug, unter Chemotherapie 6,7 Monate. Jeder dritte Patient unter Immuntherapie blieb über zwei Jahre in Remission (Chemotherapie: 8 %).
Die Immuntherapie konfrontiert Onkologen und Pneumologen mit neuen Formen der Toxizität, die durch unspezifische Immunaktivierung ausgelöst wird und nahezu jedes Organsystem in Mitleidenschaft ziehen kann.2
In den ersten beiden Monaten besonders gut aufpassen
Besonders häufig betroffen von solchen unerwünschten entzündlichen Reaktionen sind Haut, Gastrointestinaltrakt, Lunge, Niere und endokrine Organe, berichtete Dr. Tsim. Da sie verzögert auftreten und prolongiert verlaufen können, ist vor allem in den ersten zwei Monaten der Therapie besondere Wachsamkeit geboten. Eine kombinierte Checkpoint-Blockade ruft derartige Effekte besonders häufig hervor.
Entscheidend ist, sich mit den Grundlagen des Managements solcher Ereignisse vertraut zu machen. Bei Reaktionen der Schweregrade 1 und 2 reicht es oft aus, die Therapie zu unterbrechen, bis die Symptome verschwunden sind. Schweregrad 3 und 4 können Anlass sein, die Behandlung zu beenden. Der Stopp ist allerdings nicht zwingend. Ab Schweregrad 2 werden gewöhnlich Steroide benötigt, bei Steroidrefraktärität zusätzliche Immunsuppressiva, z.B. Infliximab oder Mycophenolat-Mofetil. Eine Ausnahme sind endokrine Probleme, bei ihnen sind Steroide oft unnötig. Dagegen sollte das Hormondefizit gecheckt und ggf. substituiert werden.
Benefit war unabhängig von der PD-L1-Expression
Ob man die Therapie wieder aufnehmen kann, richtet sich nach den Umständen im Einzelfall. In eine große retrospektive Kohortenstudie sind Daten von über 24.000 Fällen immunassoziierter Nebenwirkungen (irAE) unter Checkpoint-Inhibition eingeflossen.3 Bei jedem vierten Patienten wurde die Behandlung nach Unterbrechung wieder angesetzt, woraufhin bei 28 % dieselbe irAE erneut auftrat. Höhere Rezidivraten wurden nach Kolitis, Pneumonitis und Hepatitis beobachtet, niedrigere nach Nebennierendysfunktion.
Für Dr. Tsim sprechen die Studiendaten klar für die kombinierte Immuntherapie als Option der ersten Wahl bei inoperablem Mesotheliom. Sie hob hervor, dass der Benefit unabhängig von der PD-L1-Expression auf den Tumorzellen war, eine routinemäßige Bestimmung dieses Parameters beim Mesotheliom also nicht geboten erscheint. Jetzt wird es darum gehen, Biomarker zu identifizieren, an denen sich Patienten mit besonders guter Reponse vorab erkennen lassen, aber auch jene mit besonderer Anfälligkeit für irAE.
* European Respiratory Society
1. Baas P et al. Lancet 2021; 397: 375-386; DOI: 10.1016/S0140-6736(20)32714-8
2. Darnell EP et al. Curr Oncol Repo 2020; 22: 39; DOI: 10.1007/s11912-020-0897-9
3. Dolladille C et al JAMA Oncol 2020; 6: 865-871; DOI: 10.1001/jamaoncol.2020.0726
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).