Diagnostik und Therapie Leitlinie zur Behandlung des NSCLC auf Vordermann gebracht
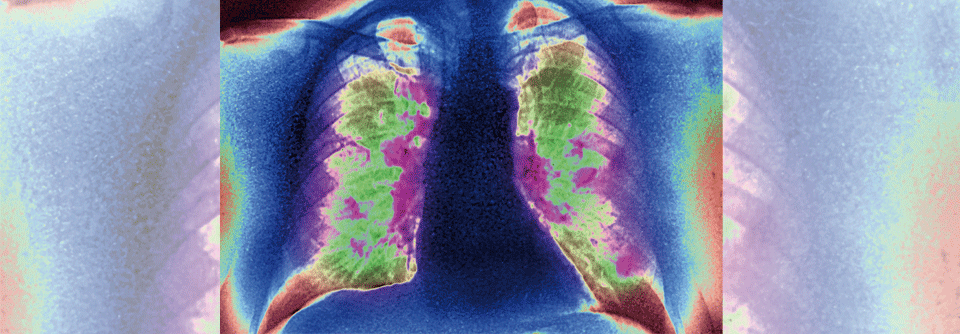 Lungenkrebs ist bei Frauen der dritt- und bei Männern der zweithäufigste maligne Tumor.
© Science Photo Library/Science Source/ James Cavallini
Lungenkrebs ist bei Frauen der dritt- und bei Männern der zweithäufigste maligne Tumor.
© Science Photo Library/Science Source/ James Cavallini
Jährlich erkranken in Deutschland rund 36.000 Männer und 21.000 Frauen an Lungenkrebs. In ca. 80 % der Fälle handelt es sich dabei um das nicht-kleinzellige Lungenkarzinom (NSCLC). Dank neuer Treibermutationen und entsprechender zielgerichteter Wirkstoffe eröffnen sich für Betroffene weitere Therapieoptionen. Um der rasanten Entwicklung Rechnung zu tragen, wurde die Leitlinie NSCLC kürzlich überarbeitet.
Noch kein Konsens hinsichtlich eines Screenings
Die Autoren hatten sich schon in den Vorgängerversionen mit der Früherkennung mittels Niedrig-Dosis-Computertomographie des Thorax beschäftigt. Dass dies die krebsspezifische Mortalität senken kann, verdeutlichen unter anderem die Daten…
Bitte geben Sie Ihren Benutzernamen und Ihr Passwort ein, um sich an der Website anzumelden.