T2-high und T2-low als Fake News
 Faktoren wie ICS, Infekte und Rauchen können die Eosinophilie beim Asthma bronchiale maskieren.
© iStock/Togetherless
Faktoren wie ICS, Infekte und Rauchen können die Eosinophilie beim Asthma bronchiale maskieren.
© iStock/Togetherless
Jeder Irrsinn hat eine Vorgeschichte! Mit diesen Worten eröffnete der Chef der Pneumologie am Universitätsklinikum Rostock seinen Vortrag zum T2-high- and T2-low-Asthma. Die Vorgeschichte besteht für ihn in den wechselnden Definitionen des Asthma bronchiale. Die wurden im Laufe der Zeit nicht schärfer, sondern diffuser und gipfelten im GINA-Report 2014 in der Aussage, obstruktive Atemwegserkrankungen bildeten ein Spektrum von Krankheiten. Asthma sei heterogen mit vielen verschiedenen klinischen und inflammatorischen Phänotypen.
Antikörperentwicklung pushte Eosinophilen-Karriere
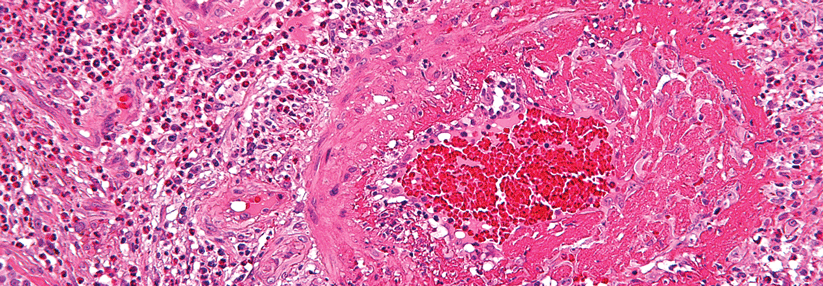
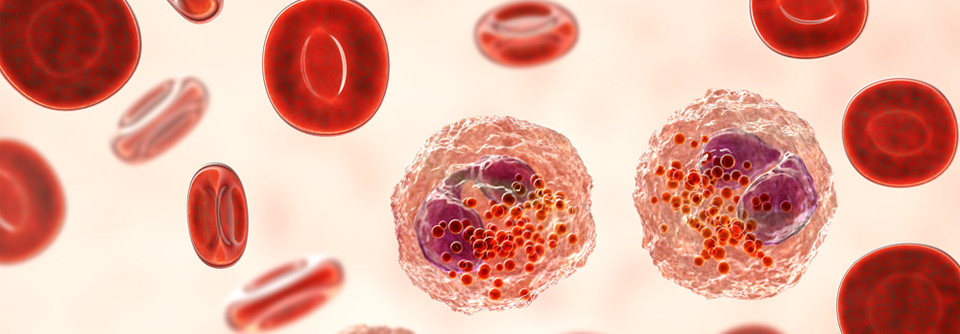
Dass Eosinophile eine zentrale Rolle bei der asthmatischen Entzündung einnehmen, ist schon seit mehr als 100 Jahren klar und seither immer wieder erhärtet worden. Schon vor Einführung der inhalativen Steroide (ICS) gab es erfolgreiche Versuche, anhand des Differenzialblutbildes die Steroiddosis zu steuern und Exazerbationen vorherzusagen.
Einen Kick bekam die Karriere der Eos beim Asthma mit Einführung der IL-5-Antikörper. „Jetzt konnte man das behandeln, also musste ein neuer Begriff her“, so Prof. Virchow. Dass nun also vom „eosinophilen Asthma“ gesprochen wird, ist ihm als Sprachpuristen ein Graus. Denn natürlich ist nicht das Asthma eosinophil, also eosinaffin, die Entzündungszellen sind es. Prof. Virchow würde den Begriff „Asthma mit Eosinophilie“ vorziehen, ist aber zugleich der Überzeugung, dass es ein Asthma ganz ohne Eosinophilie gar nicht gibt.
Mit Einführung des Anti-IL4/13-Antikörpers Dupilumab hat sich das Bild erneut gewandelt. Dessen Wirksamkeit lässt sich nämlich gleich an zwei Biomarkern festmachen, der Eosinophilenzahl und dem NO im Exhalat. FeNO ist zwar nicht gänzlich unabhängig von Eosinophilen, weil es von diesen Zellen gebildet wird. Es gibt jedoch mit den Atemwegsepithelzellen eine weitere FeNO-Quelle, sodass hohe Werte nicht automatisch mit hohen Eosinophilenzahlen korrelieren, erläuterte der Kollege.
Differenzialdiagnostisch ist das Blutbild vor allem bei unbehandelter obstruktiver Atemwegserkrankung obligat und FeNO hilfreich, etwa wenn unter inhalativen Kortikosteroiden die Eosinophilie maskiert ist, so Prof. Virchow. Er mahnte aber zur Vorsicht: „Biomarker und Treatable Traits ersetzen keine Diagnose.“ Nichtsdestotrotz gab es als neue Label „T2-high“ und „T2-low“.
Der Rostocker Kollege nahm sich als Beispiel für Letzteres das „raucherassoziierte neutrophile Asthma“ vor: „Dazu kann man im Einzelfall vielleicht auch COPD sagen.“ Die Datenlage bezeichnete er als mickrig. Sie bezieht sich ausschließlich auf Sputumanalysen, man hat keine Longitudinalverläufe, sodass unklar bleibt, wie stabil dieser Phänotyp eigentlich ist. Außerdem sind mögliche Confounder wie Rauchen, Infektionen, Steroidtherapie und Komorbiditäten schlecht untersucht. Der üblicherweise verwendete Cut-off-Wert von 40 % Neutrophilen im Sputum erscheint willkürlich gewählt, zumal bei Gesunden die 90ste Perzentile – also die obere Grenze des Normalen – bei knapp 65 % liegt. Und egal was bisher an spezifischen Strategien versucht wurde, um das „neutrophile“ Asthma zu zähmen – nichts hat gefruchtet, manches sogar eher geschadet.
Für Prof. Virchow läuft alles darauf hinaus, dass ein Asthma unwahrscheinlich ist, wenn sich bei einem Patienten mit reversibler Atemwegsobstruktion und bronchialer Hyperreagibilität weder im Blut noch im Sputum erhöhte Eosinophile nachweisen lassen. Natürlich gibt es Faktoren, welche die Eosinophilie maskieren, etwa hoch dosierte Steroide, Infekte oder Rauchen, die zudem Neutrophilie induzieren, ohne dass daraus ein „neutrophiles“ Asthma wird.
Hohe ICS-Dosen beeinflussen Anti-IL-5-Indikation
Auch ICS senken in hohen Dosen die Eosinophilenzahlen, wie eine Studie aus der Rostocker Klinikambulanz für schweres Asthma zeigt. Das gilt es zu berücksichtigen, wenn die Indikation für Biologika gestellt wird. Die Eos können so dramatisch abfallen, dass sie die Indikationsschwelle für Anti-IL-5 unterschreiten. „Deshalb ist die Einteilung von Asthma in T2-high und T2-low nicht nur sinnfrei, sondern gefährlich“, betonte Prof. Virchow. „Für den klinischen Alltag gilt: Was nicht T2 ist, ist kein Asthma.“
Kongressbericht: 61. Kongress der Deutschen Gesellschaft für Pneumologie und Beatmungsmedizin (Online-Veranstaltung)
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).