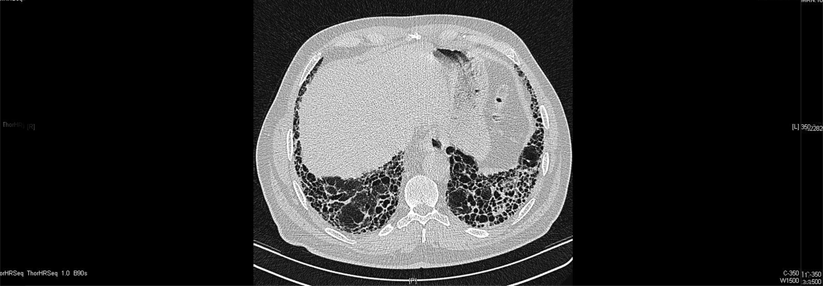
Was bei der idiopathischen Lungenfibrose für und gegen die Soforttherapie spricht
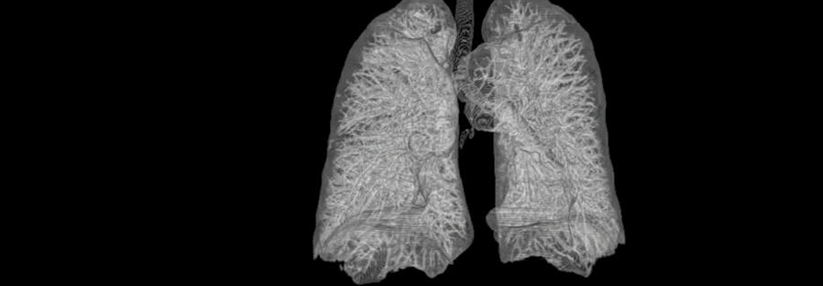
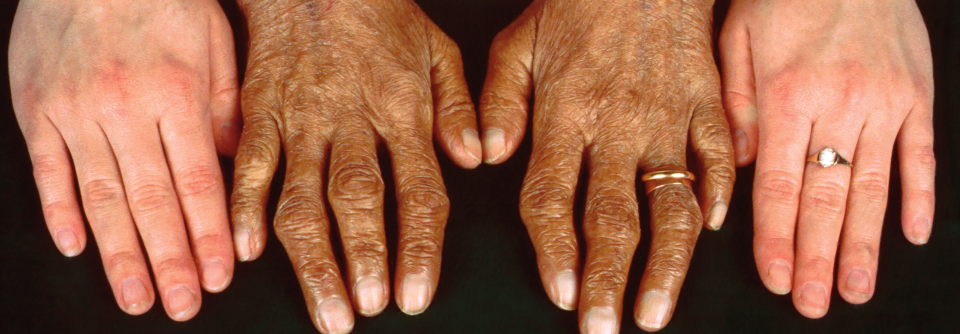
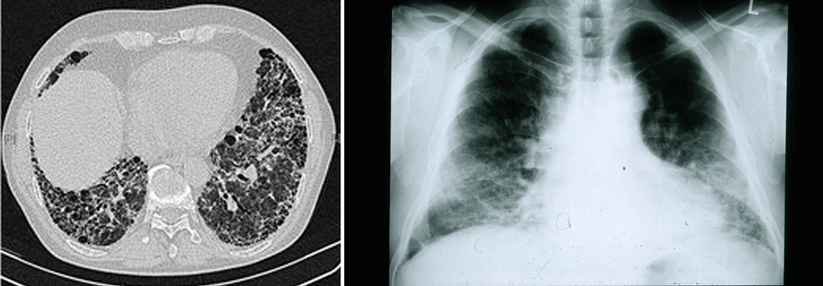 Wann sollte bei der idiopathischen Lungenfibrose mit der Therapie begonnen werden?
© Wikimedia/IPFeditor (CC BY-SA 3.0)
Wann sollte bei der idiopathischen Lungenfibrose mit der Therapie begonnen werden?
© Wikimedia/IPFeditor (CC BY-SA 3.0)
Die idiopathische Pulmonalfibrose (IPF) ist eine sehr heterogene Erkrankung, deren klinischer Verlauf sich im Einzelfall nicht vorhersagen lässt. Mit Nintedanib und Pirfenidon stehen zwei Wirkstoffe zur Verfügung, die den Abfall der forcierten Vitalkapazität als wichtigsten Surrogatparameter für das Überleben in etwa halbieren, erklärte Professor Dr. Andreas Günther, Chef der Pneumologie am Agaplesion Evangelisches Krankenhaus Mittelhessen in Gießen. Tatsächlich spiegelte sich das in den Zulassungsstudien in einem Rückgang der Gesamtmortalität um 48 % (Pirfenidon) respektive 30 % (Nintedanib) wider.1,2
Eine retrospektive Analyse australischer Registerdaten ergab, dass IPF-Patienten ohne…
Bitte geben Sie Ihren Benutzernamen und Ihr Passwort ein, um sich an der Website anzumelden.