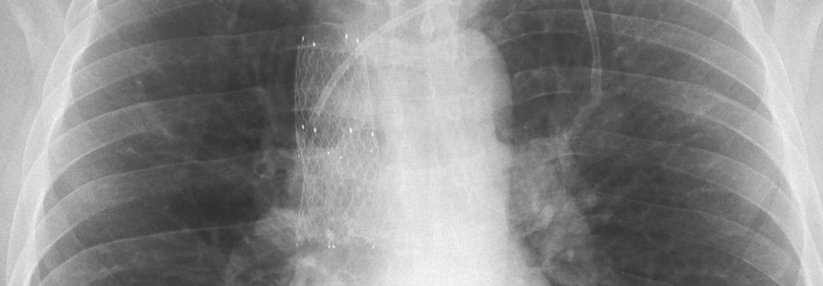
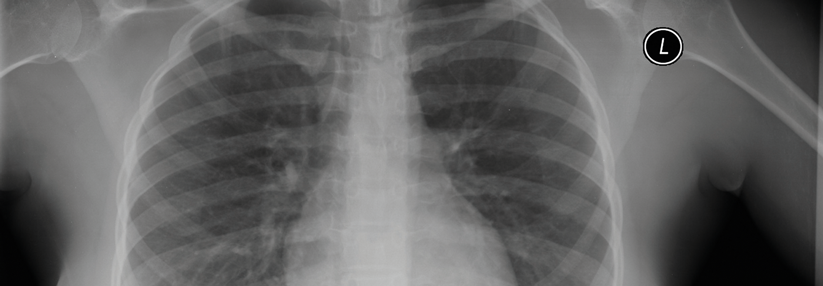
Weitere Mutationen und Hirnmetastasen beeinflussen Wirkung von Sotorasib nicht
 Für die Behandlung von Erwachsenen mit fortgeschrittenem NSCLC und KRASG12C-Mutation ist seit Kurzem der erste spezifische KRASG12C-Inhibitor als Monotherapie zugelassen.
© Aiden – stock.adobe.com
Für die Behandlung von Erwachsenen mit fortgeschrittenem NSCLC und KRASG12C-Mutation ist seit Kurzem der erste spezifische KRASG12C-Inhibitor als Monotherapie zugelassen.
© Aiden – stock.adobe.com
Mit Sotorasib ist seit Kurzem der erste spezifische KRASG12C-Inhibitor als Monotherapie für die Behandlung von Erwachsenen mit fortgeschrittenem NSCLC und KRASG12C-Mutation zugelassen, deren Tumor nach mindestens einer vorherigen systemischen Therapie progredient wurde. Die Zulassung beruht auf den Ergebnissen der Phase-3-Studie CodeBreak 200, in der 345 Patient:innen mit NSCLC und KRASG12C-Mutation nach mindestens einer vorangegangenen Behandlung, darunter Chemotherapie und CPI, randomisiert Sotorasib oder Docetaxel erhalten hatten. Der Inhibitor verbesserte Ansprechen und progressionsfreies Überleben bei geringerer Toxizität. Zwei Subgruppenanalysen geben Aufschluss zu genetischen Biomarkern und zur Wirkung auf Hirnmetastasen.
NOTCH-Mutation verschlechtert Prognose
Fanden sich Mutationen im NOTCH-Gen, so schien Sotorasib hinsichtlich des PFS mit median 2,8 Monaten vs. 7,5 Monaten schlechter abzuschneiden als Docetaxel; der Effekt war nicht signifikant, sollte aber künftig genauer untersucht werden.
Zu Studienbeginn, so Prof. Dr. Dr. Ferdinandos Skoulidis, MD Anderson Cancer Center in Houston, untersuchten die Autor:innen Tumorgewebe und Plasma mittels Next Generation Sequencing auf Mutationen in wichtigen Genen wie STK11, KEAP1, EGFR, MET und TP53 und ermittelten aus zirkulierender Tumor-DNA im Plasma die Mutationslast.1 Diese Marker wurden mit Ansprechen und progressionsfreiem Überleben korreliert.
Sotorasib verbessert PFS
Die Forschenden detektierten die häufigsten Alterationen im TP53-Gen (57,1 %), gefolgt von STK11 (37,5 %) und KEAP1 (25,9 %); 17,4 % der Teilnehmenden hatten sowohl STK11- als auch KEAP1-Mutationen. Sotorasib erwies sich der Chemotherapie in den meisten genetischen Subgruppen als überlegen und verbesserte das PFS zudem unabhängig von der PD-L1-Expression. 8,2 % der Erkrankten hatten neben der G12C-Mutation weitere Veränderungen im KRAS-Gen, einschließlich Amplifikationen; bei ihnen war keine der beiden Therapien wirksam. Die Wissenschaftler:innen beobachteten darüber hinaus eine negative Korrelation zwischen PFS und Tumormutationslast im Plasma zu Beginn der Studienteilnahme (p < 0,0001).
Viele Patient:innen mit NSCLC entwickeln Hirnmetastasen, die sich sowohl auf die Prognose als auch auf die Lebensqualität negativ auswirken. In CodeBreak 200 wiesen 40 vs. 29 Personen (23 % vs. 17 %) im Sotorasib- vs. Docetaxelarm ZNS-Metastasen auf, so Prof. Dr. Anne-Marie C. Dingemans, Erasmus MC Cancer Institute Rotterdam. In dieser Gruppe betrug das mediane systemische PFS nach median 20 Monaten 6,1 Monate versus 4,5 Monate (HR 0,57; 95%-KI 0,30 – 1,07; p = 0,045). Die Zeit bis zu einem intrakraniellen Rezidiv erreichte median 9,6 Monate vs. 5,4 Monate (HR 0,84; 95%-KI 0,32–2,19; p = 0,37).
Quellen:
1. Skoulidis F et al. 2023 ASCO Annual Meeting; Abstract 9008
2. Dingemans AM et al. 2023 ASCO Annual Meeting; Abstract 9016
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).