Wenn das Heparin nicht wirkt
 Im Rahmen von akuten Infektionen muss die Heparindosis mitunter erhöht werden. Wie hoch, ist allerdings schwierig zu ermitteln.
© Angel Arredondo – stock.adobe.com
Im Rahmen von akuten Infektionen muss die Heparindosis mitunter erhöht werden. Wie hoch, ist allerdings schwierig zu ermitteln.
© Angel Arredondo – stock.adobe.com
Anhand des Molekulargewichts unterscheidet man unfraktioniertes (UFH) und niedermolekulares (NMH) Heparin. Die blutverdünnende Wirkung von UFH beruht hauptsächlich auf der Hemmung von Thrombin und weniger auf der Inhibition von Faktor Xa. NMH hemmt dagegen im Wesentlichen den Faktor Xa, erläutern Dr. Jerrold Levy vom Department of Anesthesiology, Critical Care und Surgery der Duke University School of Medicine in Durham und Professor Dr. Jean Connors von der Hematology Division am Brigham and Women’s Hospital in Boston. UFH stellt aufgrund seiner kurzen Halbwertszeit sowie der Antagonisierbarkeit mit Protamin gerade bei kritisch kranken Patienten sowie beim Einsatz eines extrakorporalen Kreislaufs (z.B. Bypasschirurgie, extrakorporale Membranoxygenierung/ECMO) das Antikoagulans der Wahl dar.
Eine Heparinresistenz liegt vor, wenn trotz angemessener Heparindosis das Antikoagulationsziel nicht erreicht wird, so die Wissenschaftler weiter. Beide Parameter sind allerdings nicht genau definiert. Zudem spielt es eine Rolle, welcher Labortest für die Diagnose herangezogen wird.
Heparinmoleküle binden an Proteine, Zellen und Kanülen
Das Monitoring der UFH-Therapie kann mithilfe der aktivierten partiellen Thromboplastinzeit (aPTT), der aktivierten Gerinnungszeit (ACT, activated clotting time) oder dem Anti-Faktor-Xa-Spiegel erfolgen. Zur Überwachung der NMH-Behandlung eignet sich dagegen lediglich der Anti-Faktor-Xa-Spiegel.
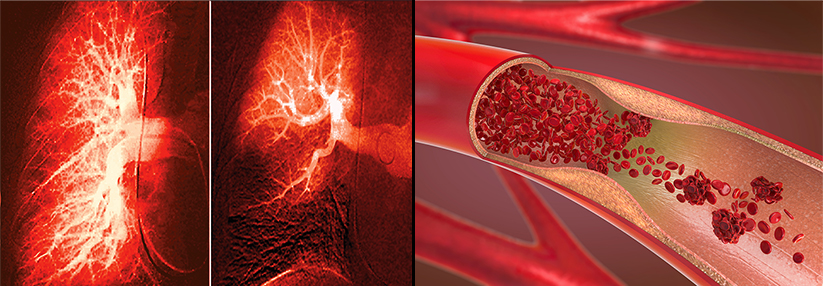
Die Ursachen der Heparinresistenz sind vielfältig, berichten Dr. Levy und Prof. Connors. Die stark negativ geladenen Heparinmoleküle, insbesondere UFH, binden unter anderem an verschiedene Proteine (z.B. Plättchenfaktor 4, Lipoproteine, von-Willebrand-Faktor, Fibrinogen), an Monozyten, Endothelzellen und Wachstumsfaktoren sowie an künstliche Oberflächen (z.B. Venenzugänge, Systeme zur extrakorporalen Zirkulation). Auch ein angeborener oder erworbener Antithrombinmangel kann eine Heparinresistenz begünstigen. Zudem verringert UFH selbst die Antithrombinaktivität, fördert die Ausschüttung von Plättchenfaktor 4 und triggert die Bildung von Antikörpern im Sinne einer heparininduzierten Thrombozytopenie.
Besondere Aktualität erlangt die Problematik der Heparinresistenz angesichts der gegenwärtigen Coronaviruspandemie, berichten die Forscher. COVID-19 induziert – ähnlich wie andere akute inflammatorische Erkrankungen (z.B. die H1N1-Influenza) – einen Zustand der Hyperkoagulabilität mit Anstieg der Faktor-VIII- und Fibrinogenkonzentration. Dadurch verkürzt sich die aPTT, sodass zum Erreichen des Zielfensters höhere Heparindosen erforderlich sind. Viele intensivpflichtige Patienten erhalten zur Thromboseprophylaxe und -therapie UFH. Unklar ist dabei allerdings, welche Dosierung eine Thrombose und andere unerwünschte Ereignisse sicher verhindert.
Bei Verdacht auf eine Heparinresistenz empfehlen die Autoren die Bestimmung des Anti-Faktor-Xa-Spiegels. Therapeutisch stellt sich ihrer Einschätzung nach zudem die Frage nach dem Nutzen einer Antithrombin-Supplementation. Belastbare Daten hierzu existieren allerdings bislang nur für herzchirurgische Indikationen. Eine weitere Option sind die intravenös zu verabreichenden direkten Thrombininhibitoren Argatroban und Bivalirudin, die zunehmend bei intensivpflichtigen COVID-19-Patienten zum Einsatz kommen. Außer der aPTT, die jedoch durch erhöhte Fibrinogenspiegel verfälscht werden kann, sowie der ACT existieren jedoch bislang keine Tests zur Überprüfung ihrer Effektivität.
Die Heparinisierung von Patienten mit akuten Infektionen ist häufig problematisch, so das Fazit der Wissenschaftler. Angesichts der prokoagulatorischen Veränderungen ergeben sich nicht selten Diskrepanzen zwischen den verschiedenen Gerinnungstests, wodurch das Monitoring erschwert wird. Zudem neutralisieren Akutphasemoleküle UFH, was Dosissteigerungen erforderlich macht.
Quelle: Levy JH, Connors JM. N Engl J Med 2021; 385: 826-832; DOI: 10.1056/NEJMra2104091
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).