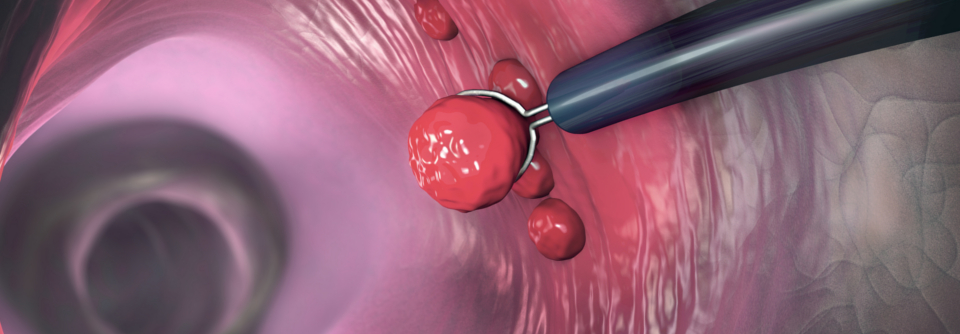
Gastrointestinale Karzinome Impfen, screenen, endoskopieren
 Ungefähr jeder dritte Krebspatient weltweit stirbt an den Folgen eines gastrointestinalen
Tumors.
© iStock/sefa ozel
Ungefähr jeder dritte Krebspatient weltweit stirbt an den Folgen eines gastrointestinalen
Tumors.
© iStock/sefa ozel
Zwar gab es in den letzten Jahren bedeutende Fortschritte in der Diagnostik und Therapie maligner Erkrankungen des Verdauungstrakts. Dennoch stirbt ungefähr jeder dritte Krebspatient weltweit an den Folgen eines gastrointestinalen Tumors. Daher stellt sich die Frage, wie sich diese verhindern lassen. Das Team um Professor Dr. Dr. Andreas Teufel vom Universitätsklinikum Mannheim fasst aktuelle Erkenntnisse zur Prävention dieser Tumoren zusammen.
Beim Plattenepithelkarzinom des Ösophagus (PECA) spielen sowohl Umwelt- als auch genetische Faktoren eine Rolle. Alkohol und Nikotin sind in westlichen Ländern in etwa 90 % der Fälle für die Entwicklung des PECA verantwortlich. Als weiterer Risikofaktor wird die Ernährung diskutiert: wenig Obst und Gemüse, eine schlechte Versorgung mit Vitaminen und Spurenelementen, mit Mykotoxinen behaftete Lebensmittel sowie der Konsum von sauer eingelegten, gepökelten und sehr scharf gewürzten, heißen Speisen lassen wohl insbesondere in asiatischen Ländern die Inzidenzen steigen. Auch ein niedriger sozioökonomischer Status sowie u.a die Exposition gegenüber polyzyklischen Kohlenwasserstoffen wird mit dem Plattenepithelkarzinom des Ösophagus in Verbindung gebracht.
Darüber hinaus begünstigen bestimmte Viren und Bakterien ein Plattenepithelkarzinom des Ösophagus, es sollte daher auf eine gute Zahngesundheit geachtet werden. Welche Screeningmethoden (z.B. Zytosponge oder Liquid-Biopsy) sich für diese Karzinomform eignen konnte nicht eindeutig geklärt werden, die Autoren empfehlen in jedem Fall Patienten nach einem PECA oder einem Tumor im Kopf-Hals-Bereich engmaschig zu überwachen.
Barrett im Frühstadium kann man gut in Schach halten
Als prädisponierend für das ösophageale Adenokarzinom (EAC) gilt die Barrett-Ösophagus-Metaplasie (BE). Hauptrisikofaktor für ihre Entstehung sind chronische Refluxsymptome z.B. im Rahmen der gastroösophagealen Refluxkrankheit (GERD). Wichtig in diesem Zusammenhang: die inflammatorische Reaktion auf den Reflux, die ein krebsförderndes Milieu schafft.
Einerseits entwickeln nur wenige Barrett-Patienten ein ösophageales Adenokarzinom, weshalb sich ein flächendeckendes BE-Screening nur eingeschränkt eignet, um die Karzinom-Mortalität zu senken. Andererseits lässt sich durch ein frühes Einschreiten mit PPI, NSAR oder ablativen Verfahren der Barrett-Ösophagus im Frühstadium gut unter Kontrolle bringen und einer mögliche Progression vorbeugen.
Die allgemeinen Risikofaktoren für BE und damit ösophageale Adenokarzinome sind ähnlich: männliches Geschlecht, kaukasische Ethnie, Adipositas (z.B. Taillenumfang > 102 cm), Rauchen, Alter > 50 Jahre oder eine positive Familienanamnese. Die Autoren schlagen ein Screening auf BE bzw. ösophageale Adenokarzinome bei Männern vor, die zwei Jahre oder länger mindestens wöchentlich unter Refluxsymptomen leiden oder die fünf Jahre oder länger Reflux plus wenigstens zwei der o.g. Risikofaktoren aufweisen. Ob sich auch ein allgemeines Screening für Menschen mit Refluxsymptomen lohnt, müsste anhand von Risikofaktoren stratifiziert werden.
An der Pathogenese des Magenkarzinoms sind verschiedene Faktoren beteiligt. Der Wichtigste ist die durch H. pylori bedingte Gastritis. In Deutschland sind etwa 50 % der über 50-Jährigen mit dem Stäbchenbakterium infiziert, bei jungen Erwachsenen findet sich eine Infektionsrate von ca. 20 %. Präventiv empfehlen die Autoren eine Eradikation in Risikogruppen, wobei diese möglichst früh im Verlauf der Gastritis durchgeführt werden sollte, noch bevor sich präneoplastische Läsionen gebildet haben. Patienten mit fortgeschrittener Atrophie oder intestinaler Metaplasie des Magens sollten endoskopisch überwacht werden. Als weitere risikoassoziierte Faktoren gelten Alkohol, nitrithaltige Lebensmittel und Tabakkonsum.
Rauchen erhöht auch signifikant das Risiko, an einem Pankreaskarzinom zu erkranken. Alkoholkonsum fördert die Entwicklung einer chronischen Pankreatitis, die ihrerseits das Karzinomrisiko ansteigen lässt. Ebenso ist Adipositas ein (oft unterschätzter) Risikofaktor für die Entwicklung eines Pankreaskarzinoms, was darauf zurückgeführt wird, dass Fettzellen Mediatoren freisetzen, die eine chronische Inflammation bedingen. Umgekehrt kann körperliche Aktivität das Risiko reduzieren. Daher empfiehlt die deutsche S3-Leitlinie zur Prävention des Pankreaskarzinoms den Verzicht auf Tabak- und exzessiven Alkoholkonsum, die Vermeidung von Übergewicht und die Förderung körperlicher Aktivität. Eine etablierte Früherkennung gibt es für das Pankreaskarzinom in Deutschland aufgrund des fehlenden Nutzennachweises noch nicht. Bei einzelnen Hochrisikopatienten allerdings genauer hinzuschauen, könne nach Meinung der Autoren aber nicht schaden.
Größter Risikofaktor für das hepatozelluläre Karzinom (HCC) ist die Leberzirrhose. Meist wir sie durch eine chronische Hepatitis B bzw. C, chronischen Alkoholkonsum und Fettleberhepatitiden ausgelöst. Innerhalb von fünf Jahren entwickeln 5–30 % der Zirrhotiker ein HCC und stellen damit eindeutig die Risikogruppe dar. Für die Prävention des Karzinoms lassen sich folgende Maßnahmen ableiten: Hepatitis-B-Impfung, Alkoholkarenz bei bekannter Lebererkrankung, medikamentöse Behandlung, falls eine chronische Hepatitis vorliegt sowie Gewichtsreduktion bei Fettleber. Außerdem wurden positive Effekte von Medikamenten wie Metformin oder Statinen in einzelnen Studien beschrieben. Zusätzlich sollten die Patienten halbjährlich zur Ultraschallkontrolle, wenn eine Leberzirrhose oder hochgradige Leberfibrose vorliegt.
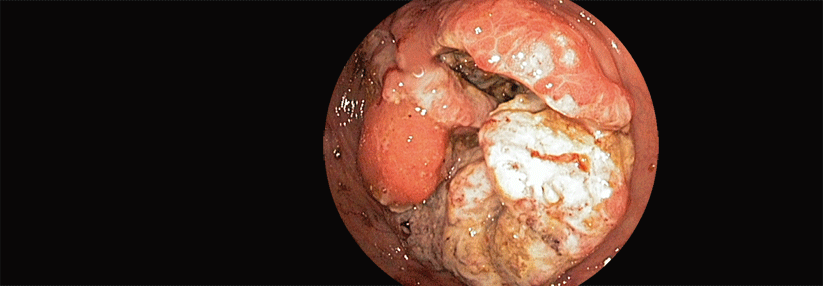
Beim kolorektalen Karzinom werden als Risikofaktoren Rauchen, erhöhter Alkoholkonsum, Bewegungsmangel, Übergewicht, rotes und verarbeitetes Fleisch und eine ballaststoffarme Ernährung sowie in diesem Zusammenhang auch ein Diabetes mellitus Typ 2 gehandelt. Das Risiko lässt sich folglich durch einen gesunden Lebensstil positiv beeinflussen.
Wer keine Koloskopien will, sollte Stuhlproben abgeben
Die Datenlage zu präventiv wirkenden Medikamenten oder Mikronährstoffen ist mau. Nachweislich sinnvoll ist dagegen die Vorsorge-Darmspiegelung für Männer ab dem 50. Lebensjahr und für beide Geschlechter ab dem 55. Lebensjahr. War die erste Koloskopie unauffällig, sollte nach zehn Jahren eine weitere Untersuchung erfolgen. Bei Patienten, die Koloskopien ablehnen, sollten regelmäßig immunologische Tests auf okkultes Blut (i-FOBT) durchgeführt werden.
Quelle: Teufel A et al. Z Gastroenterol 2021; 59: 964-982; doi: 10.1055/a-1540-7539