Radiofrequenzablation schaltet ventrikuläre Tachykardie ab
 Supraventrikuläre Arrhythmien können ventrikuläre imitieren.
© iStock/Andrey Mitrofanov
Supraventrikuläre Arrhythmien können ventrikuläre imitieren.
© iStock/Andrey Mitrofanov
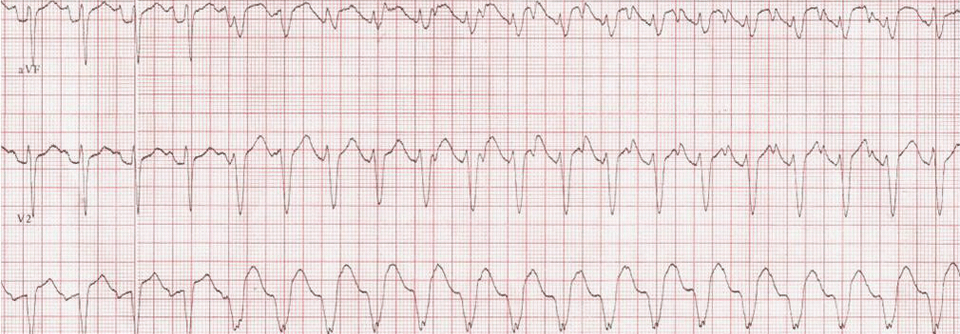
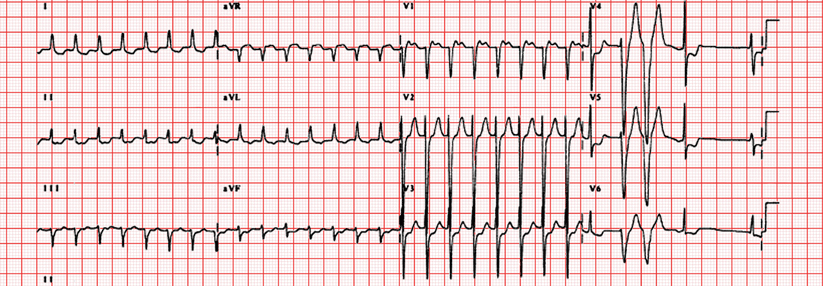
Kammertachykardien nehmen ihren Ursprung in abnormen elektrischen Herden oder Kreisläufen im Myokard. Im EKG stellen sie sich meist als Tachyarrhythmie mit breitem QRS-Komplex dar. Klinisch reicht die Palette von völliger Beschwerdefreiheit über Schwindel und Synkope hin zum plötzlichen Herztod. In der Betreuung der Patienten stellen sich drei grundsätzliche Fragen:
- Liegt eine strukturelle Herzerkrankung vor – und falls ja, wie ausgeprägt ist sie?
- Besteht aufgrund der Rhythmusstörung ein hohes Risiko für plötzlichen Herztod?
- Wie sieht es mit dem Nutzen-/Risikoprofil der verfügbaren Therapien aus?
Im Gefolge struktureller Herzerkrankungen gehen Kammertachykardien mit einem erhöhten Risiko für plötzlichen Herztod einher, schreibt Dr. Kalyanam Shivkumar, Kardiologe von der University of California in Los Angeles. Daher werden Betroffene meist mit einem implantierbaren Cardioverter-Defibrillator (ICD) versorgt. Allerdings verhindert der ICD das ventrikuläre Rasen nicht.
Für den Eingriff reicht meist eine leichte Sedierung
Tritt es häufig auf, können die vielen Stromstöße den Kranken sehr belasten, sodass eine zusätzliche Behandlung erforderlich ist. Medikamentös kommen dafür Betablocker und Antiarrhythmika wie Amiodaron infrage. Bei Patienten mit ventrikulärer Tachykardie ohne strukturelle Herzerkrankung besteht nur ein geringes Risiko für einen plötzlichen Herztod. Häufig werden sie symptomatisch behandelt, wobei Betablocker und Nicht-Dihydropyridin-Kalziumantagonisten als Erstlinientherapie zum Einsatz kommen.
Erste Berichte über den erfolgreichen Einsatz einer Katheterablation in der Therapie einer Kammertachykardie gab es 1983. Seit der Entwicklung der Radiofrequenzablation in den 1990er-Jahren findet das Verfahren zunehmend Verbreitung. Im Falle einer strukturellen Herzkrankheit ist die Ablation bei anhaltender monomorpher Kammertachykardie indiziert, die trotz medikamentöser Behandlung rezidiviert oder wenn die Präparate zu inakzeptablen Nebenwirkungen führen bzw. nicht gewünscht werden. Liegt kein strukturelles Leiden vor, besteht die Indikation zur Verödung, sobald ein monomorphes ventrikuläres Rasen Beschwerden verursacht oder Antiarrhythmika nicht ausreichend wirken. Patienten, die stark unter monomorphen ventrikulären Extrasystolen mit einer Kammerdysfunktion leiden, können ebenfalls von der Intervention profitieren.
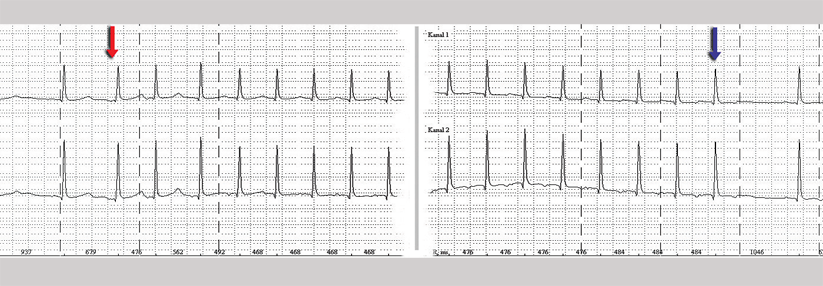
Meist reicht für sie eine leichte Sedierung. Ein 12-Kanal-EKG, das während einer entsprechenden Tachykardie-Episode aufgezeichnet wurde, weist darauf hin, wo das arrhythmogene Areal liegt. Dennoch führt man vor der Ablation immer eine vollständige elektrophysiologische Untersuchung durch, um Lokalisation und Art der Arrhythmie genau zu bestimmen. Sie dient zudem dazu, die Entstehung aus der Kammer zu bestätigen. Denn manche supraventrikuläre Rhythmusstörungen können ventrikuläre imitieren.
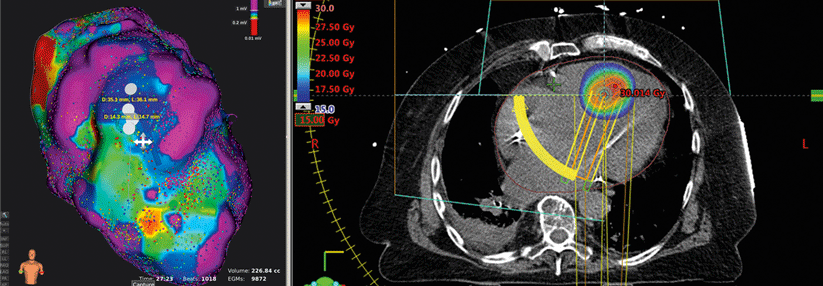
Wenn der Ursprungsort mithilfe einer elektrophysiologischen Kartierung („Mapping“) gefunden wurde, lässt er sich mittels Radiofrequenz über einen entsprechenden Katheter veröden. Die klinischen Erfolge hängen von verschiedenen Faktoren ab. Besonders gute Chancen haben Patienten ohne strukturelle Herzkrankheit (s. Kasten).
Wie sind die Erfolgsaussichten?
- Unter Patienten ohne strukturelle Herzerkrankung wurde über Erfolgsquoten von mehr als 80 % berichtet – sowohl bei anhaltender Kammertachykardie als auch bei ventrikulären Extrasystolen.
- Bei struktureller Herzerkrankung und ICD-Schocks reduziert die Katheterablation die Belastung durch ventrikuläres Herzrasen. Kranken mit mehr als drei Kammertachykardie-Episoden („elektrischer Sturm“) täglich kann die Ablation sogar das Leben retten.
- Insgesamt liegt die Erfolgsrate durch die Verödung in Fällen ischämischer Kardiomyopathien nach einem Herzinfarkt höher (56–77 %) als bei nicht-ischämischer Kardiomyopathie (38–67 %).
Quelle: Shivkumar K. N Engl J Med 2019; 380: 1555-1564