Endlich ein Standard für die akute Graft-versus-Host-Erkrankung?
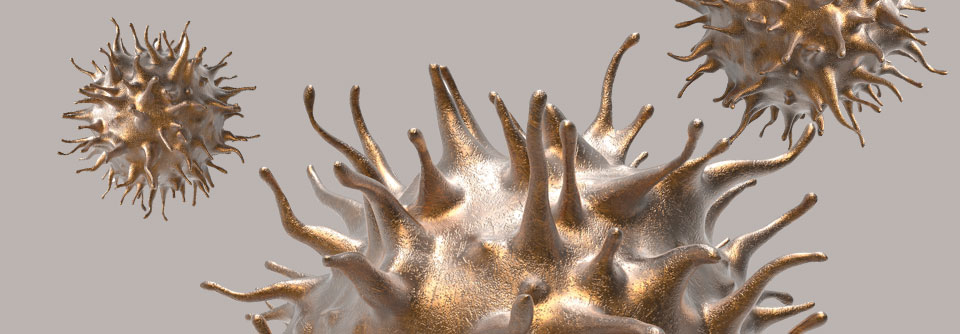
 Bei diesem Mann hat sich aus einer akuten eine chronische GvHD gebildet – zu sehen an der vermehrten Hautpigmentierung.
© Science Photo Library/Biophoto Associates
Bei diesem Mann hat sich aus einer akuten eine chronische GvHD gebildet – zu sehen an der vermehrten Hautpigmentierung.
© Science Photo Library/Biophoto Associates
Der Signalweg von JAK* und STAT** ist maßgeblich an der Pathogenese der akuten Graft-versus-Host-Erkrankung (aGvHD) beteiligt. Denn er fördert Immunzellen und Entzündungsreaktionen im Gewebe, einschließlich der Aktivierung von dendritischen Zellen und Neutrophilen sowie der Expression inflammatorischer Zytokine. Nach positiven Phase-2-Daten untersuchten deshalb Forscher um den Onkologen Professor Dr. Robert Zeiser von der Uniklinik Freiburg den JAK1/2-Inhibitor Ruxolitinib in der internationalen Phase-3-Studie REACH2 bei Menschen mit schwerer aGvHD.
Sie randomisierten 309 steroidrefraktäre Patienten entweder zu Ruxolitinib oder zu einer vom behandelnden Arzt ausgewählten Option aus…
Bitte geben Sie Ihren Benutzernamen und Ihr Passwort ein, um sich an der Website anzumelden.