„Sehr gute Aufklärung ist wesentlich“
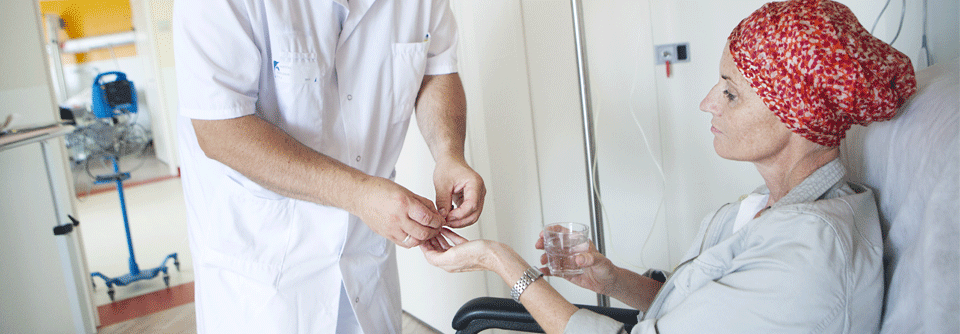
 Nicht nur Chemotherapien können sich negativ auf die Herzgesundheit auswirken. Auch Checkpoint- oder Wachstumsfaktorenhemmer bergen Risiken.
© iStock/Hanna Sova
Nicht nur Chemotherapien können sich negativ auf die Herzgesundheit auswirken. Auch Checkpoint- oder Wachstumsfaktorenhemmer bergen Risiken.
© iStock/Hanna Sova
Professor Dr. Stephan Baldus, Präsident der Deutschen Gesellschaft für Kardiologie, erläutert, wie sich die Effekte minimieren lassen und eine Langzeitbetreuung aussehen sollte.
Sowohl klassische Zytostatika als auch moderne Krebsmedikamente können Herz und Gefäße schädigen. Gibt es Beispiele, die in der Klinik besonders relevant sind?
Professor Dr. Stephan Baldus: Das klassische Beispiel sind Anthrazykline. Diese seit Jahrzehnten angewendeten Chemotherapeutika induzieren Strangbrüche in der DNA und stoppen damit das Zellwachstum. Aber sie schädigen auch die Mitochondrien und beeinträchtigen so den Energiehaushalt der Zellen, und sie generieren aggressive Radikale. All diese Effekte können zu einer Schädigung von Herzmuskelzellen führen – die gefürchtete Folge ist eine Herzinsuffizienz.
Eine neue Klasse von Medikamenten, die ebenfalls kardiotoxisch wirken kann, sind Checkpoint-Inhibitoren. Diese hochwirksamen Substanzen werden von onkologischen Patienten insgesamt sehr gut vertragen, aber in seltenen Fällen tritt eine schwerwiegende Herzmuskelentzündung auf. Warum und bei welchen Patienten es zu dieser Nebenwirkung kommt, muss weiter geklärt werden. Aber auch eine Bestrahlung kann den Herzmuskel schädigen und eine Bindegewebsproliferation im Herzen induzieren. Die Blutgefäße können durch Strahlung ebenfalls geschädigt werden. Arteriosklerose der Koronargefäße bis hin zum Herzinfarkt sind mögliche Folgen.
In einem 2020 publizierten Konsensuspapier1 wird die Erhebung individueller kardiovaskulärer Risikoprofile als Basismaßnahme vor der Planung kardiotoxischer Therapien genannt. Wie genau gehen Sie vor?
Prof. Baldus: Es ist klar, dass Patienten mit bekannten Herz-Kreislauf-Erkrankungen vor einer onkologischen Therapie bezüglich ihres kardiovaskulären Zustands neu untersucht werden und beim Einsatz kardiotoxischer Medikamente engmaschig kontrolliert werden müssen. Das gilt zum Beispiel für den Fall, dass ein Patient mit einer Herzschwäche eine Checkpoint-Inhibitor-Therapie erhalten soll. Aber auch Patienten ohne Anamnese für Herz-Kreislauf-Erkrankungen sollten vor dem Einsatz eines solchen Inhibitors entsprechend untersucht werden.
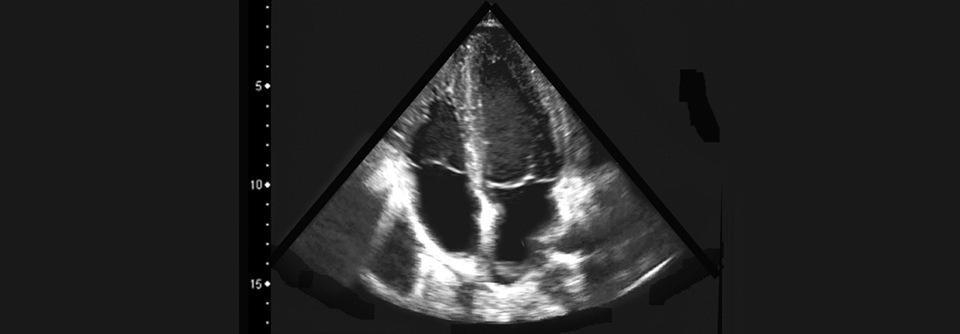
Ist auch eine bildgebende Herzdiagnostik erforderlich?
Prof. Baldus: Ja, primär wird eine Echokardiographie durchgeführt und je nach Befund eine weiterführende Bildgebung, in Einzelfällen auch eine Kernspintomographie des Herzens.
Sind genetische oder andere Biomarker bekannt, die eine Abschätzung des therapiebedingten kardiovaskulären Risikos erlauben?
Prof. Baldus: Genetische Biomarker, die eine Gefährdung des Patienten spezifisch vorhersagen, gibt es bisher nicht. Aber Biomarker, die die Volumenbelastung der Herzkammern oder auch einen Myokardzelluntergang anzeigen, sind wichtige Hilfen in der Einschätzung des Risikos des Patienten. Beispiele dafür sind natriuretische Peptide oder Troponin.
Sie nennen im Konsensuspapier drei Risikogruppen, die einer engen kardiologischen Mitbetreuung unter der Krebstherapie bedürfen. Welche sind das?
Prof. Baldus: Das sind erstens Patienten, die schon herzkreislauferkankt sind. Zweitens Patienten nach einer Bestrahlung des Brustkorbs, etwa bei Mammakarzinom, oder nach einer systemischen Chemotherapie mit bekanntem Risiko für das Herz-Kreislauf-System. Ein Beispiel dafür sind Anthrazykline mit dem Risiko für die Entstehung einer Herzschwäche. Und die dritte Risikogruppe sind Patienten vor einer geplanten Chemotherapie mit erhöhtem Risiko für Nebenwirkungen im Bereich des Herz-Kreislauf-Systems. Anthrazykline hatte ich genannt, aber auch Wachstumsfaktorenhemmer oder Checkpoint-Inhibitoren gehören dazu.
Welche Maßnahmen sind geeignet, auf der Basis der individuellen Risikoprofile kardiotoxische Nebenwirkungen zu minimieren?
Prof. Baldus: Ganz wichtig ist die maximale medikamentöse Therapie kardiovaskulärer Grunderkrankungen. Ein Patient mit vorbestehender Herzschwäche sollte eine optimale Herzinsuffizienz-Therapie erhalten, bei einer Person mit bekannter Koronarkrankheit sollten Blutdruck und Lipidspiegel optimal eingestellt werden.
Gibt es für die Prävention gegen bestimmte kardiotoxische Effekte von Krebsmedikamenten Optionen einer medikamentösen Prophylaxe?
Prof. Baldus: Nein, bisher leider nicht. Eine prophylaktische Behandlung beispielsweise mit Medikamenten gegen Herzschwäche vor einer onkologischen Therapie, die potenziell Herzschwäche provoziert, hat bisher keinen präventiven Nutzen erbracht.
Können Patienten selbst etwas zum Herzschutz beitragen?
Prof. Baldus: Ja, unbedingt. Ein Beispiel: Eine Patientin mit Brustkrebs profitiert unter bestimmten Bedingungen ganz erheblich von einer Strahlentherapie. Wenn diese Patientin aber raucht, erhöht sie damit nicht nur das Risiko von Lungenkrebs durch die Bestrahlung, sondern auch das Risiko von Verengungen der Herzkranzgefäße und Herzinfarkten. Bei Raucherinnen ist der sterblichkeitsreduzierende Nutzen der Bestrahlung bei Brustkrebs aufgehoben!
Stichwort „Survivorship-Programme“: Welche Bedeutung hat die Langzeitbetreuung onkologischer Patienten mit Blick auf kardiovaskuläre Erkrankungen? Empfehlen Sie regelmäßige Check-ups?
Prof. Baldus: Das ist ein wichtiger Punkt. Während Chemotherapien im klassischen Sinn meist nur kurzzeitig appliziert werden, sind moderne Immuntherapien häufig chronische Behandlungsformen. Die Konsequenz ist, dass diese Patienten lebenslang unter Beobachtung bleiben müssen. Das gilt nicht nur mit Blick auf die Tumorerkrankung, sondern auch für mögliche Langzeitnebenwirkungen wie kardiotoxische Effekte.
Immer mehr Tumorpatienten haben ja heute eine relativ hohe Lebenserwartung, sodass sie andererseits auch eher Nebenwirkungen der Krebstherapie erleben, die sich erst langfristig manifestieren. Deshalb sollte man Patienten nach kardiotoxischen Therapien auch langfristig im Auge behalten. Das gilt umso mehr für Kinder. Gerade die oben beschriebenen Anthrazykline können – besonders in Kombination mit einer Bestrahlung – auch noch zehn Jahre nach Beendigung der Therapie Herzschwäche provozieren. Deshalb ist bei Kindern nach einer solchen Therapie eine lebenslange Nachsorge erforderlich.
Brauchen Patienten nach kardiotoxischen Krebstherapien eine Schulung – etwa mit Blick auf das Wahrnehmen von Kontrolluntersuchungen oder das Erkennen von Anzeichen einer kardiovaskulären Schädigung?
Prof. Baldus: Ja, ich halte eine sehr gute Aufklärung für wesentlich. Patienten können viel dazu beitragen, dass eine Schädigung des Herzens frühzeitig erkannt wird. Personen, die eine kardiotoxische Krebstherapie erhalten, sollten wissen, wie sich kardiovaskuläre Funktionsstörungen bemerkbar machen. Oft sind die Beschwerden gar nicht so leicht zuzuordnen. So können zum Beispiel Durchblutungsstörungen des Herzens – abgesehen vom typischen Brustschmerz – auch Schmerzen im Kiefer, Oberbauch und Rücken provozieren.
Ein weiterer Aspekt, der bisher noch gar nicht zur Sprache kam, sind Herzrhythmusstörungen wie Vorhofflimmern. Einerseits haben viele Tumorpatienten vorbestehende Arrhythmien, andererseits können Arrhythmien aber auch eine kardiotoxische Begleiterscheinung moderner onkologischer Therapien sein, zum Beispiel von Kinasehemmern.
Wie ist der Status quo: Werden die Empfehlungen zu Prävention bzw. Management von Kardiotoxizitäten onkologischer Therapien flächendeckend umgesetzt? Ist die Kooperation von Onkologen und Kardiologen schon Standard?
Prof. Baldus: Wir stehen sicher erst am Anfang. Sowohl der onkologischen als auch der kardiologischen Fachgesellschaft ist das Thema in seiner Wichtigkeit bewusst. Jetzt muss es darum gehen, dass wir qualitativ gute Daten erheben. Wir brauchen eine solide Evidenzbasis, um die Patienten in Zukunft noch besser präventiv beraten zu können, sie während der onkologischen Therapie optimal zu betreuen und ihnen anschließend die bestmögliche Nachsorge bieten zu können.
1. Rassaf T et al. Onkologische Kardiologie; Kardiologe 2020; 14: 267-293; DOI: 10.1007/s12181-020-00395-z
Medical-Tribune-Interview
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).