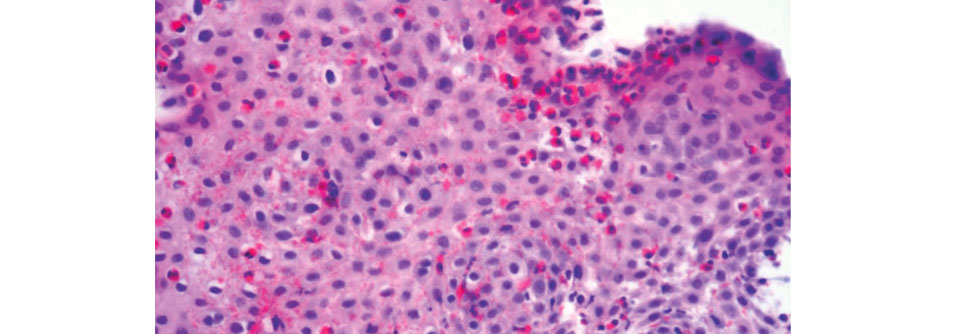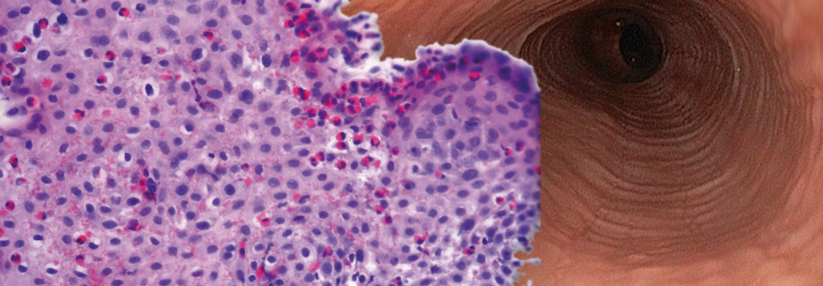
Was therapeutisch bei eosinophiler Ösophagitis möglich ist
 Nach Aktivierung durch eine antigenpräsentierende Zelle schüttet die T-Helferzelle Interleukine aus.
© Science Photo Library/Gaertner, Juan
Nach Aktivierung durch eine antigenpräsentierende Zelle schüttet die T-Helferzelle Interleukine aus.
© Science Photo Library/Gaertner, Juan
Bei eosinophilen Erkrankungen spielen T-Helferzellen vom Typ 2 (Th2) eine bedeutende Rolle. Die Th2-Reaktion führt zu einer vermehrten Produktion von Zytokinen wie Interleukin(IL)-4, IL-5 und IL-13. Entsprechende Antikörper werden derzeit in klinischen Studien geprüft. Professor Dr. Robert D. Pesek, pädiatrischer Allergologe von der University of Arkansas in Little Rock und Dr. Sandeep K. Gupta, pädiatrischer Gastroenterologe des University of Illinois College of Medicine in Peoria haben den aktuellen Forschungsstand in einer Übersichtsarbeit zusammengetragen.
Interleukine als Targets
Dupilumab bindet an die α-Untereinheit des IL-4-Rezeptors und blockiert so sowohl den IL-4- als auch den IL-13-Signalweg. In einer randomisierten, placebokontrollierten Phase-2-Studie führte die Therapie von Patienten mit eosinophiler Ösophagitis (EoE) mit Dupilumab (subkutan, 600 mg Startdosis, dann 300 mg wöchentlich) über insgesamt zwölf Wochen zu einer deutlichen Verbesserung von Dysphagie, endoskopischen Befunden und den Spitzen-Eosinophilenzahlen im Vergleich zu Patienten, die Placebo erhielten. Eine Phase-3-Studie mit Erwachsenen und Adoleszenten soll 2023 abgeschlossen sein. Außerdem wird Dupilumab für die Indikation eosinophile Gastritis untersucht.
Mögliche Therapieoption für steroidrefraktäre Patienten
Zwei bislang noch nicht auf dem Markt befindliche Antikörper bedienen sich ausschließlich des IL-13-Wegs:
- QAX576 bindet direkt an IL-13 und hemmt so dessen Aktivität sowie die Produktion des Chemokins Eotaxin. In einer randomisierten, placebokontrollierten Studie an Erwachsenen mit EoE führte die Behandlung mit QAX576 zu einer Reduktion der mittleren Eosinophilenzahl im proximalen und distalen Ösophagus um 60 %. Unter Placebo betrug die Abnahme 23 %.
- RPC4046 hemmt die IL-13-Bindung an der α1- und der α2-Untereinheit des IL-13-Rezeptors. In einer randomisierten, placebokontrollierten Studie erhielten erwachsene Patienten mit EoE entweder 180 oder 360 mg des Inhibitors oder Placebo über 16 Wochen. Zu Studienende wiesen mehr als die Hälfte der mit RPC4046 behandelten Patienten weniger als 15 Eosinophile pro Gesichtsfeld (high-power field, HPF) auf. In der Placebogruppe war das bei keinem Patienten der Fall. Auch endoskopische und histologische Befunde sowie patientenberichtete Endpunkte verbesserten sich durch den Antikörper im Vergleich zu Placebo signifikant. Der Wirkstoff könnte eine wichtige Alternative für die Therapie steroidrefraktärer Patienten sein. Denn diese sprachen ähnlich gut auf die Behandlung an wie steroidempfindliche.
Die IL-5-Antikörper, die für die Therapie des eosinophilen Asthmas bereits auf dem Markt sind, wurden und werden auch bei EGID untersucht. Studien zu Mepolizumab prüften das Erreichen des primären Endpunkts einer Eosinophilenzahl von unter 5/HPF bei Patienten mit EoE. Dieser Endpunkt wurde bei Erwachsenen nicht und bei Kindern nur selten erreicht, wenngleich die Eosinophilenzahlen deutlich und gegenüber der Placebogruppe auch signifikant gesenkt wurden. Der klinische und endoskopische Befund verbesserte sich nur bei Erwachsenen.
Reslizumab wurde randomisiert und placebokontrolliert in drei Dosierungen bei Kindern und Adoleszenten mit EoE untersucht. Die Spitzen-Eosinophilenzahlen konnten mit dem Antikörper gegenüber Placebo signifikant gesenkt werden, im Hinblick auf klinische Symptome oder die Lebensqualität gab es keinen Unterschied. Sechs Patienten setzten die Behandlung über weitere sechs bis sieben Jahre fort. Bei ihnen zeigte sich im Verlauf eine Verbesserung der klinischen Symptome sowie eine Reduktion der Eosinophilenzahlen im Vergleich zu Placebo.
Studien mit Benralizumab zur Therapie der eosinophilen Gastritis oder der EoE laufen oder sind in Planung. In einer Studie an Patienten mit hypereosinophilem Syndrom erreichten die sieben Teilnehmer mit einer Eosinophilie des Magen-Darm-Trakts eine nahezu komplette Rückbildung der Entzündung (≤ 1 Eosinophil/HPF).
Antikörper gegen Siglecs, Integrine, IgE
Sialinsäurebindende immunglobulinähnliche Lektine (Siglecs) spielen eine Rolle bei der Zellkommunikation und der Regulation des Immunsystems. Siglec-8 wird vorzugsweise von Eosinophilen, Basophilen und Mastzellen exprimiert. Der Anti-Siglec-8-Antikörper AK002 führte in einer Phase-2-Studie mit Erwachsenen mit eosinophiler Gastritis oder eosinophiler Gastroenteritis zu einer 95%igen Reduktion der Gewebe-Eosinophilen. In der Kontrollgruppe kam es zu einem 10%igen Anstieg. Die Eosinophilen-Reduktion ging mit einer signifikanten Linderung der Symptome einher.
Anti-IgE-Therapie bislang ohne nennenswerten Erfolg
Der monoklonale Antikörper Vedolizumab bindet an α4β7-Integrine auf Lymphozyten und verhindert deren Bindung an Endothelzellen. In einer Fallserie konnten steroidbehandelte Patienten mit eosinophiler Gastritis oder Gastroenteritis unter Vedolizumab die Dosis systemischer Steroide verringern oder diese ganz absetzen. Eine Kohortenstudie wies auf eine klinische und histologische Wirksamkeit von Vedolizumab bei steroidrefraktären Patienten hin.
Studien, die die Effektivität von Anti-IgE-Therapien untersuchen, blieben bislang ohne klare Ergebnisse. Zwar weisen Untersuchungen darauf hin, dass IgE bei der eosinophilen Ösophagitis eine Rolle spielen und entsprechende Antikörper wirksam sein könnten, so die Autoren. Bisherige Daten dazu waren allerdings nicht überzeugend.
Altbewährtes in neuem Gewand
Ein alter Hase in der Therapie eosinophiler Erkrankungen ist die systemische Behandlung mit Steroiden. Vor nicht allzu langer Zeit wurde eine Budesonid-Schmelztablette zur EoE-Therapie zugelassen. Die Wirksamkeit und Sicherheit einer orodispersiblen Fluticason-Formulierung wird derzeit in Studien geprüft.
Quelle: Pesek RD, Gupta SK. Ann Allergy Asthma Immunol 2020; 124: 219-226; DOI: 10.1016/j.anai.2019.11.018
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).